Sumário
- 1 - Resumo
- 2 - INTRODUÇÃO
- 3 - JUSTIFICATIVA
- 4 - OBJETIVO
- 5 - METODOLOGIA
- 6 - DESCOBERTA DO VIDRO
- 7 - DEFINIÇÃO VÍTREA
- 8 - FABRICAÇÃO DO VIDRO
- 9 - CONSIDERAÇÕES FINAIS
- 10 - Referências bibliográficas
1. Resumo
Este presente trabalho visa em falar sobre o vidro, um material que foi descoberto por acaso pela antiguidade que durante o passar dos anos foram tomando formas e se evoluindo para atender todas as necessidades que são utilizadas por nós diariamente. Durante a sua evolução houve descobertas de como da cor ao vidro e qual a sua definição, que pelo resfriamento forma uma estrutura desordenada e sem periodicidade, mas para lhe dar uma definição concreta houve vários autores e cada um com sua opinião diferenciada sobre o que seria o vidro. Em uma indústria vidreira nos processos de fabricação, cada tipo de vidro é produzido tanto para decoração até para utilidades domésticas e laboratoriais, uma produção com recursos que permitem fabricar os vidros com qualidade. Para fabricar um vidro tem que haver um descarte sem que atinja o meio ambiente, a reciclagem dos vidros, que permite um método de economia e baixo custo de matéria prima, todas as empresas devem ficar atentas para não agredir o meio ambiente, seguindo anexadas as ordens de Gestão Ambiental, um assunto que vem sendo muito discutido pelos defensores do meio ambiente.
Palavras- chave: vidros, origem, definição, métodos.
Abstract
This present work aims at in saying on the glass a material, that was discovered by chance by the antiquity that during passing of the years forms had been taking and if evolving to take care of to all the needs that are used by us daily. During its evolution it had discovered of as of the color to the glass and which its definition, that for the cooling forms a disordered structure and without regularity, but for giving a concrete definition to it had some authors and each one with its differentiated opinion on what it would be the glass. In a glass industry in the manufacture processes, each type of glass is produced in such a way for decoration even for domestic and laboratory utilities, a production with resources that allow to manufacture glasses with quality. To manufacture a glass it has that to have a discarding without it reaches the environment, the recycling of the glasses, that allows to a method of economy and low cost of substance cousin, all the companies must be intent not to attack the environment, following attached the orders of Ambient Management, a subject that comes very being argued for the defenders of the environment.
Keywords: glasses, origin, definition, methods.
2. INTRODUÇÃO
Convivemos diariamente com o vidro ao nosso redor, presente em qualquer lugar de nossa casa, ou no trabalho, na rua e etc, tendo se varias utilidades como em janelas, em copos, vasilhas, mesa, lente dos óculos, binóculos e muitos outros objetos aplicados com varias formas e cores.
Ter o vidro para atender a suas necessidades, deixa despercebido que vem sendo utilizados pelo homem há muitos anos e que desde a sua descoberta teve muitas evoluções na fabricação e estudos para definir sobre o que ocorre quimicamente com o vidro quando fabricados ou utilizados na presença de altas e baixas temperaturas.
Aprender mais profundamente sobre o tema específico é abrir a mente para novos esclarecimentos sem gerar desconfianças ou duvidas, temos que dar uma nova oportunidade para a mente em leituras e pesquisas e não pensar que o vidro é somente um objeto. Por estes motivos me incentivou a estudar e conhecer quimicamente bem mais a fundo sobre este tema, que através de pesquisas e leituras tive conhecimentos em geral de como o vidro não é só um material, mas sim um objeto de estudo que merece ser explorado.
Adquiridos em teses com temas vítreos pela internet, livros de química geral e engenharias dos materiais, foi descrito nesse trabalho de conclusão de curso toda sabedoria de vários autores, um momento de saber o que realmente é o vidro.
O trabalho subdivide em três capitulo, na qual:
No capitulo 1- aborda, que por acaso o Fenicios na antiguidade descobriram o vidro e expandiu pelo mundo todo com evoluções e métodos para a melhora de uso do vidro. E também fala de como se deu a indústria vidreira no Brasil.
No capitulo 2- será abordada uma definição vítrea e que por vários autores teve opiniões diferenciadas e definiu como se dá o vidro quimicamente, também relata a transição vítrea pelo gráfico de volume x temperatura. Ainda no mesmo capitulo acrescenta sobre como os vidros são formados pelos óxidos, e como se cor e descolore o vidro, para completar os vários tipos de vidros existentes.
No capitulo 3- finaliza sobre os processos envolvidos em uma fabricação vidreira, propondo somente os quatros processos mais importante para se produzir o vidro e encerra com o método de reciclagem que ultimamente entrou em discussão com defensores do meio ambiente, implantando a ordem de Gestão Ambiental para não atacar a natureza.
3. JUSTIFICATIVA
Diariamente convivemos muito com o vidro, porem a curiosidade do saber sobre a origem, definição, fabricação e método de reciclagem, me moveu a pesquisas e relatar neste trabalho de conclusão do curso tudo sobre o vidro. E juntamente com leituras para os temas vítreos cedidos pela a internet e livros disponíveis na biblioteca e mais as aulas ministrada pelo corpo docente pela Instituição Faculdade de Campo Limpo Paulista me convenceu a explorar sobre este tema, e ter um conhecimento mais químico do vidro.
4. OBJETIVO
Demonstrar um conhecimento geral do vidro, como foi dada a descoberta na antiguidade pelos Fenicios e sua evolução na fabricação vidreira. Dar uma definição dos vidros, de como acorre à transição vítrea e a coloração, e falar os tipos de vidros produzidos. Finaliza falando como é o processo de fabricação na indústria vidreira e métodos de reciclagem para não prejudicar o meio ambiente.
5. METODOLOGIA
Através de livros disponíveis na biblioteca pela Instituição Faculdade de Campo Limpo Paulista foram realizadas pesquisas e leitura para descrever este trabalho.
Também pelo Google Acadêmico pude encontrar tese com temas vítreos e artigos da Química Nova. Outra colaboração foi feita pela tese da Professora Doutora Lisete Maria Luiz Fischer para dar complementos a este trabalho de conclusão de curso.
6. DESCOBERTA DO VIDRO
Conta-se de uma história lendária, em uma referência encontrada na História Natural de Plínio, comerciantes Fenícios que viajavam pelo Rio Belo, na Síria, desembarcaram nas margens arenosas. Para se alimentar improvisaram um fogão com bloco de soda e salitre, algum tempo depois foi observado que no meio dessa fogueira escorria um liquido brilhante que se solidificava rapidamente. Até esse momento o vidro era conhecido como ‘’Obsidiana’’, pelas rochas vulcânicas tinha o vidro natural, que eram feitas flechas, ponta de lanças e facas.
Figura 1- Descoberta do Vidro pelos Fenícios.

Fonte: Costa, 2006.
Tinha então se descoberto o vidro, que por volta de 5000 AC, os egípcios já começavam a fabricar os vidros, eram contas opacas e coloridas encontradas em túmulos de faraós, com pouca utilidade o vidro era usado como enfeite, sendo também já comercializados pelos Fenícios em toda Síria e Fenícia. Passado algum tempo os egípcios descobriram que podiam fazer com vidro vasos e copos, com o vidro fundido filetes eram enrolado sobre um molde de argila, depois que o vidro esfriava retiravam a parte da argila do interior e obtia-se uma peça oca. Nessa época eram comercializados somente aos nobres, devido ao alto custo.
Já em 300 DC, na fabricação de vidro foi descoberto o método do sopro, em uma barra de ferro com aproximadamente 100 a 150 cm de comprimento, com uma abertura de 1 cm de diâmetro (Alves; Gimenez; Mazali, [s.d.]), era colhido por essa barra uma bolha de vidro, um liquido viscoso, sopravam sobre essa barra e dava-se molde ao vidro, formando uma peça oca, o vidro não era transparente, mas sim colorido pela contaminação de ferro na cor esverdeado.
Figura 2. Fabricação pelo método do sopro.

Fonte: Costa, 2006.
Também a partir de gotas, colhidas nas pontas de tubos e sopradas, passou-se a produzir vidro plano. Depois que a bolha estava grande, cortava-se o fundo, deixando a parte que estava presa no fundo e, com a rotação deste, produzia-se um disco de vidro plano, que eram utilizadas para fazer vidraças e vitrais (Martins; Pinto, 2004). Com esse método do sopro a fabricação do vidro ficou mais amplo e conhecido mundialmente, tanto que por segurança a indústria vidreira mudou-se para a Ilha de Murano, para que não fossem expostos os conhecimentos da fabricação do vidro, caso os vidreiros dessa indústria precisassem se ausentar por motivos maiores, eram rigorosamente vigiados e se não voltassem no tempo determinado, corriam o risco de morrerem. Na ilha houve uma nova descoberta, vidros muito transparentes, finos e claros, denominados como “Cristallo”, característicos de um cristal. Foi então, que criaram lentes e inventaram binóculos (1590) e telescópios (1611), e começaram grandes pesquisas do universo. Na mesma época a química tem uma evolução devido a recipientes especiais e termômetros de laboratórios.
Data já em 1665, na França, sob o reinado de Luz XIV, foi fundada uma indústria vidreira, secretamente vidreiros venezianos conseguiram fugir para a França, com grandes conhecimentos na Ilha de Murano, os franceses começam suas próprias produção de vidros, dando-lhe continuidade do método do sopro e do vidro plano para produzir espelhos, mas sem sucesso os franceses ainda davam preferência à vidraria veneziana, e mesmo com uma lei proibindo a importação de espelhos venezianos, os franceses conseguiam comercializá-los ilegalmente, porem, a indústria francesa teve novas evoluções para os espelhos e acabaram sendo aceitos nacionalmente e sendo utilizados para decoração.
Assim deu-se a continuidade da fabricação do vidro e cada vez mais o vidro foi se evoluindo e criando novas técnicas para a indústria.
Em 1612 publicado por Neri, em Florença, teve-se exposto o primeiro trabalho sobre a Tecnologia do vidro, “L’Art Vittraria” , foi traduzida para o latim e outras línguas vernaculares, à partir daí foram empregadas grandes estudo sobre a Tecnologia do Vidro. Em 1675 descobriu o emprego de óxido de chumbo no vidro, e a durabilidade química com a ação da água e de ácidos fracos por Schawb, Scheele e Lavousier.
Para dar continuidade ao desenvolvimento e estudos sobre o vidro à tabela 1 mostrará com mais detalhes referente aos últimos 300 anos
Tabela 1. Nos últimos 300 anos estudos e desenvolvimento do vidro.
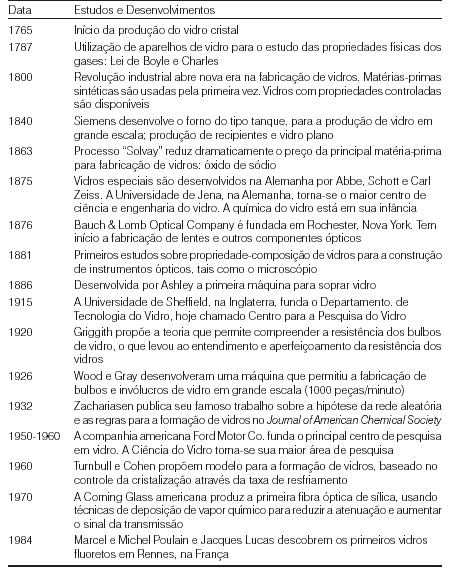
Fonte: Alves; Gimenez; Mazali, 2001.
6.1. Indústria vidreira no Brasil
No Brasil com a chegada dos vidreiros holandeses, em Pernambuco, pode-se produzir as primeiras peças de vidros como janelas, copos e frascos, porem, com a expulsão dos holandeses a indústria no país teve uma queda.
No século IX, algumas indústrias de vidros tentaram as instalações no Brasil para produção de vidros, mas umas tiveram sucesso e outras não sucederam.
Com grandes indústrias já instaladas no país, foi introduzida a fabricação de vidro em moldes indústrias, nessas indústrias eram fabricados desde garrafas até os serviços com cristal, produtos de boa qualidade igualados aos europeus. Houve o primeiro desembarque de mercadorias da Europa no Rio de Janeiro, foram descarregadas caixas de cerveja de origem alemã, onde os brasileiros começaram a degustar as cervejas em garrafas de vidro. No ano de 1895, em São Paulo, é fundada a Vidraria Santa Marina, que já produzia garrafas de vidro.
Começa então os crescimentos das indústrias de vidros no Brasil no fim do século de IX. Com esse crescimento o Brasil vai progredindo com fabricação de vidros planos nas indústrias automobilísticas e construção civil, diversificando também em outras áreas.
7. DEFINIÇÃO VÍTREA
Para umas das primeiras definições do vidro, Michael Faraday em 1830, explica os vidros como sendo materiais “mais aparentados a uma solução de diferentes substâncias do que um composto em si” (Vieira, 2008). Este conceito foi baseado na idéia de que o vidro pode ser formado com a viscosidade, devido à preparação por fusão/resfriamento, que não seja submetida às forças moderadas, pois no critério da viscosidade um sólido é um material rígido. Então com base nesse conceito pode-se dizer que o vidro um produto inorgânico fundido ao atingir uma condição rígida por resfriamento, não ocorre à cristalização.
Mas adiante com os estudos para esclarecimentos dos vidros, tem também o conceito de Zachariasen, em 1932, com um artigo publicado The Atomic Arrangement in Glass (O Arranjo Atômico em Vidros), ele afirma que “dever ser francamente admitido, que não conhecemos praticamente nada sobre os arranjos atômicos dos vidros”. Caracterizado por uma rede bidimensional estendida com ausência de simetria e periodicidade ele propôs o arranjo atômico, e completou que as forças atômicas eram comparáveis a do cristal, e que a ausência de simetria e periodicidade diferencia um vidro do cristal.
De acordo com a figura 3, ele representa uma rede bidimensional para (a) arranjo atômico cristalino simétrico e periódico de um cristal e a (b) rede desordenada do vidro com ausência de simetria e periodicidade a longo alcance posicional, ambas para o composto A2O3.
Figura 3: Representação bidimensional de Zachariasen: a) arranjo de um cristal assimétrico e periódico e b) rede de um vidro sem periodicidade e simetria.
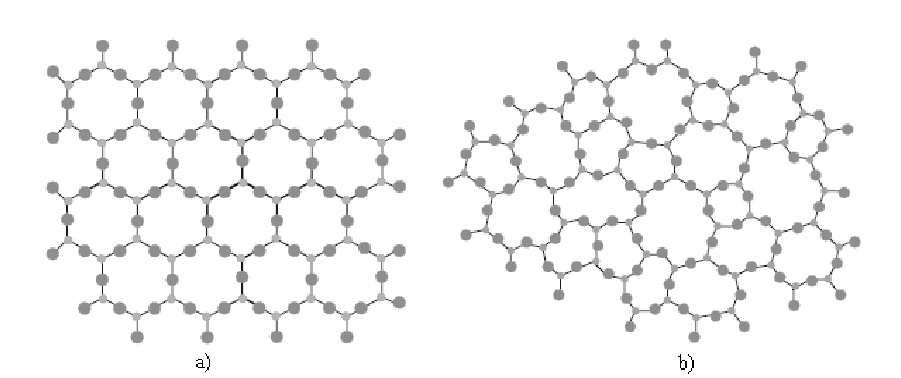
Fonte: Gordo, 2010.
Para uma definição mais moderna por Gupta, em 1996, em seu artigo publicado Non-Crystalline Solids: Glasses and Amorphous Solids (Sólidos Não- Cristalinos: Vidros e Sólidos Amorfos), diz que essas expressões não seriam sinônimas e sim um conceito específico. Gupta diz que um sólido- não cristalino pode ser divido do ponto de vista termodinâmico em duas classes: vidros e sólidos amorfos. Os materiais que apresentam uma rede tridimensional estendida e aleatória, isto é, com ausência de simetria e periodicidade translacional são os sólidos não- cristalinos (Gimenez; Mazali; Alves, [s.d.]). Supondo um aspecto termodinâmico, um sólido não- cristalino é o vidro que apresenta o fenômeno de transição vítrea (Tg). Que consequentemente, sólidos amorfos são sólidos não- cristalinos que não demonstra um fenômeno de transição vítrea (Gimenez; Mazali; Alves, [s.d.]).
De acordo com a tabela 2, Gupta resumidamente com a definição para vidro apresenta uma imprecisão por considerar os vidros como sólidos amorfos.
Tabela 2: Definição de vidros por outros autores na década de 90.

Fonte: Alves; Gimenez; Mazali, 2001.
Acredito que para uma definição ao vidro, um produto inorgânico obtido por fusão foi resfriado a uma condição rígida sem que ocorra a cristalização, com uma característica de transição vítrea.
O cristal quando começa a se fundir, os arranjos atômicos com ordem assimétricos e periódicos lentamente com a solidificação vão se expandindo para uma distância de longo alcance, com a fundição do cristal conforme cresce o volume, tem-se o aumento da temperatura até uma fusão constante, porem, abaixo dessa temperatura de fusão, há um liquido viscoso, esse liquido rapidamente é resfriado e tem a formação do vidro, com o resfriamento rápido os arranjos atômicos fixam- se de uma forma desordenada, conforme a Figura 4 se for dado à continuidade do aquecimento, terá se um liquido e uma viscosidade menor, tendo o risco de ocorrer a desvitrificação, uma nova formação de cristais, mas para não acontecer tem-se uma quebra fazendo do liquido super-resfriado.
Em temperaturas mais baixas na curva sobre volume versus temperatura ocorre um desvio e muda de inclinação como na temperatura de fusão, Tf, semelhante ao de cristal, essa curva é a temperatura de transição vítrea, Tg ou temperatura de transformação.
Figura 4: Demonstração para a formação dos vidros.
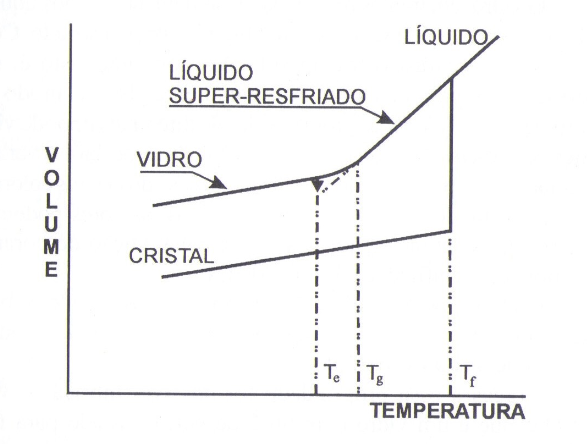
Fonte: Maia, 2003.
Abaixo da temperatura de Tg já não se apresenta mais um liquido, mas sim o vidro. Se olharmos para o gráfico será observado que o volume do vidro com uma certa temperatura fica maior que o volume do cristal, mostrando que a estrutura do vidro é mais aberta que a do cristal. Se a temperatura for abaixada lentamente o vidro será contraído até o volume de corresponder um ponto na curva de equilíbrio, que pode ser identificado como estabilização, Te.
7.1. Formação para Vidros Óxidos
Zachariasen propôs que os vidros óxidos apresentam uma estrutura tridimensional, sem periodicidade e simetria, e ainda completou que para ser um formador de rede teriam que se adequar as quatros seguintes regras:
-
cada oxigênio não pode ligar a mais de dois cátions de metal;
-
cada átomo de metal não pode ligar-se a mais de quatro átomos de oxigênio;
-
os poliedros de coordenação devem se ligar pelas vértices e não pelas arestas e faces;
-
cada poliedro de coordenação deve se compartilhar a três ou mais vértices.
Seguindo essas regras os óxidos que apresentam a formula química AO e A2O não são adequados para a formação de um vidro, mas caracterizando os A2O5 e AO5 podem apresentar uma formação de estrutura vítrea e sendo A2O3 são formadores intermediários.
Ainda para a formação dos vidros, Sun com sua teoria baseou-se com a importância nas ligações atômicas entre os cátions formadores e os oxigênios rodeados. A sua teoria conclui que óxidos com uma energia de ligação entre 80 e 120 kcal/mol tem uma tendência maior em formar os vidros, denominado em formadores de rede. Os que apresentam uma menor tendência na energia de ligação entre 10 a 60 kcal/mol são os modificadores, e para os intermediários tem uma energia de ligação entre 60 a 80 kcal/mol.
7.2. Óxidos Formadores de Rede
São óxidos que formam ligação iônica, para a formação da rede a sílica, SiO2, com uma rede tridimensional de tetraedros de silício- oxigênio (SiO4), torna-se uma componente principal do vidro, ligado pelas vértices, um íon silício se faz o centro em um tetraedro unido a quatro oxigênio e cada um desses a um outro íon de silício (Maran, 2010.), detalhadamente na figura 5.
Figura 5: Rede sílica SiO4; a) estrutura cristalina e b) estrutura vítrea.
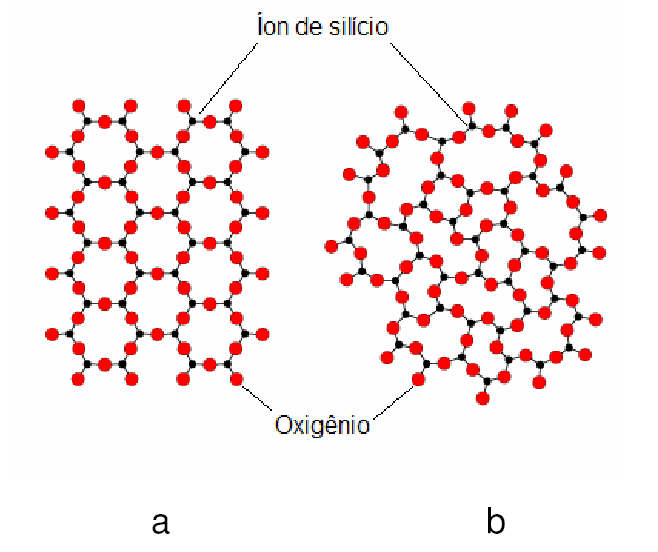
Fonte: Maran, 2010.
Os óxidos B2O3, SiO2, GeO2 e P2O5 são formadores de rede por serem capazes de formar sólidos não-cristalinos sozinhos, já os As2O3 e Sb2O3 também formam um reticulado, e submetidos a altas taxas de resfriamento farão sólidos não- cristalinos. Óxidos TeO2, SeO2, MoO3, WO3, Bi2O3, Al2O3, Ga2O3 e V2O5 também é aceito como formadores de rede ou modificadores de rede. Os vidros formadores de rede apresentam alta viscosidade e alta temperatura de fusão.
7.3. Óxidos Modificadores de Rede
Para os óxidos modificadores de rede tem a participação dos metais alcalinos e alcalino- terrosos, não participam diretamente da estrutura, pois enfraquecem as ligações que se ajustam melhor nos interstícios.
Para melhor visualização de um óxido modificador de rede observa-se a figura 6, com uma rede estrutural do SiO2-Na2O, tem se a formação na estrutura um par SiO-, que se dá devido ao modificador Na2O adicionado ao SiO2, com a ação do modificador na estrutura do SiO2 que rompe a ligação do oxigênio, entre os tetraedros nas ligações Si-O-Si, com essa alteração na estrutura as propriedades do vidro são alteradas.
Figura 6: Rompimento da ligação Si-O-Si pelo modificador Na2O; a) estrutura SiO2 e b) SiO2 após a ação do modificador e formação de um par de oxigênio não ligante.
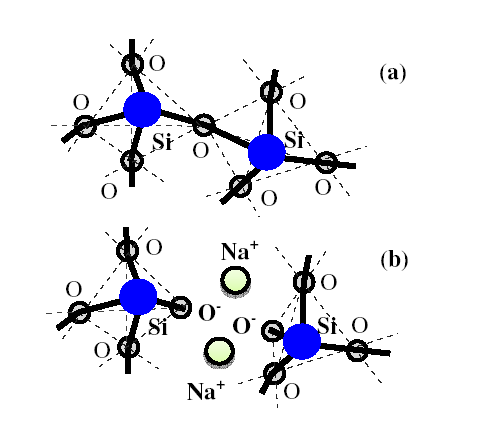
Fonte: Martins, 2009.
Para aumentar a viscosidade e diminuir o ponto de fusão aos óxidos modificadores são acrescentados Al2O3, CaO e MgO.
Como modificadores de rede os óxidos são Y2O3, MgO, CaO, PbO, Na2O.
7.4. Óxidos Intermediários
Óxidos que não participam diretamente na estrutura, agem como intermediários devido capacidade de não formar um reticulo sozinho, podendo fazer uma substituição parcial, também age como modificador de rede rompendo as ligações e diminuindo o ponto de fusão.
Óxidos aceitos como intermediários são TiO2, ZnO, BeO, PbO2 e AlO3.
7.5. Coloração nos Vidros
Uma das características importantes dos vidros são as cores, que podem variar com as tonalidades deixando uma leve transparência ou opacidade. Para a coloração do vidro são usados agentes colorantes.
Em todos os óxidos utilizados as cores mudam em função de uma composição química incorporadas nos processos de misturas e preparação da fusão.
Através de um equipamento chamado calorímetro, pode ser medido o grau de cor nos vidros, depois do vidro pronto são comparadas as cores pelo gráfico, se coincidir as cores o processo da continuidade, caso a cor fuja do esperado são adicionados colorantes até se aproximar a uma certa tonalidade correta que se pede.
Podem ser identificadas as cores nos vidros com absorção pela frequência da luz pelos agentes em solução no vidro, esse óxido são elementos de transição adicionados, principalmente do primeiro grupo. Através de partículas coloidais precipitadas, que de primeira são incolores pelo tratamento térmico, também deixam os vidros coloridos, esse processo a cor desenvolve logo após a fabricação do produto através do reaquecimento. A aparência do vidro opalino é causada pela difusão na luz por causa de pequenas inclusões dispersas na massa. A cor vermelha se deu pelo ouro e cobre, e a cor amarela pela prata.
A tabela 3 são detalhada agentes que dão cor ao vidro.
Tabela 3: Agentes de Coloração para o Vidro.
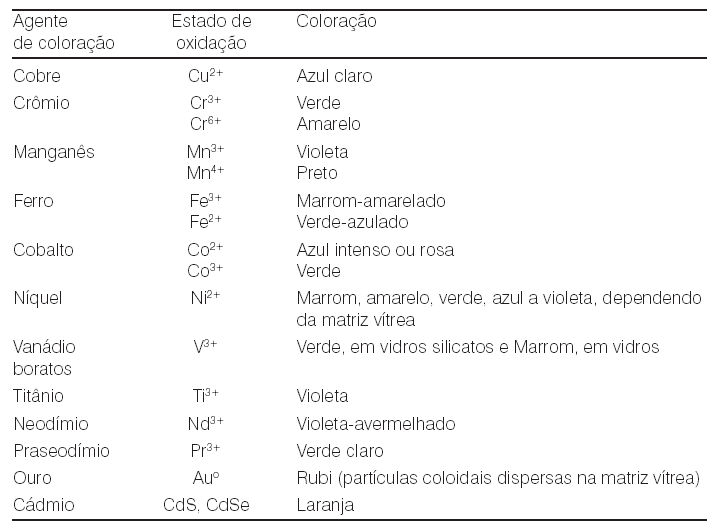
Fonte: Alves; Gimenez; Mazali, 2001.
A descoloração do vidro esta em matérias primas com impurezas de ferro e cromo que lhe dará uma cor esverdeada, com agentes oxidantes como selênio e juntamente com o óxido de cobalto oculta a cor originário do ferro, este procedimento visa descartar uma cor usando outra cor complementar.
7.6. Alguns Tipos de Vidros
São listados abaixo alguns vidros visando melhoras e desenvolvimentos na qualidade, com novas composições e desempenhos variáveis em seus materiais no processo de fabricação vidreira.
7.6.1. Sílica Vítrea
Este tipo de vidro se dá com a preparação do aquecimento de areia de sílica até a temperatura maior que do ponto de fusão da sílica, é identificado pelo baixo coeficiente de expansão que lhe concede uma grande resistência térmica, devido à radiação ultravioleta fica transparente. Aplicado em janelas de veículos, produção de fibras óticas e espelhos astronômicos, em geral para laboratórios de alta tecnologia. Contém 100% de SiO2 e um custo superior.
7.6.2. Silicatos Alcalinos
Para diminuir a viscosidade de um vidro fundido de sílica adiciona um modificador de rede, óxido alcalino, capazes de enfraquecer as estruturas vítreas devido os oxigênio não ligantes.
Solúveis em água, com grandes concentrações e menor resistência química de álcalis são utilizados em adesivos, produtos de limpeza e películas protetoras.
7.6.3. Vidros Sodo- Cálcicos
Esse tipo de vidro é identificado pelo fato de diminuir a solubilidade de vidros alcalinos conservando-se a facilidade de fusão, é acrescentado na composição fluxos estabilizantes, geralmente são utilizados cálcio e óxido de magnésio. Se for adicionado uma quantidade de cálcio a mais o vidro terá uma tendência em cristalizar, caso a quantidade for menor terá pouca durabilidade química. Sua aplicação esta em garrafas, frascos, potes, janelas, bulbos e tubos de lâmpadas.
7.6.4. Vidros de Chumbo
Possui uma propriedade de absorção de raios-X com adição de óxido de chumbo nos processos da indústria. Com alto teor de PbO são usados como protetor e diminui as radiações gama. Pode se um modificador de rede, mas dependo da composição também agem como um formador de rede, diminuição da temperatura altera a viscosidade.
Importante característica de alto índice de refração para dar mais brilho ao vidro, fabricado para cristais e artigos decorativos com alto custo e também utilizados em ótica.
7.6.5. Vidros Borossilicatos
Contendo B2O3 o resfriamento tem temperaturas de fusão aproximadamente 460°C, os vidros Borossilicatos apresentam grande resistência ao choque térmico com produtos de podem ser levados ao fogo, com baixo coeficiente e estabilidade química, vidros utilizados em laboratórios que resiste ao ataque químico.
7.6.6. Vidros Opalinos
Com formas minúsculas de cristais de CaF2 exibe se a opalescência no vidro, com densidades no meio transparente, que difundem a luz incidente. (Sherve; Brink, 1997)
7.6.7. Vidros Especiais
São vidros coloridos, vidros cerâmicos, vidros temperados, fibra de vidro, vidro ótico, vidro fotossensível e que tenham diferentes aplicações.
8. FABRICAÇÃO DO VIDRO
Para a fabricação do vidro é necessário fundir a matéria prima a altas temperaturas adequadamente para obter o vidro fundido. Temperaturas altas são importantes, pois reduz a viscosidade de um vidro fundido e tira as bolhas realizadas. Há quatro etapas principais para a fabricação, subdivididas em:
8.1. Fusão
Transformar matéria prima em vidro é iniciar se o calor em fornos de vidros, todos os processos são revestidos na operação e qualidade do vidro fabricado. Os fornos de vidros são distinguidos pela geometria, pela maneira como o vidro foi colhido, pelo tipo de separação entre zonas de fusão, no interior a localização e direção das chamas e pelo modo como o calor da combustão é recuperado, para cada tipo de vidro produzido. Fornos de cadinho e forno- tanque são determinados para os fornos de vidro.
Os fornos de cadinho tem produção de vidros especiais, ou é essencial para proteger banho fundido da ação dos produtos de combustão, e capacita aproximadamente 2 tonelada ou menos. Aplica-se em manufatura de vidro ótico, vidro artístico e vidro plano em chapa fundida. Pode ter cadinhos de platina ou argila especial. (SHREVE; Brink Jr., 1997)
Em forno- tanque uma grande extremidade do tanque de tijolos refratários, materiais de partida são introduzidos: certos tanques possuem cerca de 38 por 9 por 1,5 metros, tendo capacidade de 1.400 toneladas de vidro fundido. Pela massa liquida o vidro é acumulado sobre chamas alternadas de um lado para o outro. Vidro refinados são retirados do tanque por uma operação continua. Dependendo da qualidade de tijolos, podem ter interferência na duração e qualidade do vidro. Os fornos- tanque são aquecidos eletricamente ou a gás, e propõe uma demanda de 1 a 10 toneladas de vidro fundido diariamente.
Esses fornos são regenerativos e realizam trabalho em dois ciclos, com duas câmaras de regeneração, que alçam altas temperaturas e poupam- se muito calor.
Ao iniciar a produção a temperatura do forno só se aumenta de acordo com a capacidade dos refratários, assim aquecidos a temperatura alcança 1.204°C e precisa ser mantido todo tempo. Devido à radiação do forno, perde se parte do calor e um pouco acaba se desprendendo na fusão, porem se as paredes esfriam por causa da radiação, a temperatura se elevaria e o vidro fundido se dissolveria mais rápido. Esta ação do vidro fundido se diminui usando frequentemente tubos de arrefecimento a água nas paredes do forno. (SHREVE; Brink Jr., 1997)
8.2. Conformação ou Moldagem
O vidro é formado a máquina ou modelado a mão. Na conformação mecânica o que lhe chama a atenção é o modelo da maquina de vidro que tem a capacidade de concluir em segundos alguns objetos. Em um curto tempo o vidro começa a se transformar de um liquido viscoso em sólido transparente. Conformado mecanicamente tem– se os vidros mais comuns, como: vidro de janela, chapa de vidro, vidro por flutuação, garrafas, bulbos de lâmpadas e tubos.
8.3. Recozimento
Para o vidro o recozimento esta em aquecer a uma certa temperatura para eliminar as tensões internas em médio tempo, e logo em seguida esfria-lo para entrar um mínimo possível de tensões. Não é possível recozer o vidro perfeitamente, quando atingido a certa temperatura na faixa de recozimento, ao esfriar uma peça de vidro surgirão tensões na massa, porem parte dessa tensão sumirá, pois é impossível levar a peça de vidro para uma condição elástica (Maia, 2003). Quando recozimento é feito a uma temperatura próxima da superior de recozimento, onde se tem uma viscosidade baixa, rapidamente terá um desaparecimento, pois lentamente deve ser feito o processo de esfriamento, do contrario, o gradiente de uma temperatura determinado no esfriamento causa um esforço que uma certa quantidade desaparece e leva a grandes introduções de esforços residuais logo após ao esfriamento da peça. Por outro lado, com uma temperatura de recozimento menor escolhida, mesmo que tenha um tempo preciso para o vidro se livrar das tensões ainda quente, rapidamente pode se esfriar, pois a viscosidade é maior, portanto, tolerará um gradiente de temperatura grande, sem se ter desaparecimento das tensões e naturalmente um esforço residual.
Em fornos de Lehr são produzidos o recozimento do vidro, e esses fornos são continuas ou estacionárias e podem ser aquecidas a eletricidade, a óleo ou a gás.
Depois de se fabricar uma peça de vidro, inicia- se um resfriamento¸ por causa da má condutibilidade térmica do vidro, partes externas são mais frias que as partes internas e geram tensões que ficam na peça logo após atingir a temperatura ambiente. Causadas por essas tensões certas peças são quebradas em estilhaços ou tem somente rachaduras que acontece com uma pequena batida. ( Maia, 2003)
Reduz-se essas tensões aceitavelmente o mínimo que se puder ou suprimi pelo recozimento e eleva a temperatura da peça para um ponto em que o vidro muda do estado elástico para o estado plástico, depois que a temperatura se conserva o suficiente para relaxar as tensões, vagarosamente começa o resfriamento, para tornar uma temperatura com mínima diferença nas partes externas e internas, evitando o reaparecimento das tensões.
Em câmaras de Lehr são feitas o recozimento do vidro que funcionam constantemente. As peças de vidro são transportadas em uma esteira rolante de aço, e durante o percurso aumenta se a temperatura até atingir o estado plástico em um tempo suficiente pra ter as tensões aliviadas, e em seguidas diminui a temperatura gradualmente até a temperatura ambiente.
Essa sequencia de aquecimento e resfriamento tem-se em conta as velocidades de como as peças entram nas Lehr, o tipo de vidro e a espessura. Em fabricas pequenas o recozimento é produzido em Lehr estacionarias, e utilizam técnicas seguras capaz de manter uma temperatura para certas peças de vidro, que depois de resfriar lentamente o forno de recozimento desliga sozinho e deixa naturalmente esfriar sem reaparecimento de tensões para as peças do vidro.
8.4. Acabamento
Depois que as peças do vidro são fabricadas e recozidas são feito os acabamentos, processo simples, porem muito importante. São feitos vários acabamentos como esmerilhamento, polimento, gravação, corrosão ácida, jateamento com areia, esmaltagem, tingimento, pintura com metais preciosos, vidro iridescentes, metalização a vácuo e espelhagem. Nem todos os tipos de vidro recebem esses acabamentos, somente alguns.
8.5. Método de Reciclagem do Vidro
Ultimamente tem- se discutido muito sobre a importância da defesa ambiental. Mobilizado pela sociedade há varias organizações para a conservação do meio ambiente.
Pelo ISO já foi implantado procedimentos e requisitos que estabelecem a segurança do meio ambiente em empresas, à Gestão Ambiental com objetivo de redução de custos, valorização de recursos naturais, reaproveitar e armazenar apropriadamente, tratamento de efluentes industriais e eliminação de efluentes tóxicos.(Maia, 2003).São acompanhados pela Gestão Ambiental processos produtivos e impactos com o meio ambiente.
Na fabricação de vidro são gerados materiais poluentes e liberados mais outros tipos, que necessitam ser observados atentamente para que o meio ambiente não seja atacado. E o homem sempre se atentou em aproveitar cacos de vidros para novas peças com o objetivo de economizar matérias primas.( Maia, 2003)
O vidro é um material que se utiliza varias vezes. No Brasil, em 1985, para reutilização do vidro foi introduzido o primeiro programa racional, existente em muitas cidades programas para a reciclagem do vidro, que para atender as necessidades das fabricas tem uma mão de obra não qualificada.
Os cacos de vidros para a reciclagem resultam-se em vários benefícios:
-
Protege o meio ambiente porque reduz volume do lixão e elimina materiais não perecíveis;
-
Quando aproveitados na fabricação do vidro há uma redução na poluição atmosférica, pois permite temperaturas menores em fornos operados, com eliminação de CO2, SO2 e NO, juntamente economizando energia. As matérias primas consumidas como areia, barrilha e calcário também são reduzidas com o caco.
-
De volta para os fornos de fabricação, para ser reciclado terá que estar livre de matérias incomuns do tipo papel, plástico, madeira, louça, tijolos, cerâmicas, ferro, alumínio e cobre.
E também alguns tipos de vidros devem separadamente reciclados, como vidro plano, vidros de laboratórios, peças usadas em cozinha e até mesmo os coloridos, que não pode se misturar com os incolores. E mais são usados em fabricas de vidro duas origens do caco, as procedidas em processos de fabricação que são peças quebradas, com defeitos e devolvidas, e as que são compradas em próprias firmas especializadas em coletas do caco dos lixões, bares, residências ou clubes. Quando são utilizados cacos de fabricação no próprio local, não se acham materiais estranhos no meio, portanto, será preciso somente em diminuir o tamanho dos cacos antes de voltar à produção. Porem cacos que foram de lixões, antes tem que passar por processos de seleção rigorosos devido às impurezas inorgânicas e orgânicas.
Provas beneficiam o caco que cada impureza se reúne a dificuldade técnica na fabricação do vidro, pois partículas refratarias como cerâmicas, porcelanas e minerais diminui a resistência mecânica e aumenta o índice de quebra em serviço; substancias orgânica modifica o equilíbrio redox do banho fundido que causa alterações no processo e ligas metálicas e metais traz variação de cor. Um emprego de 90% do caco não perde a qualidade do vidro através de estudos. O Manual de Reciclagem do Vidro com dados econômicos publicados pela ABIVIDRO (Associação Brasileira das Indústrias do Vidro) disponibiliza diferentes processos e equipamentos usados.
9. CONSIDERAÇÕES FINAIS
Depois do tema escolhido, em busca de bibliografias para leituras e pesquisas, foram concluído nesse trabalho de conclusão de curso que os vidros são materiais inorgânicos, merecem ser estudos e não somente utilizados para atender as necessidades para alguma utilidade. Especificamente este tema merece ser explorado nos estudos, com mais leituras e pesquisas para maiores conhecimentos. Acredito que foi absorvido todos os conhecimentos vítreo, para futuramente poder explorar com técnicas experimentais. Devido ás evoluções que foram feitas durante anos para o vidro, com mais estudos pode ter novas evoluções e métodos na fabricação vidreira.
Para a produção deste trabalho de conclusão de curso, tive a mente aberta para poder enxergar quimicamente melhor sobre os materiais vítreos, podendo repassar ao próximo todo conhecimento adquirido. Foi importante ter em mente todo o conhecimento do vidro desde a origem, a sua definição e o processo de fabricação.
10. Referências bibliográficas
Alves, O. L.; Gimenez, I. F.; Mazali, I. O. Vidros. Cadernos Temáticos- Química Nova na Escola, [S.l.], p. 9- 20, fev. Disponível em: <http://lqes.iqm.unicamp.br/images/pontos_vista_artigo_divulgacao_vidros.pdf>. Acesso em: 12 out. 2013
Amâncio, C. T. Produção e Caracterização de Vidros de Telureto Tridopados com Íons de Terra Raras e Nanoparticulas Metálicas para Usos e Displays Coloridos. 2011. 114 f. Dissertação (Mestrado em Engenharia de Sistema Eletrônico) – Escola Politécnica, Universidade de São Paulo, São Paulo, 2011.
Aranha, N. Vidros Niobofosfatos: Preparação, Caracterização e Propriedades. 1994. 133 f. Tese (Doutorado em Química) – Instituto de Química, Universidade Estadual de Campinas, Campinas, 1994. Disponível em: <http://biq.iqm.unicamp.br/arquivos/teses/vtls000082396.pdf>. Acesso em: 12 out. 2013.
Araujo, E. B. Vidro: Uma Breve História, Técnicas de Caracterização e Aplicações de Tecnologia. Revista Brasileira de Ensino de Física, [S.l.], v. 19, n. 3, p. 325- 329, set. 1997. Disponível em: < http://www.sbfisica.org.br/rbef/pdf/v19_325.pdf>. Acesso em: 12 out. 2013.
Askeland, D. R; Phulé, P. P. Ciência e Engenharia dos Materiais. Tradução Vertice Translate All Iasks. São Paulo: Cengage Learning, 2008. p. 461- 468.
ATKINS, P. W., Jones, L. Princípios de química. Tradução Ricardo Bicca de Alencastro. Porto Alegre: Bookman, 2006. P. 279- 280- 658.
Brady, J.; Hamiston, G. E. Química Geral. 2º ed. Rio de Janeiro: LTC, 1986. p. 298- 299.
Brown, T. L.; Lemay, H. E. Jr.; Bursten, B. E.; Burdge, J. R. Química- A Ciência Central. Tradutor Robson Matos. 9º ed. São Paulo: Pearson Prentice Hall, 2005. p. 845- 856.
Costa, H. R. N. Aplicação de Técnicas de Inteligência Artificial em Processos de Fabricação de vidro. 2006. 248 f. Tese (Doutorado em Engenharia de Telecomunicações e Controle) – Escola Politécnica da Universidade de São Paulo, São Paulo, 2006. Disponível em: <http://discoverynbo.com.br/wp-content/uploads/2012/08/Inteligencia-Artificial.pdf>. Acesso em: 28 ago. 2013.
Dal Bó, M.; Silva, L.; Oliveira, V. Fabricação de Vetrosas com a Utilização de Resíduos de Vidro Plano e Bulbo de Lâmpadas. 2009, Disponível em: <http://www.ceramicaindustrial.org.br/pdf/v14n4/v14n4a05.pdf>. Acesso em: 28 ago. 2013.
Furtado, L. M. L. Preparação, Caracterização e Propriedades do sistema Vítreo: Nb2O5- SiO2- B2O3- M2O (M= Na+, K+). 1995. 120 f. Tese (Doutorado em Química Inorgânica) – Instituto de Química, Universidade de São Paulo, São Paulo, 1995.
Gordo, V. O. Estudo das Propriedades Estruturais e Ópticas do Sistema Vítreo 80TeO2- 20WO3 dopado com Yb2O3. 2010. 73 f. Dissertação (Mestrado em Ciência dos Materiais) – Faculdade de Engenharia de Ilha Solteira, Universidade Estadual Paulista, Ilha Solteira, 2010. Disponível em: <http://penelope.dr.ufu.br/bitstream/123456789/721/1/EstudoPropriedadesOpticas_parte_1.pdf>. Acesso em: 13 set. 2013.
Junior, W. D. C. Fundamentos de Engenharia de Materiais: Uma Abordagem Integrada. Tradução de S. M. S. Soares. 5º ed. Rio de Janeiro: LTC, 2001. p. 414- 415- 449- 452.
Kotz, J. C.; Treichel, P. M.; Weaver, G. C. Química Geral e Reações Químicas. Tradução Solange Aparecida Visconte. São Paulo: Cengage Learning, 2010. p. 570- 571.
LEE, J. D. Química inorgânica não tão concisa, tradução da 5ª edição inglesa, São Paulo: Edgard Blucher, 1999. p. 224.
Maia, S. B. O Vidro e sua Fabricação. Rio de Janeiro: Interciência. 2003.
Maran, M. A. Materiais Elétricos: Compêndio de trabalhos. 2010 135 f. Dissertação (Mestrado em Centro de Engenharia e Ciências Exatas) – Universidade Estadual do Oeste do Paraná, Foz do Iguaçu, 2010. Disponível em <http://www.foz.unioeste.br/~lamat/downcompendio/compendiov1.pdf#page=3>. Acesso em: 20 set. 2013.
Marçal, R. L. S. B. Fabricação de Vidros Especiais a Partir de Resíduos da Indústria de Rochas Ornamentais. Dissertação (Mestrado em Ciência dos Materiais) – Instituto Militar de Engenharia, Rio de Janeiro, 2011. Disponível em: < http://www.ime.eb.br/arquivos/teses/se4/mec2011/Dissert_RuMar.pdf>. Acesso em: 12 out. 2013.
Martins, J. G.; Pinto, E. L. Materiais de Construção I: O Vidro. 2004. Disponível em: <http://xa.yimg.com/kq/groups/24054498/1296748103/name/Vidros+2.pdf> Acesso em: 28 ago. 2013.
Martins, V. M. Desenvolvimento e Caracterização Fototérmica de Novos Materiais Vítreos Dopados com Íons Emissores Terras-Raras. 2009. 150 f. Dissertação (Mestrado em Física) – Instituído de Física, Universidade Federal de Uberlândia, Uberlândia, 2009. Disponível em: <http://penelope.dr.ufu.br/bitstream/123456789/749/1/DesenvolvimentoCaracterizacaoFototermica.pdf>. Acesso em: 21 set. 2013.
Mata, T. M. C. P. Comparação de Processos de Reutilização/Reciclagem usando a Metodologia de Analise do Ciclo de Vida. 1998, 176 f. Dissertação ( Mestrado em Engenharia do Ambiente) – Faculdade de Engenharia, Universidade do Porto, [S.I.], 1998. Disponível em: <http://repositorio-aberto.up.pt/bitstream/10216/58012/1/Texto%20integral.pdf>. Acesso em: 06 out. 2013.
Nascimento, M. L. F. Condutividade Elétrica de Vidros de Boratos, Silicatos e Sílico- Sulfatos de Íons Alcalinos. 2000. 196 f. Dissertação (Mestrado em Ciências) – Instituto de Física, Universidade de São Paulo, São Paulo, 2000. Disponível em: <http://www.teses.usp.br/teses/disponiveis/43/43133/tde-09122001-161054/pt-br.php>. Acesso em: 02 set. 2013.
Nogushi, Y. Y. Métodos de Preparação e Propriedades de Vidros de Fluoretos. [s.d.]. 96 f. Dissertação (Mestrado em Física,), Universidade Federal de Mato Grosso do Sul, [s.n.t]. Disponível em: < http://200.129.202.51:8080/jspui/bitstream/123456789/516/1/Yuri%20Yasuo%20Noguchi.pdf>. Acesso em: 12 out. 2013.
Padilha, A. F. Materiais de Engenharia: Microestrutura e Propriedades. 1º ed. São Paulo: Hemus,1997. p. 201- 210.
Sousa, P. P; Silva G. G.; Amaral, O. F. O Cotidiano é meio Amorfo Transição Vítrea, Uma Abordagem para o Ensino Médio, Química Nova na Escola. [S.l.], n 20, p. 21- 25. nov., 2004. Disponível em: >http://qnint.sbq.org.br/qni/visualizarConceito.php?idConceito=35>. Acesso em: 12 out. 2013.
Shreve, R. N., Brink Jr. J. A. Indústrias de Processos Químicos, 4 ed. Rio de Janeiro: LTC, 1997. p. 159- 175.
Vieira, H. Avaliação da Cristalização e Durabilidade Química de Vidros Niobofosfatos Visando a Imobilização de Rejeitos Radioativos. 2008. 68 f. Dissertação (Mestrado em Ciência na Área de Tecnologia Nuclear- Materiais) – Instituto de Pesquisas Energéticas e Nucleares, Universidade de São Paulo, São Paulo, 2008. Disponível em: < http://pelicano.ipen.br/PosG30/TextoCompleto/Heveline%20Vieira_M.pdf>. Acesso em: 12 out. 2013.
Vlack, L. H. V. Princípios de Ciência dos Materiais. São Paulo: Blucher. 1970. p. 73- 75.
Yamaky, S. B.; Pedroso, A. G.; Atvars, T. D. Z. O Estado Vítreo Dentro da Perspectiva do Curso de Graduação em Química (Físico- Química). Química Nova, Campinas, v.25, n. 2, p.330- 334, nov., 2002. Disponível em: < http://www.scielo.br/pdf/qn/v25n2/10462.pdf> Acesso em: 12 set. 2013.
Zanoto, E. D. Vidros: Arte, Ciência e Tecnologia de 4000 A.C. a 2000 D.C. Artigos Técnicos, [S.l.], n. 1, p. 33- 36, mai. jun. jul., 1989. Disponível em: < http://www.lamav.ufscar.br/artpdf/em1-89.pdf>. Acesso em: 12 out. 2013.
Ziemath, E. C. Caracterização de Vidros e Vitro- Cerâmicas com composição 2Na2O.1CaO3SiO2. 1990, Disponível em: < http://www.teses.usp.br/teses/disponiveis/54/54132/tde-16012008-095911/pt-br.php> Acesso em: 14 set. 2013.