Sumário
RESUMO
Este trabalho objetivou analisar o comportamento hidroquímico das águas do Igarapé Lagoa Azul no município de Monte Alegre, visando estabelecer um estudo sobre as características das águas diante das crescentes modificações que as mesmas vêm sofrendo devido as influências trópicas e antrópica. A coleta dos dados foi efetuada no período seco e foram estudados a temperatura da água, pH, oxigênio dissolvido, Ca2+, e alcalinidade. Para as amostras analisadas diretamente nos pontos de coleta as variáveis analisadas mostram que as águas do Igarapé Lagoa Azul são ácidas, com temperatura ideal e altos teores de oxigênio dissolvido. Para as amostras analisadas no laboratório do Colégio Fernando Henrique Cardoso as variáveis analisadas mostram que as água do Igarapé Lagoa Azul apresentaram aumento de pH, e considerável concentração de Ca2+, em relação às características hidroquímicas dos igarapés naturais da região, portanto, apresenta indícios de impactos trópicos e antrópicos.
Palavras - chave: Água superficial; Hidroquímica; Impactos ambientais.
ABSTRACT
This study aimed to analyze the behavior of hydro chemical at Lagoa Azul stream in the municipality of Monte Alegre, to establish a study on the characteristics of the water by the grow in changes that it has suffered due to the tropics and anthropogenic influences. Data collection was performed during the dry period and were studied he water temperature, pH, dissolved oxygen, Ca2+, and alkalinity. The samples analyzed directly on the collection points show that the waters of Lagoa Azul stream are acidic, with ideal temperature and high levels of dissolved oxygen. For samples analyzed in the laboratory of Fernando Henrique college variables analyses how that the water of Lagoa Azul stream demonstrated a increased pH, and considerable concentration of Ca2+ compared to others hydro chemical features of the streams in the region, therefore, presents evidence of tropics and anthropics impact.
Keywords: Surface water, hydrochemistry, environmental impacts.
INTRODUÇÃO
De que trata este trabalho? o tema deste trabalho se resume aos elementos químicos Hidrogênio e Oxigênio, que, combinados em uma fórmula, de duas moléculas de Hidrogênio e uma de Oxigênio, resultam no bem vital água ( H2O ), e suas reações quando em contato com outros sais ou elementos químicos.
Águas naturais possuem, em graus distintos, um conjunto de sais em solução, em maior ou menor quantidade. Sendo que as águas subterrâneas possuem em geral, teores mais elevados do que as águas superficiais, devido a falta de preservação e preocupação com a conservação das águas superficiais.
A determinação de padrões físico-químicos da água e ambientes aquáticos é de suma importância, pois representa um bem utilizado por todos os seres vivos de formas múltiplas. Com base nisto é necessário determinar a temperatura, o pH e a alcalinidade, a quantidade de oxigênio dissolvido e a quantidade de Mg e Ca que representam a dureza da água.
A falta de preservação das águas no município de Monte Alegre nos despertou o interesse de conhecermos a qualidade e o comportamento hidroquímico do Igarapé Lagoa Azul.
Monte Alegre é um município brasileiro do estado do Pará, pertencente a Mesorregião do Baixo Amazonas e Microrregião de Santarém, localizado a uma altitude de 02º00’28’’ sul e a uma longitude 54º04’09’’ oeste, estando a uma altitude de 38 metros.
O Igarapé Lagoa Azul, local onde nosso trabalho foi realizado está situado a 17 quilômetros da cidade de Monte Alegre, localizada a latitude 01º51.011’ sul e a uma longitude 54º02.783’ oeste, com a elevação de 69 metros.
Para se chegar a um resultado satisfatório nesta pesquisa sobre as propriedades hidroquímicas do Igarapé Lagoa Azul, fez-se necessário estabelecer critérios de avaliação da qualidade da mesma. O melhor modo de fazer isso é analisar suas características e suas variáveis naturais. O resultado é surpreendente quando se percebe que os recursos hídricos sofrem ações de condicionantes que naturalmente alterariam sua composição, ainda que sem ação humana.
A IMPORTÂNCIA DO EQUILÍBRIO NO MEIO FÍSICO-NATURAL.
“Da relação, (em diferentes épocas e lugares) dos seres humanos entre si e com o meio físico-natural emerge o que se denomina neste texto de meio ambiente. Diferente dos mares, dos rios, das florestas, da atmosfera, que não necessitaram da ação humana para existir, o meio ambiente precisa do trabalho dos seres humanos para ser construído e reconstruído e, portanto, para ter existência concreta. Não existe meio ambiente sem o trabalho dos seres humanos”. (Quintas, 2006, p. 20)
Apesar do ser humano depender do meio ambiente ou meio físico-natural para garantir seu sustento e sobrevivência, seu uso e degradação são tão antigos quanto a existência humana no Planeta Terra. Criando assim a interdependência homem-natureza denominada de meio ambiente. Ao homem foi dado o poder de construir, destruir e reconstruir todas as coisas da natureza, garantindo equilíbrio ou desequilíbrio ao meio físico-natural. O desaparecimento do mesmo implica também o fim da espécie humana e do Planeta Terra.
Desde a criação do Planeta Terra o ser humano vem explorando o meio físico-natural de maneira desastrosa sem se preocupar com as consequências. Não obstante, derruba e incendeia florestas destruindo e empobrecendo o solo que pode ser utilizado para plantil, alterando o ciclo das chuvas. Assoreia lagos, rios e igarapés. Polui o bem mais precioso e vital a todos os seres vivos do planeta “a água”
Ao longo de toda a história da humanidade, o elemento “água” sempre esteve presente, sendo de grande importância para o meio físico-natural, fazendo com que as civilizações se estabelecessem às margens dos rios, regiões costeiras e insulares.
Pode-se afirmar que a relação homem-água originou-se no útero materno e vai até as necessidades mais banais dos seres humanos. Esse bem que proclamamos ambiental, encontra-se em perigo. E a “água”, considerada símbolo da vida, tornou-se objeto de disputa e conflitos geopolíticos, pois devido a falta de preservação dos recursos hídricos constatou-se sua finitude e escassez.
A água existente no planeta não é a mesma desde que a terra existe. Não se produz água, ela não vem de outros planetas. Mas a sua conservação advém do uso moderado, mantidas as condições de seu ciclo.
Portanto entendem-se por recurso ambiental aatmosfera, as águas interiores, superficiais e subterrâneas, os estuários, o mar territorial, o solo, o subsolo, os elementos da biosfera, a fauna e a flora. A biosfera compreende a vida na terra nos diferentes ambientes, repousados nos estados químicos gasoso (a atmosfera), líquido (hidrosfera) e sólido (litosfera).
.jpg)
Fonte: Luciana Cordeiro de Souza,p. 40
Todos os estados químicos interagem de forma conjunta e harmônica. Ao se agredir um deles está se agredindo o todo. Assim trazemos à colocação essas palavras:
“Florestas e águas são tão interdependentes que em muitos casos não se sabe qual é a causa e qual é a conseqüência, ou seja, a floresta existe ali porque o ambiente é mais úmido, ou o ambiente é mais úmido porque existe uma floresta ali. A copa da árvore recebe os pingos de chuva das alturas, eles passam de folha em folha, de galho em galho. Alguns escorrem pelo tronco e chegam delicadamente na terra. Infiltram-se no solo com ajuda das raízes que abrem caminho, pois dentro do solo a água corre lentamente. A água fica armazenada dentro do solo, onde é mais difícil o sol secá-la e ela pode ir minando devagarinho para os rios. A chuva que cai de enxurrada arrasta a terra com ela para dentro dos açudes e rios, isto chama-se assoreamento. Todos os açudes e rios devem ter árvores nas margens, protegendo-os como os cílios protegem os olhos. Estas florestas que protegem os rios são chamadas matas ciliares. Além disso, o solo da floresta trabalha com um gigantesco filtro físico e biológico, garantindo a limpeza e pureza da água.
“As florestas nos garantem água em quantidade e com qualidade”.(Duarte, 2009,p. 5).
A ORIGEM DA ÁGUA NO PLANETA TERRA.
Para que possamos discorrer sobre o elemento água, urge conhecermos o objeto de nosso estudo. Dessa forma apresentaremos neste capítulo alguns dados técnicos no intuito de desvendar, de forma genérica e sucinta, as origens da água.
Ao tratarmos da origem da água, torna-se quase inevitável nos reportarmos à Bíblia Sagrada, no primeiro livro do Antigo Testamento escrito pelo profeta Moisés para – no mínimo curiosamente – lembrarmos como o tema foi tratado.
Pela leitura dos textos de gênesis percebemos a importância e os mistérios do elemento água para a formação, manutenção e o desenvolvimento do planeta e do próprio desconhecimento do “historiador”, analiticamente.
Assim temos:
“No princípio, Deus criou os céus e a terra. A terra estava informe e vazia, as trevas cobriam o abismo e o Espírito de Deus pairava sobre as águas. (Gênesis, cap. 1, v. 1-2)
(...)
“Deus disse: “faz-se um firmamento entre as água e separe ele uma das outras”. Deus fez o firmamento e separou as águas que estão debaixo do firmamento daquelas que estão por cima. E assim fez.
Deus chamou ao firmamento de Céus. (Gêneses, cap.1, v6-8)
(...)
Deus disse: “Que as águas que estão debaixo dos céus se ajudem num mesmo lugar e apareça o elemento árido”. E assim se fez.
Deus chamou ao elemento árido TERRA, e ao ajuntamento das águas MAR. E Deus viu que isto era bom. (Gêneses, Cap. 1 v. 9-10)”.
Por se tratar de um trabalho técnico não podemos nos ater somente a teorias religiosas, mas buscar a hegemonia científica, portanto vamos adotar a Teoria da Grande Explosão Cósmica ou Teoria do Big Bang, onde o universo surge a partir de uma grande explosão cósmica a 15 bilhões de anos, e que antes de tal explosão não existia nada. Apoiando a idéia de finitude da matéria como senso comum, como resultado da atividade vital do indivíduo.
“No começo, a terra era uma bola de fogo. Depois, através de um processo de resfriamento que durou bilhões de anos, formaram-se a crosta e a atmosfera terrestre.
Durante esse processo, o vapor proveniente das rochas se condensou e começou uma chuva torrencial que durou séculos, resultando na formação dos mares e oceanos.
Com o tempo, as rochas esfriaram, e a temperatura da água baixou. Nos mares apareceram então os primeiros organismos vivos, que eram seres unicelulares, isto é, formados por uma única célula. (BOULOS JR,p.22-7)”
Apresentados os fatos que possibilitaram a formação do universo e do nosso planeta, e da visão religiosa que o tema encerra, uma questão deve ser ressaltada quanto a formação da água, principalmente porque o tema deste trabalho se resume aos elementos químicos Hidrogênio e Oxigênio, que, combinados em uma fórmula, digamos, numa receita de duas moléculas de Hidrogênio e uma de Oxigênio, resultam no bem vital que não pode ser criado em laboratório: a água, objeto de nossa preocupação e estudo.
A estrutura molecular da água:
H – O – H
Onde o oxigênio está ligado a dois hidrogênios, a ligação é realizada através do compartilhamento de um elétron de cada um dos hidrogênios com um elétron desemparelhado do oxigênio. Esse tipo de ligação é chamada covalente. A formação de ligações covalentes entre o átomo de oxigênio e os dois átomos de hidrogênio é vantajosa porque cada átomo atinge um nível de valência completo através do compartilhamento desses elétrons. Para o oxigênio em uma molécula de água, essas quantidades satisfazem a regra do octeto, segundo nos mostra a Estrutura de Lewis:
A água é definida como líquido incolor, inodoro, e insípido. Na natureza ela contém pequenas quantidades de água pesada, de gases e de sólidos (principalmente sólidos), em dissolução.
Vale dizer que devido à sua estrutura molecular dipolar a importância da água está relacionada diretamente com sua função de excepcional solvente (solvente universal) que carrega os nutrientes essenciais a vida.
Em águas naturais este poder de dissolução é aumentado pela presença de ácido carbônico, formado pelo gás carbônico dissolvido, e ácidos orgânicos, principalmente húmicos, produzidos pelas atividades dos seres vivos ao nível do solo.
A água é um importante condutor de corrente elétrica. Quanto maior for a quantidade de íons dissolvidos na água, maior será sua condutividade elétrica. Esta variável hidrológica pode contribuir para o reconhecimento de impactos ambientais na bacia de drenagem ocasionados por lançamento de resíduos industriais, mineração, esgotos etc.. É o que ocorre com substâncias como os alvejantes (água sanitária), por exemplo, cujos íons de cloro, ao serem lançados no sistema, elevam sua condutividade elétrica.
CLASSIFICAÇÃO DAS ÁGUAS
São várias as classificações das águas, mais faremos menção apenas de duas:
Águas Subterrâneas
Águas subterrâneas compreendem os lençóis freáticos localizados a certa profundidade no subsolo. São atualmente a fonte de abastecimento preferida por apresentarem maior facilidade de exploração, baixo custo e boa qualidade.
O gráfico abaixo nos mostra as principais reservas de águas subterrâneas no mundo:
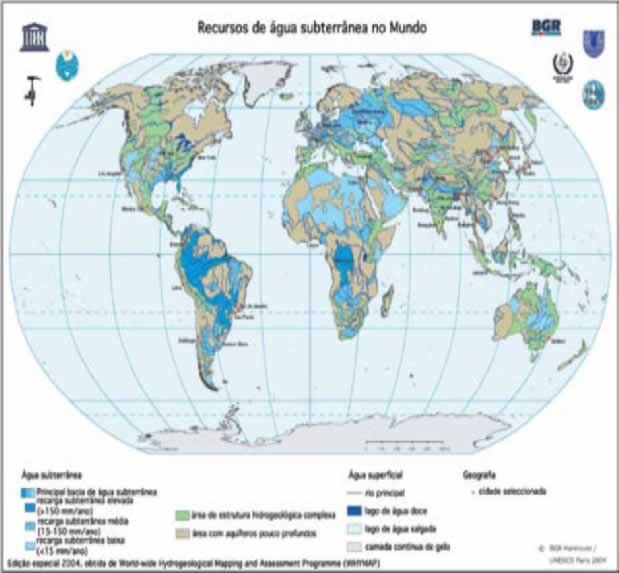
Fonte: Águas Subterrâneas,p 3
Existe hoje uma preocupação a nível mundial com a preservação das águas subterrâneas pois, já existem casos comprovados de reservas subterrâneas contaminadas por chorume de aterros sanitários, lixo industrial ou produtos agrícola.
As características químicas das águas subterrâneas refletem os meios por onde percolam, guardando uma estreita relação com os tipos de rochas drenadas e com os produtos das atividades humanas adquiridas ao longo de seu trajeto.
Águas naturais possuem, em graus distintos, um conjunto de sais em solução, em maior ou menor quantidade ou em alguns casos quantidade nenhuma. Sendo que as águas subterrâneas possuem em geral, teores mais elevados do que as águas superficiais, devido a falta de preservação e preocupação com a conservação das águas superficiais.
Tais sais são na verdade elementos químicos encontrados na água, que em dosagem certa são benéficas aos seres humanos e dão maior fertilidade ao solo.
A quantidade de sais dependerá do meio percolado.
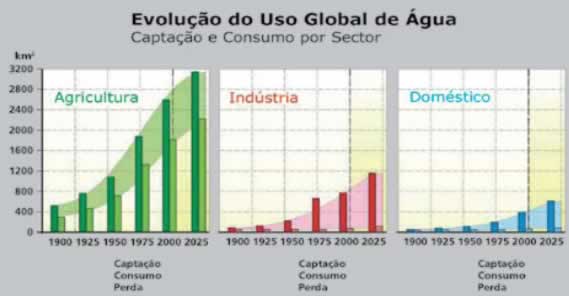
Fonte: Águas Subterrâneas, p. 10
Águas Superficiais
Águas superficiais estão na superfície da terra. Dividem-se em superficiais internas (rios,lagos e mares interiores) e superficiais externas (mar territorial, alto-mar, águas contíguas).
QUANTO AO USO PREDOMINANTE (CONFORME RESOLUÇÃO NA CONAMA 357/2005)
Doce: desprovida de salinidade. Divide-se em:
Classe especial – destinada ao abastecimento domestico, sem previa desinfecção ou tratamento; classe I – destinada ao abastecimento domestico, sem prévio tratamento convencional; classe II – destinada ao abastecimento domestico, após tratamento convencional; classe III – destinada ao abastecimento domestico; após tratamento convencional, à fauna e à flora depois de tratamento; classe IV – destinada ao abastecimento domestico, após tratamento avançado; navegação, harmonia paisagística, abastecimento industrial e irrigação.
Salobra: água de salinidade inferior à oceânica. Divide-se em:
Classe I – destinada à recreação de contato primário, à proteção das comunidades aquáticas e à criação natural e/ou intensiva das espécies destinadas à alimentação humana, para as quais se estabelecem condições de pureza similares à água doce da classe I; classe II – destinada á navegação comercial, à harmonia paisagística a à recreação de contato secundário, com condições de pureza à da água da classe III.
Salina: com salinidade oceânica. Divide-se em:
Classe I – destinada à recreação de contato primário, à proteção das comunidades aquáticas e à criação natural e/ou intensiva das espécies destinadas à alimentação humana. Suas condições e limites são os mesmos da classe I da água doce; classe II – destinada á navegação comercial, á harmonia paisagística e a recreação de contato secundário, com condições de pureza à da água da classe III.
|
TIPOS DE ÁGUA |
GRAMAS DE SAIS POR LITRO |
|
Doce |
Abaixo de 0,5 |
|
Salobra |
1,0 a 4,0 |
|
Salgada |
Acima de 0,5 |
Fonte: Luiz Roberto Magossi, Paulo Henrique Bonacela 2003,p. 11
O CICLO DA ÁGUA
O ciclo da água, também denominado ciclo hidrológico, é responsável pela renovação da água no planeta. O ciclo da água inicia-se com a energia solar, incidente no planeta Terra, que é responsável pela evapotranspiração das águas dos rios, reservatórios e mares, bem como pela transpiração das plantas.
As forças da natureza são responsáveis pelo ciclo da água. A água é fator decisivo Para que a vida surgisse e se desenvolvesse na Terra.
O vapor d'água forma as nuvens, cuja movimentação sofre influência do movimento de rotação da Terra e das correntes atmosféricas.
A condensação do vapor d'água forma as chuvas. Quando a água das chuvas atinge a terra, ocorrem dois fenômenos: um deles consiste no seu escoamento superficial em direção dos canais de menor declividade, alimentando diretamente os rios e o outro, a infiltração no solo, alimentando os lençóis subterrâneos.(CETESB 2003)
A água dos rios tem como destino final os mares e, assim, fechando o ciclo das águas. A movimentação da água na natureza é mostrada na figura a seguir:
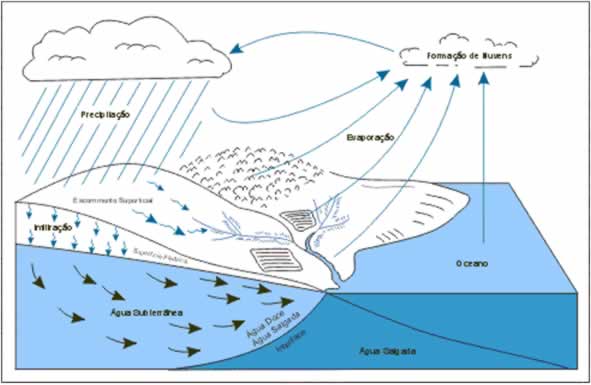
Fonte: SEMA São Paulo-SP, 2003
TEMPERATURA DA ÁGUA
A Resolução 20/86 do Conama estabeleceu em artigo 21, letra “b”, que poderá haver lançamentos, direto ou indireto, de efluentes de uma fonte poluidora, desde que a temperatura do corpo de água atingido seja inferior a 40ºc e que a elevação da temperatura não ultrapasse 3ºc. Na verdade, esse parâmetro é de fundamental importância para os sistemas aquáticos, já que os organismos reagem de forma diferente a mudanças nesse fator.
Nos ecossistemas aquáticos continentais a quase totalidade da propagação do calor ocorre por transporte de massa de água. Quando diferentes densidades estão presentes, a propagação do calor é comprometida, uma vez que enfrenta uma barreira física. Quando a temperatura é uniforme na coluna de água, a propagação do calor através de toda a massa líquida pode ocorrer de maneira bastante eficiente, uma vez que a densidade da água nessas condições é praticamente igual em todas as profundidades.
Normalmente são bastante expressivas as variações de temperatura nos recursos hídricos. Altas temperaturas provocam reações adversas, tais como a desnaturação das proteínas, isto é, quando o organismo diminui seu metabolismo para reduzir a possibilidade de danos. Quando ocorre elevação de temperatura por introdução de águas mais quentes, aceleram-se mecanismos como de respiração, nutrição, reprodução e movimentação.
As baixas temperaturas afetam especialmente seres dos países tropicais como o Brasil, pois eles possuem pouca reserva de gordura e glicogênio nos músculos, exigindo que gastem mais calorias para manter-se aquecidos, e reduzindo a intensidade de metabolismo e movimentação.
OXIGÊNIO DISSOLVIDO (OD)
Esta é uma das variáveis mais importantes dos indicadores da água. O oxigênio é necessário para a respiração da maioria dos organismos aquáticos, é de fundamental importância para avaliar as condições naturais da água e detectar impáctos ambientais como eutrofização e poluição orgânica.
Variáveis como a temperatura da água e a pressão atmosférica influem diretamente na quantidade de oxigênio dissolvido. Quanto maior a pressão, maior a dissolução, e quanto maior a temperatura, menor a dissolução desse gás.
A medida de oxigênio dissolvido na água é muito importante para determinar o estado de saúde do sistema hídrico. Por esse parâmetro pode-se descobrir se houve poluição do corpo de água, promover a responsabilização dos poluidores e garantir a proteção dos recursos hídricos
Uma conclusão enganosa a que se pode chegar é de que os rios de serra, que são encachoeirados e portanto promovem ótima oxigenação, seriam ricos em espécies. Pelo contrário, tais rios são comumente conhecidos como abióticos, ou seja, com poucas ou nenhuma espécie, o que ocorre em razão de uma combinação natural de fatores que impedem condições favoráveis de vida.
Segundo o dicionário livre de Geociências:
OD:- Abreviação para Oxigênio Dissolvido. É a quantidade, em mg/L, de oxigênio dissolvido na água. O índice OD é um dos mais importantes para se avaliar a capacidade de um corpo hídrico em suportar atividade biológica de organismos aquáticos. Nas águas naturais de superfície o índice OD varia de 0 a 19 mg/L, mas um teor de 5 a 6 mg/L já é o suficiente para suportar uma população variada de peixes. Em águas subterrâneas a quantidade de oxigênio dissolvido é muito baixa pelo fato de estar fora do alcance da atmosfera
“http//www.dicionariolivredegeociencia.com.br”
pH E ALCALINIDADE
O termo pH, usado como sigla para potencial hidrogeniônico, expressa o grau de acidez ou basicidade de uma solução, ou seja, expressa a concentração de íons de hidrogênio nessa solução. Quanto maior a concentração de íons de hidrogênio em solução aquosa, menor o pH, e vice-versa.
A escala de pH denota vários graus de acidez ou alcalinidade, que variam de 0 a 14. Valores abaixo de 7 e próximos de zero indicam aumento de acidez, enquanto valores de 7 a 14 indicam aumento de basicidade. Em um corpo de água, quanto mais próximo de zero ou de 14 o pH de uma solução, menor a diversidade de organismos existentes, isso porque é estrita sua faixa de tolerância às mudanças de pH.
Convém lembrar que a escala de pH é logarítmica, isto é, pequenas diferenças nos números correspondem a grandes diferenças da variável. O seguinte diagrama representa didaticamente uma escala de pH:
Geralmente as águas doces superficiais têm pH entre 4 e 9. Em lagoas com grande populações de algas, nos dias ensolarados o pH pode subir muito, chegando o 9 ou até mais.
Os rios brasileiros têm tendência à acidez. Sobre os efeitos de um pH muito baixo, Ponting ensina:
Um pH de 6,0 é de um nível crítico; a vida animal começa a ser afetada. Os processos exatos envolvidos são complexos, mais um dos mais sérios é a concentração elevada de metais pesados tóxicos, com níveis de pH baixos, em particular a precipitação de alumínio, como hidróxido de alumínio nas guelras dos peixes, que reduz a ingestão de oxigênio, causando grandes desiquilíbrios nos níveis internos de sal. Em água com um pH de 5,5 e 5,0, os ovos e as larvas são profundamente afetados e as lesmas não sobrevivem em um pH abaixo de 5,2. Os peixes não sobrevivem em um pH abaixo de 5,0 e, a um nível de 4,5 até a flora é terrivelmente afetada.
“uma história verde do mundo. Tradução Ana Zelma Campos, Rio de Janeiro: civilização Brasileira, 1995.p. 583.”
Por fim, é possível, ainda que existam variações no pH que reflita o tipo de solo por onde a água passou, bem como o despejos industriais.
DUREZA DA ÁGUA
Dureza da água é a propriedade relacionada com a concentração de íons de determinados minerais dissolvidos nesta substância. A dureza da água é predominantemente causada pela presença de sais de Cálcio e Magnésio, de modo que os principais íons levados em consideração na medição são os de Cálcio (Ca2+) e Magnésio (Mg2+). Eventualmente também o Zinco, Estrôncio, Ferro ou Alumínio podem ser levados em conta na aferição da dureza.
A dureza da água é composta de duas partes, a dureza temporária e a dureza permanente. A dureza temporária é gerada pela presença de carbonatos e bicarbonatos, que podem ser eliminadas por meio de fervura da água. A dureza permanente é devida a cloretos, nitratos e sulfatos, que não são susceptíveis à fervura.
À somatória da dureza temporária e permanente dá-se o nome de "Dureza Geral" (ou total) da água.
Embora não haja uma convenção formal, a título de praticidade, a água pode ser classificada quanto a dureza de acordo com a tabela seguinte:
|
Muito Mole |
0 a 70 ppm |
0-4 dGH |
|
Mole (branda) |
70-135 ppm |
4-8 dGH |
|
Média Dureza |
135-200 ppm |
8-12 dGH |
|
Dura |
200-350 ppm |
12-20 dGH |
|
Muito Dura |
mais de 350 ppm |
mais de 20 dGH |
Fonte: Frenzl
ANÁLISE QUÍMICA DA ÁGUA DO IGARAPÉ LAGOA AZUL
Conforme dados do Instituto Brasileiro de Geografia e Estatística (IBGE), 2010, Monte Alegre é um município brasileiro do estado do Pará, pertencente a Mesorregião do Baixo Amazonas e Microrregião de Santarém , que está localizado a uma latitude 02°00’28” sul e a uma longitude 54°04’09” oeste, estando a uma altitude de 38 metros. Sua população estimada em 2010 era de 55.462 habitantes, estando inserida em uma área territorial de 18.153 km².
A economia da cidade gira em torno do serviço público, do comercio e produção agrícola que gira em torno das frutas como: Banana, melancia, Manga, laranja, limão; legumes como: Tomate, jerimum acompanhados da pimenta e do milho. Entretanto estes itens atingem altos preços no mercado local tendo em vista a produção esta voltada para a tender a outros mercados como : Manaus, Belém, Macapá, Santarém, entre outros. Contudo existem muitas expectativas em torno de duas empresas que estão se instalando a fim de extrair minérios como: Calcário e pedras preciosas.
A Lagoa Azul , local onde nosso trabalho foi desenvolvido está situada a 17 quilômetros da cidade de Monte Alegre, localizada a uma latitude 01º51.011’ sul e a uma longitude 54º02.783’ oeste com a elevação 69 metros, essa coordenada geográfica foi sensoriada no talveque do igarapé da lagoa azul na sua jusante inicio do locus de nosso estudo para análise e sua montante localizada a uma latitude 01º51.011’ sul e a longitude 54º03.213’ oeste com elevação de 82m, no entanto é visitada por poucas pessoas devido ao difícil acesso. Dentro da mata são exatos 780 metros de caminhada a partir de sua jusante a sua montante.

Fotografia da Lagoa Azul – Monte Alegre - Pará
Para se chegar a um resultado satisfatório nesta pesquisa sobre as propriedades químicas da água da Lagoa Azul, faz-se necessário estabelecer critérios de avaliação da qualidade da mesma. O melhor modo de fazer isso é analisar suas características e suas variáveis naturais. O resultado é surpreendente quando se percebe que os recursos hídricos sofrem ações de condicionantes que naturalmente alterariam sua composição, ainda que sem ação humana.
As técnicas e, principalmente, os equipamentos empregados nas pesquisas hidrobiológicas variaram conforme a finalidade do estudo que está sendo realizado, as características ambientais da Lagoa Azul e, sobretudo, com os recursos disponíveis para a realização do trabalho. Estudos limnológicos com finalidade técnica ou científica requerem, geralmente, aparelhos de grande complexidade e alta precisão. Para trabalhos em áreas reduzidas e análises de rotina, como no caso desta pesquisa, pode-se empregar equipamento mais modesto, aumentando o número de dados em poucos pontos de coleta, obtendo-se, dessa forma, uma precisão razoável de resultados, com um mínimo de material.
A obtenção das informações integradas sobre a água da Lagoa Azul dependeu basicamente do estudo das interações que ocorrem entre os fatores bióticos e abióticos que regem o funcionamento desse ecossistema. Porém, não se pode esquecer que estas interações estão vinculadas a uma escala temporal, refletindo um comportamento dinâmico e imprevisível, intrínseco a cada ambiente. Dessa forma, coube-nos promover um levantamento prévio das características ambientais da área estudada, a fim de definir o melhor ponto, horário e época para a realização dos trabalhos.

Fotografia do 1º Ponto de Coleta – Monte Alegre - Pará
Os aspectos climatológicos da região da Lagoa Azul influenciam diretamente o corpo d’água, provocando sensíveis alterações no seu metabolismo. Num período de maior precipitação ocorre um aumento na turbidez da água em função do grande aporte de material que é carreado pelas chuvas para o corpo d’água em questão. A chamada corredeira por sua vez pode provocar uma mistura na água, ocasionando uma ressuspensão de nutrientes das partes mais profundas.
Assim, serão analisadas as principais condicionantes da água da Lagoa Azul, divididas em hidrológicas e físico-químicas.
TEMPERATURA DA ÁGUA DO IGARAPÉ LAGOA AZUL
No igarapé Lagoa Azul a propagação do calor ocorre por transporte de massa d’água, sendo a eficiência deste em função da ausência ou presença de camadas de diferentes densidades.
Por outro lado, constatou-se diferenças de temperatura, gerando camadas d’água com diferentes densidades, que em si já formam uma barreira física, impedindo que se misturem, e como a energia do vento não é suficiente para misturá-las, o calor não se distribui uniformemente, criando a condição de estabilidade térmica. Ocorrendo este fenômeno, o ecossistema aquático está estratificado termicamente. Os estratos formados freqüentemente estão diferenciados física, química e biologicamente.
Para as análises da temperatura na água do Igarapé Lagoa Azul, foram utilizados termômetros simples de mercúrio e o "Termistor", para registrar diretamente a temperatura das várias profundidades na coluna d’água. Estas análises foram realizadas no próprio igarapé Lagoa Azul, tendo seu primeiro ponto próximo à sua montante à temperatura ambiente de 27ºc, tendo início às 15:30 horas da tarde.
Pôde-se constatar a oscilação em sua temperatura, principalmente onde o fluxo de água é mais intenso ou menos intenso, conforme mostra a tabela a seguir:
TABELA 6: Resultados Obtidos das Análises de Temperatura da Água do Igarapé Lagoa Azul.
|
Ponto de Coleta 1 |
22.8ºc |
|
Ponto de Coleta 2 |
22ºc |
|
Ponto de Coleta 3 |
19.4ºc |
|
Ponto de Coleta 4 |
18.4ºc |
|
Ponto de Coleta 5 |
18.4ºc |
|
Ponto de Coleta 6 |
17.5ºc |
No ponto de coleta nº 1, ao verificarmos a temperatura com termômetro eletrônico, constatamos uma temperatura de 22.8ºc, pois o mesmo está mais próximo a montante do Igarapé Lagoa Azul, tratando-se de uma pequena queda dágua com o fluxo mais intenso apresentando portanto, maior propagação de calor. Outro fator que pode ter contribuído para o aumento da temperatura da água no ponto de coleta nº1 é a influência da radiação solar, devido a sua localização geográfica, pois, o mesmo está na parte mais alta de nossa pesquisa, e em mata aberta onde ocorre maior incidência dos raios solares.
No ponto de coleta nº 2 ao verificarmos a temperatura com termômetro eletrônico, constatamos uma temperatura de 22ºc, pois o mesmo está a poucos metros do ponto de coleta nº1, tratando-se também de uma pequena queda dágua próximo a montante do Igarapé Lagoa Azul, com o fluxo menos intenso apresentando portanto uma pequena diminuição de na propagação de calor com uma diferença de temperatura de 0.8ºc em relação ao ponto de coleta nº 1.
Assim como o ponto de coleta nº 1 o ponto de coleta nº 2 pode ter sofrido influência da radiação solar em sua temperatura por sua localização geográfica, pois, o mesmo está na parte mais alta de nossa pesquisa, e em mata aberta, onde ocorre maior incidência dos raios solares.
No ponto de coleta nº 3 ao verificarmos a temperatura com termômetro eletrônico, constatamos uma temperatura de 19.4ºc, pois o mesmo está se distanciando do ponto de coleta nº1, tratando-se de uma erosão ocasionada na rocha pela força da água através dos anos formando uma pequena piscina natural, sendo a mais profunda do Igarapé Lagoa Azul, com o fluxo de água menos intenso apresentando portanto uma pequena diminuição na propagação de calor com uma diferença de 3.4ºc em relação ao ponto de coleta nº 1.
Assim como o ponto de coleta nº 1 o ponto de coleta nº 2 pode ter sofrido influência da radiação solar em sua temperatura por sua localização geográfica, pois, o mesmo está na parte mais alta de nossa pesquisa, e em mata pouco fechada, com menor incidência dos raios solares.
No ponto de coleta nº 4 ao verificarmos a temperatura com termômetro eletrônico, constatamos uma temperatura de 18.4ºc, pois o mesmo está se distanciando do ponto de coleta nº1, tratando-se de uma erosão ocasionada na rocha pela força da água através dos anos formando uma piscina natural, pouco profunda do Igarapé Lagoa Azul, com o fluxo de água mais lento e menos intenso, apresentando portanto uma pequena diminuição na propagação de calor com uma diferença de temperatura 4.4ºc em relação ao ponto de coleta nº 1.
Essa queda brusca de temperatura da água se deve a localização geográfica, pois, o ponto de coleta nº 4 está distante das quedas dágua já com uma certa calmaria, em mata fechada, o que impede a incidência de raios solares no local.
No ponto de coleta nº 5 ao verificarmos a temperatura com termômetro eletrônico, constatamos uma temperatura de 18.4ºc, pois o mesmo está se distanciando do ponto de coleta nº1, tratando-se de uma erosão ocasionada na rocha pela força da água através dos anos formando uma piscina natural, pouco profunda do Igarapé Lagoa Azul, com o fluxo de água mais lento e menos intenso, apresentando portanto uma pequena diminuição na propagação de calor com uma diferença de temperatura de 4.4ºc em relação ao ponto de coleta nº 1.
Essa queda brusca de temperatura da água se deve a localização geográfica, pois, o ponto de coleta nº 4 está distante das quedas dágua já com uma certa calmaria, em mata fechada, o que impede a incidência de raios solares no local.
Como podemos observar os pontos de coleta nº 4 e 5 apresentam as mesmas características pois, apresentam a mesma temperatura.
No ponto de coleta nº 6 ao verificarmos a temperatura com termômetro eletrônico, constatamos uma temperatura de 17.5ºc, pois o mesmo está a 764 metros de distância do ponto de coleta nº1, tratando-se de uma lagoa, pouco profunda, conhecida com Lagoa Azul, com o fluxo de água lento, apresentando portanto uma diminuição bastante considerável na propagação de calor com uma diferença de 5.3ºc em relação ao ponto de coleta nº 1.
Essa queda 5.3ºc na temperatura da água se deve provavelmente a maior concentração no volume de água, pois, o ponto de coleta nº 6 está distante das quedas dágua já com uma certa calmaria, em mata aberta, com incidência de raios solares no local.
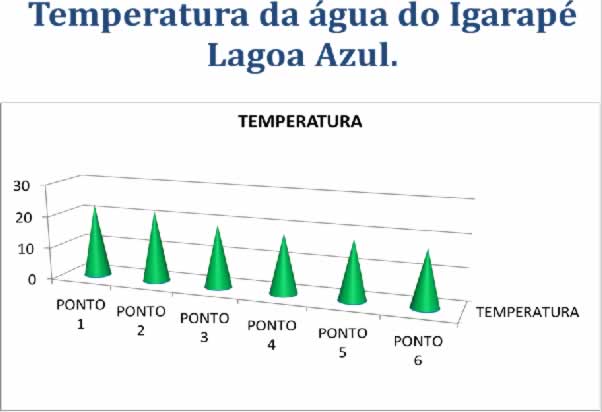
Os resultados das análises de temperatura da água do Igarapé Lagoa Azul estão acima de 3ºc e abaixo de 40ºc, estando segundo resolução do Conama 20/86 dentro dos parâmetros fundamentais para a vida aquática.
QUANTIDADE DE OXIGÊNIO DISSOLVIDO DA ÁGUA DO IGARAPÉ LAGOA AZUL.
A água do Igarapé Lagoa Azul é rica em oxigênio dissolvido. Isto devido ao constante estado de movimento da água, estimulando a produção de oxigênio.
Apesar da presença de oxigênio,que é considerado de vital importância para os seres aquáticos, como os peixes, por se tratar de um igarapé encaixoeirado e devido a sua localização geográfica é impossível a permanência dos mesmos no local.
Para as medidas de oxigênio dissolvido na água do Igarapé Lagoa Azul, foi utilizado o "Termistor", para registrar a quantidade de oxigênio dissolvido diretamente das várias profundidades na coluna d’água. Estas medidas foram realizadas no próprio igarapé Lagoa Azul, tendo seu primeiro ponto próximo à sua montante à temperatura ambiente de 27ºc, tendo início às 15:30 horas da tarde.
Pôde-se constatar a oscilação na quantidade de oxigênio dissolvido, principalmente onde o fluxo de água é mais intenso ou menos intenso, conforme mostra a tabela a seguir:
Tabela 7: Resultados Obtidos das Análises da Quantidade de OD na Água do Igarapé Lagoa Azul.
|
Ponto de Coleta 1 |
6.8 mg/L |
|
Ponto de Coleta 2 |
8.1 mg/L |
|
Ponto de Coleta 3 |
6.8 mg/L |
|
Ponto de Coleta 4 |
5.1 mg/L |
|
Ponto de Coleta 5 |
6.8 mg/L |
|
Ponto de Coleta 6 |
7.1 mg/L |
No ponto de coleta nº 1 ao verificarmos com o Termstor a quantidade de oxigênio dissolvido na água, constatamos uma quantidade de 6.8, pois o mesmo está mais próximo a montante do Igarapé Lagoa Azul, tratando-se de uma pequena queda dágua com o fluxo mais intenso apresentando portanto, maior quantidade de calor na água estimulando a produção de oxigênio.
No ponto de coleta nº 2 ao verificarmos com o Termstor a quantidade de oxigênio dissolvido na água, constatamos uma quantidade de 8.1, pois o mesmo está mais próximo a montante do Igarapé Lagoa Azul, tratando-se de uma pequena queda dágua com o fluxo mais intenso apresentando portanto, maior quantidade de calor na água estimulando a produção de oxigênio. Uma diferença de 1.3 na quantidade de oxigênio dissolvido, em relação ao ponto de coleta nº 1.
No ponto de coleta nº 3 ao verificarmos a quantidade de oxigênio dissolvido com o Termstor , constatamos uma quantidade de 6.8, pois o mesmo está se distanciando do ponto de coleta nº1, tratando-se de uma erosão ocasionada na rocha pela força da água através dos anos formando uma pequena piscina natural, sendo a mais profunda do Igarapé Lagoa Azul, com o fluxo de água menos intenso apresentando portanto uma pequena diminuição na propagação de calor, e a mesma quantidade de oxigênio dissolvido do ponto de coleta nº1.
No ponto de coleta nº 4 ao verificarmos a quantidade de oxigênio dissolvido na água, constatamos uma quantidade de 5.1, pois o mesmo está se distanciando do ponto de coleta nº1, tratando-se de uma erosão ocasionada na rocha pela força da água através dos anos formando uma piscina natural, pouco profunda do Igarapé Lagoa Azul, com o fluxo de água mais lento e menos intenso, apresentando portanto uma pequena diminuição na produção de oxigênio, com uma diferença de oxigênio dissolvido de 1.7 em relação ao ponto de coleta nº 1.
No ponto de coleta nº 5 ao verificarmos com o Termstor a quantidade de oxigênio dissolvido, constatamos uma quantidade de 6.8, pois o mesmo está se distanciando do ponto de coleta nº1, tratando-se de uma erosão ocasionada na rocha pela força da água através dos anos formando uma piscina natural, pouco profunda do Igarapé Lagoa Azul, com o fluxo de água mais lento e menos intenso, apresentando portanto a mesma quantidade de oxigênio dissolvido que o ponto de coleta nº 1.
No ponto de coleta nº 6 ao verificarmos com o Termstor a quantidade de oxigênio dissolvido, constatamos uma quantidade de 7.5, pois o mesmo está a 764 metros de distância do ponto de coleta nº1, tratando-se de uma lagoa, pouco profunda, conhecida com Lagoa Azul, com o fluxo de água lento, apresentando portanto um aumento na produção de oxigênio, com uma diferença de oxigênio dissolvido de 0.3 em relação ao ponto de coleta nº 1.
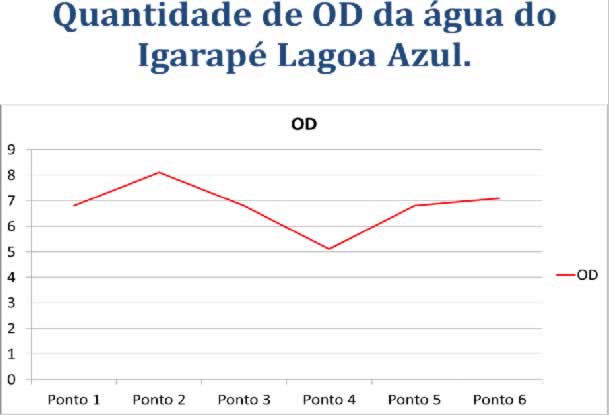
Os resultados das análises de oxigênio dissolvido na água do igarapé Lagoa Azul nos mostram uma ótima oxigenação, porém para Shiavenatti tais rios são abióticos em razão de uma combinação natural que impedem condições favoráveis à vida.
pH E ALCALINIDADE DA ÁGUA DO IGARAPÉ LAGOA AZUL
Para as análises da quantidade de pH na água do Igarapé Lagoa Azul, foram utilizado medidor de pH digital ou eletrônico, para registrar diretamente nas várias profundidades da coluna d’água. Estas análises foram realizadas no próprio igarapé Lagoa Azul, tendo seu primeiro ponto próximo à sua montante à temperatura ambiente de 27ºc, tendo início às 15:30 horas da tarde.
Para as análises de pH na água do Igarapé Lagoa Azul, foram utilizadosdois tipos de análise, a primeira foi realizada com medidor digital diretamente na fonte nos diferentes pontos de coleta, onde também foram colhidas amostras de água em pequenos frascos, com suas devidas identificações e levadas ao laboratório para que fosse feita a segunda análise através de titulação, acarretando resultados diferentes.
Pôde-se constatar a oscilação em sua temperatura, principalmente onde o fluxo de água é mais intenso ou menos intenso, conforme mostra a tabela a seguir:
Tabela 8: Resultados Obtidos das Análises de pH realizadas nos Pontos de Coleta de Água do Igarapé Lagoa Azul
|
AMOSTRAS |
pH |
|
Ponto de Coleta nº 1 |
5.7 mg/L |
|
Ponto de Coleta nº 2 |
6.6 mg/L |
|
Ponto de Coleta nº 3 |
6.6 mg/L |
|
Ponto de Coleta nº 4 |
5.9 mg/L |
|
Ponto de Coleta nº 5 |
5.9 mg/L |
|
Ponto de Coleta nº 6 |
6.9 mg/L |
No ponto de coleta nº 1, ao analisarmos o pH da água com o medidor digital, constatamos um pH de 5,7, pois o mesmo está mais próximo a montante do Igarapé Lagoa Azul, tratando-se de uma pequena queda dágua com o fluxo de água mais intenso apresentando portanto, o maior índice de acidez em nossa pesquisa.
Nos pontos de coleta nº 2 e nº 3 ao analisarmos o pH da água com medidor digital, constatamos um pH de 6,6, pois os mesmos começam a se distanciar da montante do Igarapé Lagoa Azul e do ponto de coleta nº 1. Embora os dois pontos apresentem características geográficas diferentes o resultado obtido na análise de pH foi exatamente o mesmo de 6,6.
Nos pontos de coleta nº 4 e nº 5 ao analisarmos o pH da água com medidor digital, constatamos um pH de 5,9, pois os mesmos encontram-se distantes da montante do Igarapé Lagoa Azul e do ponto de coleta nº 1. Os dois pontos apresentam as mesmas características geográficas e o resultado obtido na análise de pH foi exatamente o mesmo de 5.9.
No ponto de coleta nº 6, ao analisarmos o pH da água com o medidor digital, constatamos um pH de 6,9, o mesmo está bem distante da montante do Igarapé Lagoa Azul. Trata-se de uma pequena lagoa, conhecida como Lagoa Azul com o fluxo de água lento, sendo bastante freqüentada por banhistas, apresentando portanto, o pH mais próximo de 7.
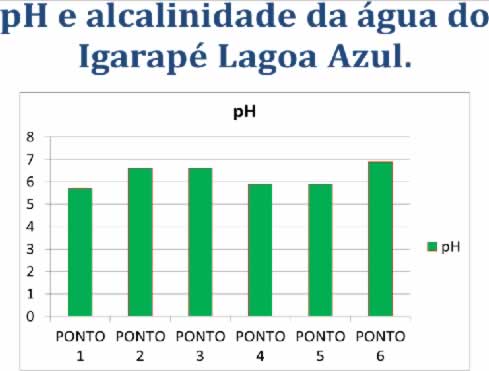
Para as análises de pH nas amostras da água colhidas do Igarapé Lagoa Azul, realizadas no laboratório do Colégio Estadual de Ensino Médio Presidente Fernando Henrique Cardoso foram utilizados como reagente de pH sal de ácido Toluenossulfônico e tabela de cores indicadoras do kit de análise de água.
Essas análises em laboratório foram realizadas 24 horas após a coleta das amostras de água do Igarapé Lagoa Azul à temperatura ambiente de 17ºc.
Foram admistradas 4 gotas de reagente de pH (sal de ácido Toluessulfônico) para cada 5 ml das amostra de água coletadas no Igarapé Lagoa Azul, diretamente no recipiente do kit de análise de água, onde foram obtidos os seguintes resultados:
Tabela 9: Resultados Obtidos Para as Análises de pH e Alcalinidade das Amostras de Água Coletadas no Igarapé Lagoa Azul, Realizadas em Laboratório.
|
AMOSTRAS |
pH |
|
Ponto de Coleta nº 1 |
7.6 mg/L |
|
Ponto de Coleta nº 2 |
7.4 mg/L |
|
Ponto de Coleta nº 3 |
7.2 mg/L |
|
Ponto de Coleta nº 4 |
7.2 mg/L |
|
Ponto de Coleta nº 5 |
7.2 mg/L |
|
Ponto de Coleta nº 6 |
7.4 mg/L |
No primeiro caso, com as análises realizadas no local da coleta com medidor digital foi obtido um resultado de pH levemente ácido, entre 5.7 e 6.9
No segundo caso, com as análises realizadas em laboratório através de titulação foi obtido um pH mais alcalino, entre 7.2 e 7.6.
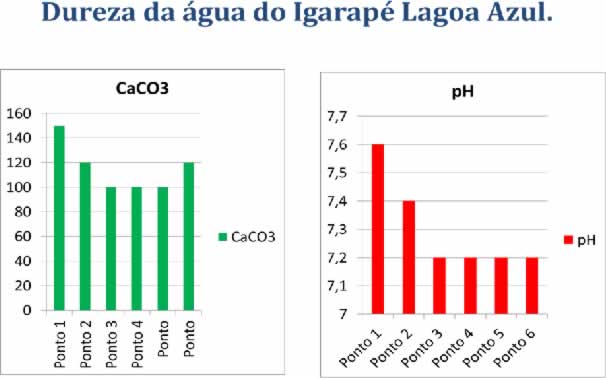
Os resultados das análises de pH da água do Igarapé Lagoa Azul estão numa escala de 5.7 a 7.6. Estando portanto, segundo Deberdt, dentro dos parâmetros considerados ideais para águas doces superficiais, que obedecem uma escala de 4 a 9. Porém, para Pontin um pH abaixo de 6 afeta completamente a vida no ambiente aquático em questão.
DUREZA DA ÁGUA DO IGARAPÉ LAGOA AZUL
Para as análises de duereza nas amostras de água colhidas do Igarapé Lagoa Azul, realizadas no laboratório do Colégio Estadual de Ensino Médio Presidente Fernando Henrique Cardoso, primeiramente foi analisado o pH para se chegar ao índice de basicidade ou alcalinidade das amostras de água.
Essas análises em laboratório foram realizadas 24 horas após a coleta das amostras de água do Igarapé Lagoa Azul, à temperatura ambiente de 17ºc.
Foram utilizados como reagente de pH sal de ácido Toluenossulfônico, colorímetro e tabela de cores indicadoras do kit de análise de água.
Para as análises de dureza nas amostras de água coletadas no Igarapé Lagoa Azul, realizados através do método de titulação, foram utilizados: 1 pisseta, 1 beker de 250 ml, titulante AT1 ( sais de ácido benzóico ), e reagente AT2 ( sais de ácido toluenossulfônico ), ambos contidos no kit de análise de água do laboratório.
Para a análise de dureza da amostra de água do ponto de coleta nº1, foram realizados os seguintes processos: foram colocados com a pisseta 100ml da amostra de água em um beker de 250ml, 3 gotas de titulante AT1 e foram adicionadas 15 gotas de titulante AT2, até que sua cor mudasse de azul para rosa.
Para a análise de dureza da amostra de água do ponto de coleta nº 2, foram realizados os seguintes processos: foram colocados com a pisseta 100ml da amostra de água em um beker de 250ml, 3 gotas de titulante AT1 e foram adicionadas 12 gotas de titulante AT2, até que sua cor mudasse de azul para rosa.
Para a análise de dureza da amostra de água do ponto de coleta nº 3, foram realizados os seguintes processos: foram colocados com a pisseta 100ml da amostra de água em um beker de 250ml, 3 gotas de titulante AT1 e foram adicionadas 10 gotas de titulante AT2, até que sua cor mudasse de azul para rosa.
Para a análise de dureza da amostra de água do ponto de coleta nº 4, foram realizados os seguintes processos: foram colocados com a pisseta 100ml da amostra de água em um beker de 250ml, 3 gotas de titulante AT1 e foram adicionadas 10 gotas de titulante AT2, até que sua cor mudasse de azul para rosa.
Para a análise de dureza da amostra de água do ponto de coleta nº 5, foram realizados os seguintes processos: foram colocados com a pisseta 100ml da amostra de água em um beker de 250ml, 3 gotas de titulante AT1 e foram adicionadas 10 gotas de titulante AT2, até que sua cor mudasse de azul para rosa.
Para a análise de dureza da amostra de água do ponto de coleta nº 6, foram realizados os seguintes processos: foram colocados com a pisseta 100ml da amostra de água em um beker de 250ml, 3 gotas de titulante AT1 e foram adicionadas 12 gotas de titulante AT2, até que sua cor mudasse de azul para rosa.
Os métodos para determinar a dureza da água usam técnicas de titulação úmida. Os resultados obtidos para as análises de cada 100 ml de água coletadas no Igarapé Lagoa Azul, realizadas através de titulação, estão melhor explicados na tabela a seguir:
Tabela 10: Resultados Obtidos das Análises de Dureza da água do Igarapé Lagoa Azul.
|
AMOSTRAS |
pH E ALCALINIDADE |
CaCO 3 |
CLASSIFICAÇÃO |
|
Ponto de Coleta nº 1 |
7.6 mg/L |
150 ppm |
Média Dureza |
|
Ponto de Coleta nº 2 |
7.4 mg/L |
120 ppm |
Mole ( branda ) |
|
Ponto de Coleta nº 3 |
7.2 mg/L |
100 ppm |
Mole ( branda ) |
|
Ponto de Coleta nº 4 |
7.2 mg/L |
100 ppm |
Mole ( branda ) |
|
Ponto de Coleta nº 5 |
7.2 mg/L |
100 ppm |
Mole ( branda ) |
|
Ponto de Coleta nº 6 |
7.4 mg/L |
120 ppm |
Mole ( branda ) |
Para as análises de dureza da água realizadas em laboratório foram obtidos resultados entre 100 e 150 ppm. Indicando que a água do Igarapé Lagoa Azul não é muito densa, e que pode segundo Frenzl ser classificada como mole.
CONCLUSÃO
Para se chegar a um resultado satisfatório nesta pesquisa sobre as propriedades físicas e químicas da água da Lagoa Azul, fez-se necessário estabelecer critérios de avaliação da qualidade da mesma. O melhor modo de fazer isso é analisar suas características e suas variáveis naturais. O resultado é surpreendente quando se percebe que os recursos hídricos sofrem ações de condicionantes que naturalmente alterariam sua composição, ainda que sem ação humana.
A obtenção das informações integradas sobre a água da Lagoa Azul dependeu basicamente do estudo das interações que ocorrem entre os fatores bióticos e abióticos que regem o funcionamento desse ecossistema. Porém, não se pode esquecer que estas interações estão vinculadas a uma escala temporal, refletindo um comportamento dinâmico e imprevisível, intrínseco a cada ambiente. Dessa forma, coube-nos promover um levantamento prévio das características ambientais da área estudada, a fim de definir o melhor ponto, horário e época para a realização dos trabalhos.
Os aspectos climatológicos da região da Lagoa Azul influenciam diretamente o corpo d’água, provocando sensíveis alterações no seu metabolismo. Num período de maior precipitação ocorre um aumento na turbidez da água em função do grande aporte de material que é carreado pelas chuvas para o corpo d’água em questão. A chamada corredeira por sua vez pode provocar uma mistura na água, ocasionando uma ressuspensão de nutrientes das partes mais profundas.
A concepção de que a questão ambiental diz respeito à relação homem-natureza não é suficiente para direcionar um processo de análise e reflexão que permita a compreensão deste relacionamento em toda a sua complexidade. É necessário, ainda, assumir-se que a construção do conhecimento sobre esta relação se realiza sob a ótica dos processos que ocorrem na sociedade. Isso significa que a chave do entendimento da problemática ambiental está no mundo da cultura, ou seja, na esfera da totalidade da vida em sociedade. Contudo, não se está afirmando que o conhecimento do meio físico-natural não seja importante para uma compreensão da problemática ambiental. É mais do que importante, é fundamental para verificarmos as implicações da ação do homem no meio natural, para o próprio meio e para o meio social. Afinal, são as práticas do meio social que determinam a natureza dos problemas ambientais que afligem a humanidade. Obviamente não estamos falando daquelas catástrofes provocadas pela natureza, como terremoto, furacões, erupção vulcânica etc”.
Atualmente, as populações dos grandes aglomerados urbanos, industriais, áreas de desenvolvimento agrícola que fazem uso intensivo de insumos químicos e áreas adjacentes a grandes projetos (minerais, hidrelétricos) já se defrontam com problemas de escassez qualitativa de água para consumo. Convém ressaltar, ainda, que se a escassez quantitativa de água constitui fator limitante ao desenvolvimento socioeconômico, a escassez qualitativa engendra problemas muito mais sérios à saúde pública, à economia e ao ambiente em geral.
REFERÊNCIAS BIBLIOGRÁFICAS
BOULOS Jr., p.22-27
CETESB, 2003
DUARTE, 2009, p. 5
GÊNESES, cap. 1, v. 1-10
ISKANDAR, Jamil Ibrahim. Normas da ABNT. Curitiba: Juruá, 2009
LIVRO ÁGUAS SUBTERRÂNEAS
LIVRO ÁGUAS SUBTERRÂNEAS
MAGOSSI, Luiz Roberto. 2003,p. 11
PELLACANI, Christhian Rodrigo Poluição das Águas Doces Superficiais &Responsabilidade Civil. Curitiba: Juruá, 2009.
QUINTAS, 2006, p. 20
Resolução do CONAMA 357/2005.
SOUZA, Luciana Cordeiro. Águas subterrâneas e a legislação brasileira. Curitiba: Juruá, 2009, p. 40
____________(2009) Águas e sua proteção, Curitiba: Juruá.