Sumário
- 1 - RESUMO
- 2 - INTRODUÇÃO
- 3 - OBJETIVOS
- 4 - REVISÃO BIBLIOGRÁFICA
- 5 - MATERIAL E MÉTODOS
- 5.1 - Material
- 5.2 - Local da pesquisa
- 5.3 - Softwares e Instrumentos utilizados
- 5.4 - Procedimentos experimentais
- 5.4.1 - ANÁLISE DO PREPARO DO CARVÃO DE CAROÇO DE AÇAÍ (CCA)
- 5.4.2 - ESTUDO DOS PARÂMETROS FÍSICOS DO SISTEMA
- 5.4.3 - DETERMINAÇÃO DO pH DE PONTO DE CARGA ZERO (pHPCZ)
- 5.4.4 - TITULAÇÃO DE GRUPOS ÁCIDOS E BÁSICOS ATRAVÉS DO MÉTODO DE BOEHM
- 5.4.5 - Determinação de grupos ácidos
- 5.4.6 - Determinação de grupos básicos
- 5.4.7 - ENSAIO DE TEMPO DE CONTATO EM LEITO FIXO
- 5.4.8 - DETERMINAÇÃO DA CURVA DE CALIBRAÇÃO ATRAVÉS DE ANÁLISE POTENCIOMÉTRICA
- 5.4.9 - ENSAIO DE ISOTERMA DE EQUILÍBRIO
- 5.4.10 - ENSAIO EM MODO DINÂMICO EM LEITO FIXO
- 6 - RESULTADOS E DISCUSSÃO
- 6.1 - Análise do preparo do carvão de caroço de açaí
- 6.2 - Estudo dos parâmetros físicos do sistema
- 6.3 - Análise do tempo de contato em leito fixo
- 6.4 - Análise do pH de ponto de carga zero (pHPCZ)
- 6.5 - Titulação de grupos ácidos e básicos através do método de Boehm
- 6.6 - Avaliação do potencial de limpeza do carvão não ativado em leito fixo
- 6.7 - Perfil de saturação do leito para diferentes recheios
- 6.8 - Determinação da curva de calibração do sistema
- 6.9 - Análise da cinética de equilíbrio em função das concentrações de contaminante
- 7 - CONCLUSÃO
- 8 - REFERÊNCIAS
1. RESUMO
Na literatura, já se encontra uma vasta quantidade de pesquisas voltadas para a aplicação de adsorventes de baixo custo visando a remoção de contaminantes, como os tensoativos. No entanto, verifica-se que a maioria dos estudos é dirigida para ensaios de batelada, em sistemas não contínuos. Do ponto de vista industrial, sistemas de batelada demandam espaço físico e tempo de operação, o que limita o volume de rejeitos destinados ao tratamento, além de ser mais dispendioso financeiramente. Desse modo, sistemas de fluxo contínuo são mais promissores por minimizar esses transtornos mencionados, além da vantagem de se trabalhar com materiais de baixo custo, que permitem que eventuais despesas com reposição de adsorvente sejam reduzidas. Ademais, o uso de carvão de açaí é uma alternativa interessante, pois além de ser resíduo industrial, também tem potencial de aplicação para contaminantes. Por conta da perspectiva de aplicação, o presente trabalho se propôs a investigar o potencial de um adsorvente de baixo custo, o carvão de caroço de açaí, na adsorção de uma solução de dodecil sulfato de sódio (SDS) em sistema de fluxo contínuo (leito fixo). Foram analisadas as características do sistema e do adsorvente, abrangendo as propriedades físicas e químicas. Os resultados mostram que o carvão apresenta uma grande carga de grupos superficiais ácidos, favoráveis a adsorção de cargas negativas, assim como o emprego de baixos valores de pH também podem favorecer a adsorção do tensoativo.
Palavras-chave: Leito fixo, carvão, caroço de açaí, adsorção, SDS.
ABSTRACT
In the literature, there is many researches aimed at the application of low cost adsorbents for the removal of contaminants, such as surfactants. However, it is verified that most of the studies are directed to batch tests in non-continuous systems. From an industrial point of view, batch systems require space for treatment and time of operation, which limits the volume of waste destined for the treatment, in addition to being more expensive. Thus, continuous flow systems are more promising for minimizing these mentioned disorders, besides the advantage of working with low cost materials that allows any expenses with adsorbent replacement are reduced. In addition, the use of acai berry coal is an interesting alternative, as besides being an industrial waste also has potential of application for contaminants. Due to the application perspective, the present work intends to investigate the potential of a low cost adsorbent, acai berry stone coal, in the adsorption of sodium dodecyl sulfate solution (DSS) in a continuous flow system. The characteristics of the system and the adsorbent were analyzed, covering the physical and chemical properties. The results show that the coal presents a great load of acidic surface groups, favorable to the adsorption of negative charges, as well as the use of low pH values can favor the adsorption of the surfactant.
Keywords: Fixed bed, acai berry, stone coal, adsorption, DSS.
2. INTRODUÇÃO
Devido ao incessante crescimento populacional, ao intenso uso industrial e agrícola e ao aumento da poluição dos recursos hídricos, ocasionado pelo despejo desordenado dos rejeitos industriais e urbanos, cresce a necessidade de promover uma consciência sustentável (BARBOSA, 2013). A sustentabilidade se baseia na preocupação acerca da qualidade de vida das gerações futuras, bem como a preservação da Terra. Esse desenvolvimento sustentável deve ser capaz de contemplar as necessidades presentes, ao mesmo tempo em que assegura o atendimento às necessidades das gerações posteriores (GOMES, NASCIMENTO & SILVA, 2016).
A água é um dos recursos naturais mais utilizados pelos seres humanos, sendo fundamental para a existência e manutenção da vida (GOMES, NASCIMENTO & SILVA, 2016). Entretanto, esse recurso, em condições próprias para uso, tem se tornado cada vez mais escasso, tendo em vista que o desperdício e o despejo inadequado de substâncias nocivas têm provocado uma crescente carga de poluentes e resíduos em corpos de água (BARBOSA, 2013). Essa poluição dos recursos hídricos é capaz de afetar a dinâmica dos ecossistemas, por meio da expansão do teor de águas insalubres e inclusão de contaminantes na cadeia alimentar. Diante desse cenário, preocupações acerca da água e sua qualidade vêm sendo alvo de discussões e pesquisas (LUZ, 2012).
Dentre os diversos tipos de contaminantes existentes, os surfactantes ou tensoativos vêm ganhando cada vez mais destaque. Esses agentes de atividade superficial, como são conhecidos, possuem baixa degradabilidade no meio ambiente e são capazes de afetar as propriedades físicas de um composto quando adsorvido em sua interface (HOLMBERG, 2003). Essas substâncias interferem na potabilidade da água através da alteração de parâmetros físicos, químicos e biológicos, como turbidez, pH, demanda química de oxigênio, entre outros (VON SPERLING, 1998). Os parâmetros citados são regulados pelos padrões de qualidade da água, estabelecidos pela Portaria n 2.914/2011 do Ministério da Saúde e pela Resolução CONAMA n 357/2005 do Ministério do Meio Ambiente.
Uma considerável quantidade de surfactantes é liberada no ambiente, tendo em vista que essas substâncias possuem uma vasta aplicação em vários setores da indústria, como higiene e produtos de limpeza, além de tratamentos de superfície e extração de petróleo (BEZERRA, 2012). Os tensoativos, quando em contato com o meio ambiente e sem tratamento adequado, provocam problemas de poluição, principalmente em cidades cortadas por rios, onde a população necessita da água para suas atividades diárias, como lavagem de roupas e louças (GOMES, NASCIMENTO & SILVA, 2016). Essa contaminação causa espuma nos rios e superfície das águas, reduzindo a dissolução de oxigênio na água e ocasionando riscos ambientais para organismos aquáticos (EICHHORN, 2012).
Os surfactantes possuem origem sintética e estruturas aromáticas complexas, o que os torna mais estáveis em condições ambientais sob os efeitos da luz, pH e ataque microbiológico, aumento a sua dificuldade de biodegradação (FU & VIRARAGHEVAN, 2001). Devido a esse fato, o tratamento desse tipo de contaminante, através de métodos de tratamento convencionais como biodigestores, torna-se pouco eficiente para a remoção desses compostos nos efluentes. Em contrapartida, o uso de membranas, por meio da nanofiltração e osmose reversa, é avaliado como uma boa proposta para a minimização desses resíduos nos efluentes, tendo em vista que essa técnica consiste na separação efetiva de moléculas de dimensões maiores do que as moléculas de água. Entretanto, esse método possui um alto custo e a uma maior complexidade no que se refere à limpeza das membranas (ANJANEYULU et al., 2005).
Diante desse cenário, a adsorção tem surgido como uma alternativa economicamente viável para a solução de alguns problemas de poluição. Os carvões vegetais, obtidos através de processos de pirólise, possuem boa capacidade de adsorção e são muito úteis na separação de misturas, assim como purificação de líquidos (OTERO, 2003). Entretanto, poucas publicações científicas têm se preocupado em estudar com mais afinco o processo de adsorção utilizando carvão vegetal como adsorvente (VASQUES, 2008). Por esse motivo, alguns produtos agrícolas vêm sendo empregados como adsorventes de baixo custo, tais como semente de girassol, polpa de maçã, palha de trigo etc; porém, estes contêm cargas negativas de celulose, capazes de repelir os tensoativos aniônicos, prejudicando a eficiência do processo de adsorção (GOMES, NASCIMENTO & SILVA, 2016).
Nesse contexto, os resíduos de açaí encontram-se como uma opção promissora, tendo em vista que são comercializadas cerca de 800.000 toneladas de frutos de açaí por ano, sendo que aproximadamente 90% desse volume corresponde aos resíduos gerados após o processamento agroindustrial do fruto (SAGRI, 2011). Para minimizar o desperdício, uma boa proposta é a produção de um carvão alternativo a partir desse produto residual, sendo utilizado, posteriormente, como leito filtrante para o tratamento de efluentes, conferindo a esse resíduo valor agregado e uma destinação final adequada, fechando o ciclo de vida do produto de maneira sustentável e ambientalmente correta (COSTA, 2014).
3. OBJETIVOS
3.1. Objetivo geral
Avaliar a influência da variação da massa de adsorvente na remoção do dodecil sulfato de sódio em efluente via leito fixo empacotado com carvão obtidos de resíduos da extração da polpa de açaí.
3.2. Objetivos específicos
-
Caracterizar o carvão obtido a partir do caroço de açaí;
-
Obter os dados experimentais relacionados à adsorção de surfactante em carvão de caroço de açaí;
-
Construir a isoterma de equilíbrio do carvão, à temperatura ambiente;
-
Calcular a eficiência de utilização do leito e de recuperação do soluto;
-
Avaliar os resultados, com base no sistema em estudo, tendo como parâmetros de avaliação os coeficientes de correlação obtidos.
4. REVISÃO BIBLIOGRÁFICA
4.1. Dodecil sulfato de sódio
O dodecil sulfato de sódio (SDS) é um composto aniônico sintético que possui uma cadeira de hidrocarbonetos simples, como ilustra a Figura 1. Essa substância é bastante utilizada em indústrias de produtos de limpeza, bem como na produção de produtos como papel e polímeros (ARAÚJO, 2016). Esse composto integra um grupo denominado de “surfactantes” ou também “tensoativos”. Esses surfactantes são caracterizados por moléculas dotadas de características anfifílicas, ou seja, possuem na mesma molécula uma porção hidrofílica ou polar, denominada cabeça, e uma cadeia hidrofóbica ou apolar, a qual é referida como cauda (GOMES, NASCIMENTO & SILVA, 2016).
Figura 1 – Representação da estrutura molecular do dodecil sulfato de sódio
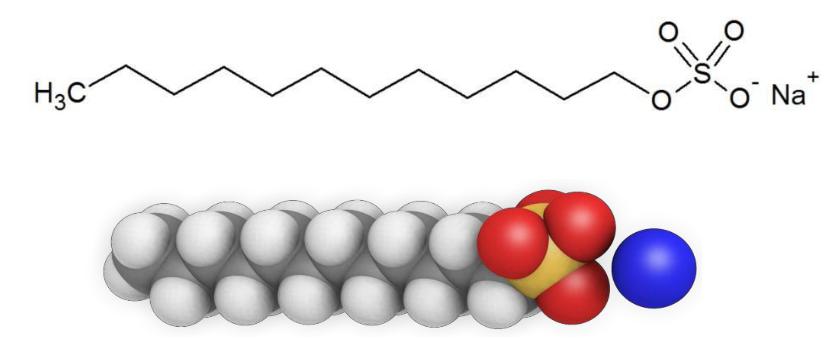
Fonte: Araújo (2016).
A presença de duas regiões distintas em uma mesma molécula é capaz de proporcionar uma grande capacidade de adsorção, seja na sua interface ar-água ou óleo-água, bem como na superfície de sólidos. Devido as suas características, essas substâncias atuam como detergentes ou agentes emulsificantes, encontrando um amplo campo de atuação (PIRES, 2002). Nesse cenário, uma considerável quantidade de surfactantes é liberada no ambiente, causando, principalmente, poluição aquática. Esses tensoativos provocam espumas nos rios e na superfície das águas. Como uma tentativa de mitigar esses problemas ambientais, a adsorção surgiu como uma potencial opção, tendo em vista o seu baixo custo e alta eficiência.
4.2. Açaí
O açaí é uma fruta de elevado valor socioeconômico para a população amazônica e é produzido por uma palmeira conhecida como açaizeiro (Euterpe oleracea, Mart.) (GANTUSS, 2006). O principal produto obtido a partir desta fruta é conhecido como "vinho do açaí", sendo considerado como um alimento predominante no dia-a-dia de muitas famílias (PEREIRA & RODRIGUES, 2013). O fruto do açaí possui formato arredondado, com diâmetro de 1 a 2 cm e peso médio variando de 0,8 a 2,3 g. Além disso, seu epicarpo possui cor violáceo-púrpura quase negro. O mesocarpo é bastante fino, dispondo de apenas 1 a 2 mm de espessura. A parte comestível do fruto relaciona-se ao mesocarpo e epicarpo (REIS et al., 2002).
As palmeiras localizam-se, principalmente, no baixo Amazonas, Tocantins, Maranhão e Amapá, chegando até as Guianas e a Venezuela. Devido a sua cor roxa escura, seu sabor exótico e seu alto valor nutricional, acabou ganhando o interesse de consumidores no mundo inteiro (COSTA, 2014). Ademais, quanto a sua utilização, o açaí é extremamente versátil. Ele pode ser empregado como planta ornamental no paisagismo, na cobertura de moradias de áreas rurais, na alimentação, como remédio – vermífugos, como ração animal, como adubo orgânico, etc. A Figura 2, descreve as diversas aplicações do fruto do açaizeiro. No que se refere ao mercado, a demanda por açaí é crescente, sendo comercializado em todo o território brasileiro, não se restringindo apenas à região produtora (JUNQUEIRA, BASSO & SOUZA, 2017).
Figura 2 – Fluxograma acerca das diversas aplicações do fruto do açaizeiro
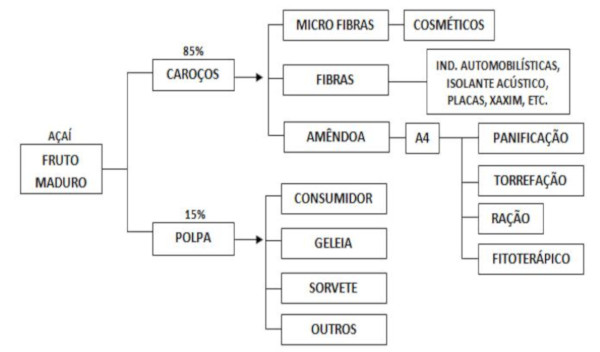
Fonte: Costa (2014).
Em meio a esse contexto, observa-se que o caroço de açaí é considerado como o principal subproduto do processamento do fruto para a obtenção da polpa. (CORDEIRO et al., 2017). O caroço constitui aproximadamente 83% do fruto e é formado por um pequeno endosperma sólido ligado a um tegumento que na maturidade é rico em celulose, hemecelulose e cristais de inulina, antes é rico em lipídeos. Um epicarpo fibroso, rico em sílica e um endocarpo pouco lenhoso (REIS et al., 2002). Devido à enorme quantidade de açaí comercializada atualmente, os resíduos gerados são muito grandes. Esse resíduo consiste basicamente em caroço, sementes e fibras (RANGEL, 2014). A Figura 3 representa o caroço de açaí com fibras.
Figura 3 – Representação do caroço de açaí com fibras

Fonte: Mesquita (2014).
4.2.1. O PROBLEMA DO DESCARTE INADEQUADO DOS RESÍDUOS DO AÇAÍ
A Política Nacional de Resíduos (BRASIL, 2012) determina que todos os resíduos devem possuir um destino ambientalmente adequado. Algumas maneiras de evitar danos à saúde pública e minimizar os impactos ambientais é através da reciclagem, compostagem, recuperação ou aproveitamento energético. Entretanto, observa-se que os resíduos originados pelo despolpamento do fruto do açaí estão sendo tratados como lixo urbano, o que ocasiona diversos transtornos para a coleta e faz com que esses rejeitos não possuam o tratamento adequado (COSTA, 2014). Esse descarte inapropriado é responsável por produzir entulhos nas ruas das cidades, terrenos baldios e lixões clandestinos, podendo gerar gases de efeito estufa quando reagidos com outros elementos (CORDEIRO et al., 2017). Além disso, esse caroço é um material de difícil decomposição, por apresentar um alto teor de lignina, variando de 11,5 a 24% (PEREIRA & RODRIGUES, 2013).
Uma possível solução para essa problemática seria o desenvolvimento de projetos que promovessem o beneficiamento do caroço do açaí por parte do poder público, frisando a importância de um destino final ecologicamente correto a esse resíduo. Todavia, a inexistência dessas medidas estimula o desenvolvimento de pesquisas relacionadas a um melhor aproveitamento desse subproduto (COSTA, 2014). Esse rejeito pode ser transformado em combustível de biomassa verde, na forma de peletes, possuindo diversas aplicações, tais como geração de energia elétrica, mecânica e gás combustível (CORDEIRO et al., 2017).
Além disso, o elevado potencial calorífico que o caroço de açaí possui reforça a sua utilidade para a geração de energias diversas. Estudos comprovam que a potência calorífica do caroço no processo de combustão figura em torno de 4.500 Kcal/Kg. A composição química desse subproduto também apresenta uma alta quantidade de celulose, lignina e um baixo teor de cinza e umidade, que enfatizam a sua possível aplicação para a produção de carvão vegetal, conferindo valor agregado a esse resíduo (CORDEIRO et al., 2017). A Tabela 1 descreve a composição química do caroço de açaí.
Tabela 1: Composição química do caroço de açaí
|
Umidade |
9,60% |
|
Extrato estéreo |
3,01% |
|
Extrato alcoólico |
9,32% |
|
Extrato aquoso |
2,80% |
|
Proteínas brutas |
4,34% |
|
Hemicelulose |
12,26% |
|
Celulose |
34,41% |
|
Lignina |
12,72% |
|
Cinzas |
1,34% |
Fonte: Reis et al. (2002).
4.3. Pirólise
Os materiais lignocelulósicos possuem biopolímeros em sua composição, que consistem em vários tipos de células, cujas paredes celulares são compostas de celulose, hemicelulose e lignina. Esses três componentes essenciais, quando combinados, tornam-se insolúveis e são difícil separação. Umas das formas mais antigas e simples de converter esses materiais lignocelulósicos em outros tipos de químicos é através da pirólise. Esse processo consiste, basicamente, na degradação de materiais macromoleculares a partir do calor e em ausência de oxigênio. Durante a pirólise ocorrem reações primárias e secundárias (MEIER & FAIX, 1999). Esse fenômeno também pode ser chamado de termólise ou craqueamento térmico e é especialmente adequado para a reciclagem química de resíduos. A Figura 4 ilustra um resumo esquemático acerca do processo de pirólise aplicado a biomassa. (PARADELA, 2012).
Figura 4 – Esquema de um processo de pirólise aplicado a biomassa
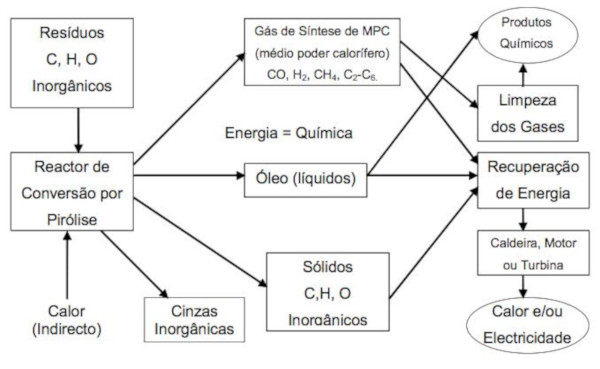
Fonte: Paradela (2012).
O termo pirólise é responsável por caracterizar a decomposição térmica de materiais que contém carbono, em ausência total de oxidante. Dessa forma, madeira, resíduos agrícolas ou qualquer outro tipo de material orgânico é capaz de sofrer decomposição, originando três diferentes fases. A primeira fase é a sólida, conhecida como carvão vegetal, a segunda fase é a gasosa e a terceira é a líquida, normalmente designada de fração pirolenhosa. Além disso, o tipo de matéria orgânica utilizada no procedimento é capaz de variar a presença de oxigênio, sendo que a introdução desse composto permite a continuidade desse fenômeno, proporcionando um aumento de rendimentos (PANNIRSELVAM et al., 2005).
No que se refere às fases formadas durante a pirólise, a fração sólida consiste principalmente em cinzas e carbono, sendo este dependente da temperatura empregada no processo. Esses produtos podem ser utilizados para a fabricação de carvão vegetal e também como combustíveis (LORA, 2012). Já a fase líquida, também conhecida como óleos pirolíticos, constitui-se de uma mistura complexa de componentes aromáticos e alifáticos oxigenados. De modo geral, essa fração líquida é caracterizada por hidrocarbonetos que possuem um importante conteúdo energético, podendo ser aproveitada em câmaras de combustão, motores a diesel e turbinas (SANTOS, 2017). Além disso, a fração gasosa também é combustível, sendo constituída, em sua maior parte, por hidrocarbonetos (LORA, 2012).
No processo de pirólise do caroço de açaí, a hemicelulose é o primeiro componente a sofrer decomposição, geralmente entre 200 e 260C. Essa decomposição produz ácido acético, furfural e furano. Já a celulose se degrada entre temperaturas que variam de 240 a 350C, resultando principalmente em formaldeído, hidroxiacetaldeído, acetol, levoglucosano e 5-hidroximetilfurfural. Ademais, a lignina, por possuir maior complexidade estrutural, forma uma enorme variedade de produtos, como pequenas quantidades de fenóis monoméricos e fragmentos oligoméricos. E, por último, tem-se a fração mais pesada do bio-óleo, sendo o último componente a se degradar, em temperaturas que podem ir de 280 a 500C. Essa última degradação é capaz de produzir fenol e seus derivados, como catecol, resorcinol, hidroquinona, guaiacol, eugenol, siringol, cresol, dimetil fenol e trimetil fenol, além de produtos oligoméricos, principalmente em que o anel benzênico se polimeriza, como naftaleno, antraceno e bifenilo (SANTOS, 2017). A Figura 5 apresenta um resumo esquemático acerca dos principais componentes da biomassa lignocelulósica e suas transformações mediante tratamento térmico.
Figura 5 - Principais componentes da biomassa lignocelulósica e suas transformações mediante tratamento térmico
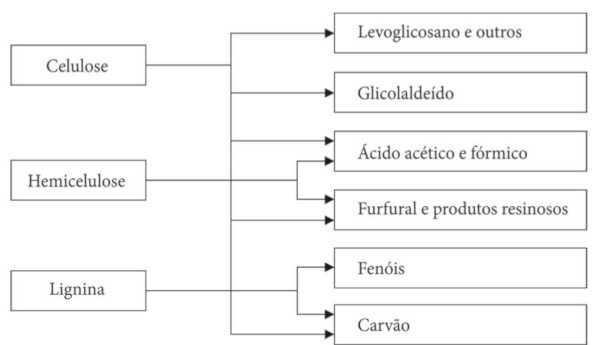
Fonte: Vieira et al. (2014).
As características dos produtos obtidos a partir da pirólise, em termos de quantidade e qualidade, estão diretamente relacionadas às condições de operação do processo. Fatores como a temperatura, a granulometria do material, a velocidade ou taxa de aquecimento, o tempo de residência, o fluxo do fluido de trabalho e as características inerentes da biomassa são variáveis importantes no desempenho e eficiência do processo (LORA, 2012). Além disso, das variáveis envolvidas no processo, tem-se a temperatura como a mais significante, visto que a mesma é capaz de influenciar na conversão da biomassa e na distribuição de produtos. A elevação da temperatura permite uma maior degradação dos componentes, aumentando a fração de gases e proporcionando a formação de um resíduo sólido denominado de biochar – que é o carvão produzido a partir de biomassa. Por outro lado, à baixas temperaturas, há maior rendimento de biochar e pouco produto líquido orgânico. Outrossim, no que condiz à taxa de aquecimento, o aquecimento gradual também favorece a formação de biochar (CANTRELL, 2012).
Os tipos de pirólise são vários e a escolha pelo melhor varia de acordo com parâmetros como a velocidade de aquecimento, a temperatura de reação, a pressão utilizada, o gás de inertização e o tempo de residência dos produtos no meio reacional (PARADELA, 2012). A Tabela 2 organiza os principais processos de pirólise utilizados para biomassa lignocelulósica. Dessa forma, podem-se definir os seguintes tipos de pirólise, que possuem o objetivo de maximizar ou minimizar determinada fração dos produtos obtidos através desse processo:
Tabela 2: Principais processos de pirólise utilizados para biomassa lignocelulósica
|
Tecnologia |
Tempo de residência |
Taxa de aquecimento |
Temperatura (C) |
Produtos obtidos |
|
Carbonização |
Dias |
Muito baixa |
400 a 500 |
Carvão vegetal |
|
Lenta (convencional) |
5 a 30 min |
Baixa |
Até 600 |
Bio-óleo, carvão e gás |
|
Rápida |
0,5 a 5 s |
Muito alta |
550 a 650 |
Bio-óleo |
|
Flash-líquido |
< 1 s |
Alta |
< 650 |
Bio-óleo |
|
Flash-gás |
< 1 s |
Alta |
> 650 |
Produtos químicos e gás combustível |
Fonte: Kimura (2009).
4.3.1. PIRÓLISE LENTA OU CARBONIZAÇÃO
Nesse tipo de procedimento, utilizam-se baixas velocidades de aquecimento (menores que 2C/s), baixas temperaturas (menores que 500C) e tempos de residência dos produtos de elevadas (gás: maior do que 5 s e sólida podem ser minutos, horas ou dias). O objetivo é maximizar o resíduo carbonáceo – sólidos –, como por exemplo na produção clássica de carvão vegetal a partir da biomassa (VIEIRA et al., 2014). Atualmente, tem se estudado muito acerca da pirólise lenta de biomassa, a fim de melhorar o rendimento do produto sólido, denominado de biochar, e garantir altos poderes energéticos (MOREIRA, 2015).
4.3.2. PIRÓLISE RÁPIDA
Utilizam-se elevadas velocidades de aquecimento (10 a 200C/s), baixos tempos de residência e temperaturas moderadas (aproximadamente 600C). Os vapores formados são rapidamente arrefecidos para condensarem, a fim de maximizar a fração líquida dos produtos (PARADELA, 2012). Além disso, o bio-óleo é o principal produto obtido e este é composto basicamente de alcatrões solúveis e insolúveis, bem como ácido pirolenhoso contendo produtos químicos tais quais o ácido acético, metanol e acetona. Esse tipo de procedimento proporciona um melhor rendimento na recuperação de co-produtos, como o carvão e o gás, além de baixo impacto ambiental e aplicabilidade do bio-óleo em escala industrial (SANTOS, 2017). A Figura 6 representa o mecanismo e a formação dos produtos durante a pirólise rápida, assim como as frações típicas de cada fase.
Figura 6 – Representação do mecanismo e distribuição dos produtos no processo de pirólise rápida
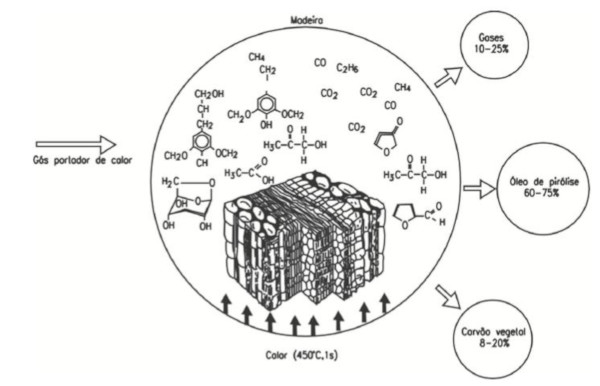
Fonte: Lora et al. (2012).
4.3.3. PIRÓLISE INSTANTÂNEA OU PIRÓLISE DE FLASH
Nesse processo, as taxas de aquecimento empregadas são ainda mais elevadas, chegando a números maiores do que 1000C/s. Além disso, os tempos de residência são bem menores, contabilizando menos de 1 s para sólidos, proporcionados pela utilização de partículas muito pequenas do material a pirolisar, objetivando maximizar a transferência de calor (VIEIRA et al., 2014).
4.4. Biocarvão ou biochar
O biocarvão é um material poroso e rico em carbono, produzido a partir da decomposição térmica de materiais orgânicos, geralmente utilizando temperaturas baixas (menores que 700C) e com presença mínima ou ausência de oxigênio (NGUYEN, 2015). Inicialmente, esse produto foi utilizado como condicionador de solos, visando o aumento da fertilidade do mesmo devido à sua elevada capacidade de absorção de água e nutrientes, além de também contribuir para a atenuação do efeito estufa, através do sequestro de gás carbônico (CASTRO et al., 2017).
É possível observar que o rendimento do biocarvão está intrinsecamente relacionado ao tipo de matéria-prima utilizada, bem como as condições durante a pirólise. Dentre todos os parâmetros do processo, constata-se que a temperatura é o mais importante. Estudos comprovam que o teor de carbono presente no biocarvão passou de 56 para 93% após uma elevação na temperatura de 300 para 800C. Além disso, o emprego de altas temperaturas (acima de 700C) resulta em uma ampliação na área superficial desse produto. Por outro lado, a taxa de aquecimento apresenta-se como o fator menos significativo no que se refere ao rendimento do biocarvão (NGUYEN, 2015).
As grandes quantidades de carbono, área superficial e porosidade do biocarvão, produzido via pirólise lenta, o fazem adequado para uma gama de finalidades (SANTOS, 2017). Apesar de a maioria dos estudos realizados atualmente estarem relacionados ao aproveitamento de biocarvão como condicionador de solos, o interesse acerca da aplicação desse produto no tratamento de águas residuais vem ganhando espaço dentre a comunidade científica. Estudos têm comprovado que o biocarvão pode ser um adsorvente muito eficiente no que refere à adsorção de metais pesados presente em soluções aquosas (NGUYEN, 2015). Diversos fatores, tais como, área superficial, propriedades moleculares do material adsorvente, grupos funcionais presentes, pH da solução e, principalmente, forças intermoleculares influenciam diretamente no processo de adsorção, podendo este ser químico ou físico (SOUZA et al., 2017).
4.5. Adsorção
A crescente contaminação química da água a partir de uma ampla gama de poluentes orgânicos e inorgânicos estimulou o desenvolvimento de tecnologias capazes de remover esses poluentes encontrados nos rejeitos. A partir desse cenário, a adsorção ganhou, nas últimas décadas, grande visibilidade como um processo de separação e purificação (NASCIMENTO et al., 2014). Esse processo apresenta um elevado potencial de aplicação industrial para a remoção ou separação de substâncias poluentes, visando a redução dos impactos ambientais causados por diversas indústrias (BARROS, 2017).
Dessa forma, a adsorção está relacionada ao enriquecimento de um ou mais componentes em uma região interfacial (FONTAN, BONOMO & COIMBRA, 2016). Essa operação de transferência de massa do tipo sólido-fluido explora a capacidade de certos sólidos em concentrar na sua superfície determinadas substâncias existentes em soluções líquidas ou gasosas, o que permite separá-las dos demais componentes dessas misturas (SANTOS, 2017). Os componentes que se unem à superfície são chamados de adsorvatos, enquanto que a fase sólida que retém o adsorvato é chamada de adsorvente (RIBEIRO, 2016).
O grau de adsorção depende das condições termodinâmicas, da superfície do adsorvente e das interações entre adsorvente e adsorvato (CAMARA, 2014). Para que essa operação seja realizada de forma satisfatória, faz-se necessário que a substância a ser adsorvida apresente afinidade com o material adsorvente (BARROS, 2017). Além disso, uma vez que os componentes adsorvidos ficam concentrados sobre a superfície externa, quanto maior for esta superfície externa por unidade de massa sólida, mais favorável será a adsorção (NASCIMENTO et al., 2014). Tendo em vista que a capacidade adsortiva por unidade de área é baixa, é importante utilizar adsorventes porosos, com grande área interna por unidade de volume (FONTAN, BONOMO & COIMBRA, 2016).
Por ser um fenômeno que ocorre quando as moléculas, ao se difundirem em uma fase fluida, são capturadas por forças atrativas de uma superfície sólida adjacente, faz-se necessário enfatizar que essa superfície apresenta descontinuidades na estrutura do sólido, disponibilizando energias residuais que não são contrabalanceadas pela vizinhança presente no corpo da estrutura. Essas forças residuais são o que se conhece por interações de Van der Waals (FONTAN, BONOMO & COIMBRA, 2016). Na maioria dos casos, o componente adsorvido é preso forte o suficiente para permitir remoção completa deste componente do fluido e uma pequena adsorção de outros componentes (BARROS, 2017).
Quando moléculas de uma fase fluida entram em contato com o sólido adsorvente, as forças de atração existentes entre o adsorvente e o adsorvato estimulam o acúmulo deste na superfície sólida (FONTAN, BONOMO & COIMBRA, 2016). A atração do sólido por certos tipos de moléculas é tão intensa que praticamente todas as moléculas incidentes podem ficar retidas até saturarem os sítios ativos ou até que as condições da superfície sofram alterações de modo a reduzir essas forças de atração (GOMIDE, 1980). A união entre o adsorvente e o adsorvato pode ser tão forte, a ponto de apresentar características de uma reação química. Esse tipo de adsorção é denominado de quimissorção ou adsorção química e é irreversível, apresentando elevado interesse no que se refere à catálise heterogênea. Por outro lado, quando a união entre o adsorvato e o adsorvente é fraca, o processo é chamado de fisissorção ou adsorção física, podendo ser invertido com facilidade (RIBEIRO, 2016). A Tabela 3 expõe, de maneira resumida, as principais características relacionadas aos fenômenos de quimissorção e fisissorção, que serão melhor abordados posteriormente.
Tabela 3: Principais características relacionadas aos fenômenos de quimissorção e fisissorção
|
Adsorção Física |
Adsorção Química |
|
Causada por forças eletrostáticas, como de van der Walls |
Causada por compartilhamento de elétrons |
|
Não há transferência de elétrons |
Há transferência de elétrons |
|
Calor de adsorção = 2~6 Kcal mol-1 |
Calor de adsorção = 10~200 Kcal mol-1 |
|
Fenômeno geral para qualquer espécie |
Fenômeno específico e seletivo |
|
A camada adsorvida pode ser removida por aplicação de vácuo à temperatura de adsorção |
A camada adsorvida só é removida por aplicação de vácuo e aquecimento a temperatura acima a de adsorção |
|
Formação de multicamada abaixo da temperatura crítica |
Somente há formação de monocamadas |
|
Acontece somente abaixo da temperatura crítica |
Acontece também a altas temperaturas |
|
Lenta ou rápida |
Instantânea |
|
Adsorvente quase não é afetado |
Adsorvente altamente modificado na superfície |
Fonte: Clark (2010).
4.5.1. QUIMISSORÇÃO OU ADSORÇÃO QUÍMICA
Esse fenômeno é realizado a partir de interações altamente específicas entre o adsorvente e a primeira camada de soluto adsorvido, envolvendo a partilha de elétrons (FONTAN, BONOMO & COIMBRA, 2016). As moléculas adsorvidas reagem quimicamente com a superfície, proporcionando o rompimento e a formação de ligações químicas (SANTOS, 2017). O adsorvato sofre uma mudança química e é geralmente dissociado em fragmentos independentes, formando radicais e átomos ligados ao adsorvente (RIBEIRO, 2016). Além disso, a liberação de energia decorrente desse processo é aproximadamente 10 vezes maior que a entalpia de condensação e proporciona a formação de uma monocamada, ou seja, a adsorção ocorre apenas na primeira camada de moléculas adsorvidas na superfície do sólido. A quimissorção geralmente é uma operação irreversível, no qual a dessorção da substância tem como consequência a sua modificação química (FONTAN, BONOMO & COIMBRA, 2016). Entretanto, é necessário ressaltar que nem todas as moléculas presentes no fluido são possíveis de serem adsorvidas quimicamente, somente aquelas capazes de se ligar ao sítio ativo (NASCIMENTO et al., 2014).
4.5.2. FISISSORÇÃO OU ADSORÇÃO FÍSICA
A operação de fisissorção é resultado de forças de atração intermoleculares fracas entre o adsorvente e a molécula a ser adsorvida, sendo um processo rápido e reversível. Essa atração é decorrente das forças de Van der Waals (FONTAN, BONOMO & COIMBRA, 2016). Observa-se que as forças intermoleculares de atração entre as moléculas na fase fluida e da superfície sólida são maiores que as forças atrativas entre as moléculas do próprio fluido (RIBEIRO, 2016). Esse fenômeno pode ocorrer em toda a superfície adsorvente, o que o faz ser conhecido como não-localizado. Além disso, como não há formação ou quebra de ligações, a natureza química do adsorvato não sofre alterações. Outro fato característico deste tipo de adsorção é a possibilidade de haver várias camadas superpostas de moléculas adsorvidas (NASCIMENTO et al., 2014). Uma curiosidade acerca da fisissorção é que um aumento na temperatura provoca uma diminuição notável na quantidade adsorvida pela superfície do sólido, portanto, esse processo geralmente ocorre a baixas temperaturas (SANTOS, 2017)
4.6. Adsorção em coluna de leito fixo
A adsorção em coluna de leito fixo tem sido amplamente aplicada em muitas áreas de separação e purificação. Ao lidar com um sistema multicomponente, o desempenho de um leito fixo é avaliado através da análise das curvas de concentração vs. tempo. Essas curvas, chamadas de “breakthrough” ou de ruptura, têm sido consideradas a base mais comum para a avaliação do comportamento de adsorventes (LUZ, 2012). O leito fixo consiste em um vaso cilíndrico vertical que contém partículas sólidas adsorventes empacotadas, através do qual se escoa a fase fluida. No que se refere a um escoamento de líquido, o fluxo geralmente é descendente, natural ou pressurizado. A coluna é operada em constante inundação, de modo a evitar a presença de ar no interior da mesma. Inicialmente, todo o leito contendo as partículas de adsorvente está isento de adsorvato. Ao começar o escoamento do fluido, inicia-se também o fenômeno de transferência de massa. Nesse tipo de processo, observa-se que a concentração de soluto em ambas as fases varia de acordo com o tempo de processo e posição no leito (FONTAN, BONOMO & COIMBRA, 2016).
Inicialmente, ao entrar em contato com a primeira porção do leito, o soluto passa a ser rapidamente adsorvido, com o efluente estando livre de soluto. Posteriormente, o soluto passa a atingir as zonas mais próximas à saída da coluna, conforme ocorre a saturação das camadas iniciais do leito, até que a concentração final esteja suficientemente próxima à inicial, indicando a total saturação do leito (DIAS, RODRIGUES & MUNIZ, 2017). Após a completa saturação da fase sólida, observa-se um aumento gradativo da concentração de soluto na saída do leito, até atingir um valor arbitrário cAb, denominado de ponto de ruptura (break point). Esse valor caracteriza a quantidade máxima de soluto admitida para descarte e localiza-se entre 1 a 5% da concentração inicial de soluto na solução (FONTAN, BONOMO & COIMBRA, 2016). A Figura 7 ilustra o comportamento de uma curva de ruptura conforme o leito fixo alcança o seu ponto de saturação total.
Figura 7 – Representação do comportamento da curva de ruptura conforme o leito fixo alcança o seu ponto de saturação total
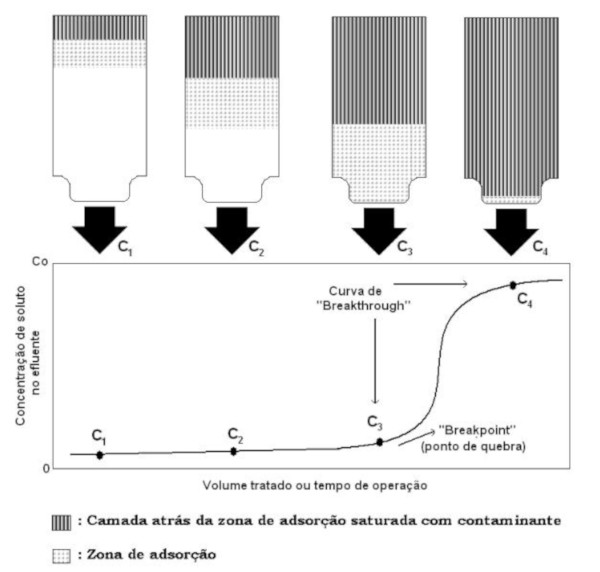
Fonte: Shahalam et al. (1997).
Um dos elementos mais importantes associados ao projeto de uma coluna de adsorção de leito fixo é determinar quando a coluna alcançará o ponto de saturação. A descrição da taxa de transferência de massa para o adsorvente pode ser obtida por meio das curvas de ruptura. Estas são desenvolvidas passando o fluido que contém o adsorvato através da coluna empacotada com adsorvente, monitorando a concentração de saída. Uma curva de ruptura típica é dada como a razão entre a concentração do efluente (Csaida) pela concentração de afluente (Centrada) vs. o tempo (SHAHALAM et al., 1997).
Inicialmente, a maior parte da transferência de massa ocorre próxima à entrada do leito, onde o fluido entra em contato com o adsorvente. Caso a fase sólida esteja livre de adsorvato no início da operação, a concentração do mesmo na fase fluida decai exponencialmente de acordo com a distância percorrida pelo fluido em um instante de tempo. Depois de decorrido certo intervalo de tempo, o adsorvente próximo à entrada torna-se saturado e a maior parte da transferência de massa ocorre dentro do leito. O formato da curva de ruptura ao longo do eixo do tempo depende da capacidade de adsorção da coluna, da concentração de alimentação e da vazão de alimentação (RIBEIRO, 2016).
Além disso, a compreensão da dinâmica da coluna de adsorção de leito fixo para a modelagem é uma difícil tarefa, devido à forte não-linearidade nas isotermas de equilíbrio, à interferência e efeitos de competição de solutos pelos sítios ativos do adsorvente, à resistência de transferência de massa entre a fase fluida e a fase sólida, e ao fenômeno de dispersão fluidodinâmico (LUZ, 2012).
5. MATERIAL E MÉTODOS
5.1. Material
Para a realização dos ensaios, foi utilizada uma solução de dodecil sulfato de sódio (SDS), da marca Merck Millipore, número de catálogo 817035, número CAS 151-21-3 e massa molar de 288,37 g/mol, além de carvão não ativado obtido a partir do caroço de açaí.
5.2. Local da pesquisa
Os experimentos realizados no presente projeto foram executados no Laboratório de Materiais e Engenharia de Processos - LaMEP/LEPEQ, Laboratório de Design Cerâmico – LDC/DEDET e Central Analítica de Química, localizados na Universidade Federal do Maranhão.
5.3. Softwares e Instrumentos utilizados
Para as medidas realizadas durante os experimentos foram utilizados um condutivímetro digital portátil modelo CD-850, com faixa de medição de 0 a 200 S e precisão de ± 1% + 2 dígitos; um pH-metro digital modelo WTW pH 330i, com exatidão de ± 0,003 pH e acoplado a eletrodo combinado de membrana de vidro; uma mesa agitadora orbital modelo TE-141, fabricada pela Tecnal e uma bomba peristáltica modelo BP200, fabricada pela Milan. Além disso, os gráficos foram plotados através do software Origin 8.
5.4. Procedimentos experimentais
5.4.1. ANÁLISE DO PREPARO DO CARVÃO DE CAROÇO DE AÇAÍ (CCA)
Inicialmente, os caroços de açaí foram separados em dois grupos para posterior comparação nos estudos: caroço sem fibras e com fibras. Após a separação, os caroços foram submetidos à lavagem com água corrente e secagem em estufa durante 3 horas à 100°C. Em seguida, foram colocados em um forno e submetidos a uma calcinação, sendo, posteriormente, separados novamente em mais dois grupos: 350°C e 400°C, ambos com duração de 3 horas e taxa de aquecimento de 10°C por minuto. O carvão preparado seguiu, então, para lavagem em água corrente e posterior secagem em estufa durante 3 horas à 100°C. Depois, esse carvão passou por um peneiramento no qual foi obtida a faixa granulométrica desejada, seguida de armazenamento.
5.4.2. ESTUDO DOS PARÂMETROS FÍSICOS DO SISTEMA
Nessa etapa, são apresentados os dados a respeito do sistema empregado para a realização do processo de adsorção em leito fixo, com informações acerca da coluna e do adsorvente empregado. Para o estudo das características físicas do sistema foram utilizadas as fórmulas de densidade aparente (Equação 1), volume aparente (Equação 2), densidade de empacotamento (Equação 3) e porosidade do leito (Equação 4). Essas expressões matemáticas foram obtidas através de informações do leito e da amostra, tais como área e volume da coluna vazia e ensaio de proveta para avaliação da densidade aparente.
(1)
Onde madsorvente corresponde à massa de adsorvente presente na proveta (g) e Vproveta se refere ao volume da proveta (cm3).
(2)
Sendo mads.leito referente à massa de adsorvente presente no leito (g) e ρA, a densidade aparente (g/cm3), já previamente calculada.
(3)
No qual mads.leito é correspondente à massa de adsorvente presente no leito (g) e Vleito caracteriza o volume total do leito (cm3).
(4)
Onde ρE é a densidade de empacotamento (g/cm3) e ρA, a densidade aparente (g/cm3).
5.4.3. DETERMINAÇÃO DO pH DE PONTO DE CARGA ZERO (pHPCZ)
O pH de ponto de carga zero foi determinado a partir da metodologia apresentada por Crispim (2009), que empregou o método desenvolvido por Strelko e Malik (2002). Esse método consistiu em misturar as amostras de CCA a 20 ml de solução de NaCl 0,1 N, mantendo-as sob agitação durante 24 horas, na qual acrescentou-se, gradualmente, NaOH ou HCl 0,1 N, de tal modo que se obtivesse uma sequência de valores de pH no intervalo de 2 a 11, com variação de uma unidade entre um valor e outro.
5.4.4. TITULAÇÃO DE GRUPOS ÁCIDOS E BÁSICOS ATRAVÉS DO MÉTODO DE BOEHM
5.4.5. Determinação de grupos ácidos
Para avaliação de grupos ácidos, foram utilizadas soluções padrões de carbonato de cálcio, bicarbonato de sódio e hidróxido de sódio, todas em concentração 0,1 mol/L. Em três erlenmeyers de 250 mL, adicionou-se 0,5 gramas de CCA, pesado analiticamente, e 50 mL de uma das bases. Os recipientes foram fechados e colocados sob agitação durante 24 horas, em banho com agitação regulada, à temperatura ambiente. Em seguida, o carvão foi filtrado e a quantidade de grupos ácidos determinada, no filtrado, por titulação de retorno, como descrito na literatura (MENDHAM et al, 2002).
5.4.6. Determinação de grupos básicos
Pesou-se analiticamente uma amostra de 0,5 gramas de CCA, transferindo-a para um erlenmeyer de 250 mL, juntamente a 50 mL de solução padrão de HCl 0,1 mol/L. Em seguida, a mistura foi submetida a agitação durante 24 horas à temperatura ambiente, em banho com agitador. A solução foi filtrada e alíquotas de 10 mL foram retiradas, a fim de titulação com solução padrão de NaOH 0,1 mol/L e determinação da quantidade de grupos básicos, por grama de carvão, em termos de mmol/g.
5.4.7. ENSAIO DE TEMPO DE CONTATO EM LEITO FIXO
O teste de preenchimento do leito foi realizado com a solução estoque de surfactante (SDS 5 ppm). O leito foi analisado em três situações, sendo totalmente vazio, recheado com carvão e esferas de vidro em proporção de 1:1 em massa e completamente recheado com esferas de vidro. Foram empregadas quatro vazões no estudo, sendo de 0,040 ml/s; 0,065 ml/s; 0,087 ml/s e 0,110 ml/s. Os tempos, obtidos em duplicata, foram submetidos ao cálculo de média.
5.4.8. DETERMINAÇÃO DA CURVA DE CALIBRAÇÃO ATRAVÉS DE ANÁLISE POTENCIOMÉTRICA
Para tal, preparou-se 5 soluções de SDS com diferentes concentrações – 1,0; 2,0; 3,0; 4,0 e 5,0 ppm – e cada solução foi submetida a agitação constante por um período de 3 min à temperatura de 25°C. Em seguida, mediu-se a condutância e registrou-se as leituras. A partir desses dados, construiu-se a curva de calibração para o presente sistema.
5.4.9. ENSAIO DE ISOTERMA DE EQUILÍBRIO
Para a realização dos experimentos em batelada, uma série de erlenmeyers foi utilizada. A cada erlenmeyer, adicionou-se 0,4 g de carvão de caroço de açaí e 50 ml de solução de SDS em concentrações de 1,0; 2,0; 3,0; 4,0 e 5,0 ppm. Os ensaios foram realizados em triplicata para cada concentração. Os erlenmeyers foram deixados sob agitação em agitador mecânico. Posteriormente, alíquotas foram retiradas para leitura no condutivimetro, após um tempo de contato de 2 h. A Figura 8 ilustra os erlenmeyers já posicionados na mesa agitadora.
Figura 8 – Representação do sistema utilizado no ensaio de isoterma de equilíbrio

Fonte: Próprio autor (2018)
5.4.10. ENSAIO EM MODO DINÂMICO EM LEITO FIXO
Nesse experimento, dois tipos de recheios foram analisados. Na primeira, a coluna foi completamente preenchida com carvão de caroço de açaí, já na segunda, a coluna foi recheada com carvão e esferas de vidro em proporção de 1:1 em massa. Após a preparação da coluna de leito fixo, conectou-se a bomba peristáltica através de mangueiras, bem como a uma área de coleta. A bomba, então, escoou a solução de SDS diretamente para o leito fixo. O recheio da coluna serviu para adsorver a solução. Posteriormente, a solução, após passar pelo leito fixo com recheio de carvão, foi coletada para a análise no condutivimetro e pH-metro. A Figura 9 representa o sistema utilizado durante o ensaio de leito fixo para coluna recheada com carvão e esferas de vidro em proporção de 1:1 em massa.
Figura 9 – Representação do sistema experimental para ensaio em leito fixo

Fonte: Próprio autor (2018)
6. RESULTADOS E DISCUSSÃO
6.1. Análise do preparo do carvão de caroço de açaí
Durante a preparação e baseado na característica física do carvão, foi verificado a importância da purificação desse material, visando o aproveitamento total de suas propriedades, mediante remoção de sujeiras ou resíduos presentes na superfície do caroço de açaí e a saída da água adsorvida na superfície, bem como de compostos voláteis presentes no material estudado. Já na etapa de calcinação, foram empregadas duas temperaturas, sendo 350C e 400C. A partir de análises posteriores realizadas em ambas as amostras, verificou-se que os carvões preparados em maior temperatura apresentaram mais falhas em sua estrutura, propiciando o aparecimento de pequenos sulcos em diversos caroços carbonizados, responsáveis por diminuir a sua resistência à compressão e tornar o material mais frágil. Esta problemática dificulta a aplicação desse carvão no processo, primeiramente devido à formação de pó, causada pela compactação do leito e, segundamente, à redução da porosidade do leito, provocada pelo arraste do material particulado. A Figura 10 ilustra o carvão empregado no processo, cujo diâmetro é de 1,18 mm.
Além disso, o carvão sem fibras, apesar de apresentar-se com maior área superficial, possui como desvantagem a remoção da fibra, pois essa retirada não se dá através de processos mecânicos, fazendo-se necessário um esforço manual dispendioso e com elevada demanda de tempo para sua execução satisfatória, não sendo viável para aplicações em larga escala. Desse modo, o carvão calcinado à temperatura de 350°C e com fibras foi o selecionado para ser utilizado no projeto de adsorção em leito fixo e, posteriormente, submetido às caracterizações necessárias.
Figura 10 – Carvão de caroço de açaí à 350ºC

Fonte: Próprio autor (2018).
6.2. Estudo dos parâmetros físicos do sistema
Em relação aos parâmetros físicos do sistema, os resultados encontram-se expostos na Tabela 4. É importante ressaltar que a densidade das fibras é bem reduzida, diferente do observado para o caroço revestido por fibras, cuja densidade é próxima de um. Como consequência, a quantidade de massa requerida para preencher o leito é pequena e a porosidade do leito é baixa, o que afeta diretamente a velocidade intersticial do fluido no sistema, parâmetro importante no processo de adsorção. Os valores organizados na Tabela 4 expressam os resultados obtidos a partir de uma coluna completamente recheada com carvão não ativado.
Tabela 4: Parâmetros físicos do sistema experimental
|
Parâmetro |
Valor |
|
Diâmetro da coluna, D (cm) |
1 |
|
Comprimento da coluna, L (cm) |
30 |
|
Comprimento útil da coluna LU (cm) |
29,5 |
|
Área da coluna (cm2) |
0,7854 |
|
Volume da coluna (cm3) |
22,93 |
|
Massa de adsorvente na coluna (g) |
9,041 |
|
Densidade aparente, ρA (g/cm3) |
0,206 |
|
Densidade de empacotamento, ρE (gm/cm3) |
0,182 |
|
Volume de partículas, Vap (cm3) |
18,925 |
|
Porosidade do leito, ε |
0,12 |
Fonte: Próprio autor (2018).
6.3. Análise do tempo de contato em leito fixo
Quanto ao tempo de preenchimento, os testes para a coluna em diferentes condições através de variadas velocidades de rotação, realizados em duplicata, tiveram como resultado a montagem das Tabelas 5, 6 e 7, bem como a plotagem dos gráficos de tempo de enchimento vs. vazão da solução (Figuras 11, 12 e 13). Observa-se que o desvio entre os pontos é bem reduzido, variando em torno de poucos segundos, muito por conta de bolhas no equipamento ou deformação gradual da mangueira, provocada pelo alongamento devido ao movimento da bomba.
Os gráficos também demonstram um comportamento semelhante à curva de calibração da bomba, o que era esperado devido à condição de preenchimento da coluna não alterar a vazão do sistema e/ou diminuir a velocidade de deslocamento do fluido.
A partir de análises dos gráficos é possível observar que o perfil das curvas obtidas é bem semelhante. No que se refere à vazão de 0,040 ml/s, o tempo de contato para o leito completamente vazio contabilizou uma média de aproximadamente 500 s. Já o tempo de contato para o leito totalmente recheado somente com esferas de vidro foi de exatamente 256,2 s. E, por último, o tempo de contato para o leito recheado com carvão e esferas de vidro em proporção de 1:1 em massa, apresentou uma média de 386,4 s. Esses tempos indicam que as esferas de vidro apresentam menor resistência ao escoamento da solução, além de o volume livre para o líquido ocupar ser menor, fazendo com que esse tempo de enchimento seja mais rápido quando em comparação com os outros. Ademais, o tempo de preenchimento para o leito recheado com carvão e esferas de vidro indica que o carvão constitui um material mais poroso do que as esferas, influenciando assim, na sua média. A mesma análise vale para todos os outros valores de vazão utilizados, tendo em vista que é possível observar um comportamento semelhante nos gráficos obtidos.
6.3.1. LEITO TOTALMENTE VAZIO
Tabela 5: Análise empírica do tempo de preenchimento para o leito vazio
|
Tempo |
0,040 (ml/s) |
0,065 (ml/s) |
0,087 (ml/s) |
0,110 (ml/s) |
|
T1 (s) |
501,6 |
312,6 |
214,8 |
187,2 |
|
T2 (s) |
496,2 |
312,6 |
214,2 |
187,2 |
|
Média |
498,9 |
312,6 |
214,5 |
187,2 |
Fonte: Próprio autor (2018).
Figura 11 – Vazão em função do tempo de preenchimento para leito vazio
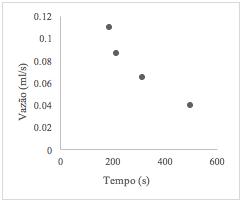
Fonte: Próprio autor (2018).
6.3.2. LEITO COMPLETAMENTE PREENCHIDO COM CARVÃO SEM ATIVAÇÃO E ESFERAS DE VIDRO EM PROPORÇÃO DE 1:1 EM MASSA
Tabela 6: Análise empírica do tempo de preenchimento para leito em proporção de 1:1
|
Tempo |
0,040 (ml/s) |
0,065 (ml/s) |
0,087 (ml/s) |
0,110 (ml/s) |
|
T1 (s) |
387,6 |
254,4 |
183,0 |
133,8 |
|
T2 (s) |
385,2 |
257,9 |
185,4 |
136,7 |
|
Média |
386,4 |
256,1 |
184,2 |
135,2 |
Fonte: Próprio autor (2018).
Figura 12 – Vazão em função do tempo de preenchimento para leito em proporção 1:1
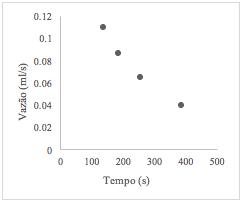
Fonte: Próprio autor (2018).
6.3.3. LEITO COMPLETAMENTE PREENCHIDO COM ESFERAS DE VIDRO
Tabela 7: Análise empírica do tempo de preenchimento para leito com esferas de vidro
|
Tempo |
0,040 (ml/s) |
0,065 (ml/s) |
0,087 (ml/s) |
0,110 (ml/s) |
|
T1 (s) |
261,6 |
154,2 |
128,4 |
87,6 |
|
T2 (s) |
250,8 |
180,0 |
127,2 |
87,6 |
|
Média |
256,2 |
167,1 |
127,8 |
87,6 |
Fonte: Próprio autor (2018).
Figura 13 – Vazão em função do tempo de preenchimento para leito com esferas de vidro
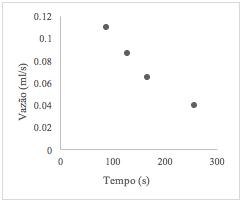
Fonte: Próprio autor (2018).
6.4. Análise do pH de ponto de carga zero (pHPCZ)
A avaliação do ponto de carga zero de um determinado compósito é necessário quando se quer estudar os fenômenos de superfície que envolvem a adsorção, pois fornece conhecimentos vitais sobre o comportamento de cargas existentes nas superfícies dos adsorventes em função do pH do meio, bem como o grau de ionização das espécies do adsorvato (BARBOSA, 2013). Esse parâmetro pode ser uma condição importante quando levado em consideração o tipo de adsorvato a ser trabalhado, devido ao fato de que alterações no pH do meio podem afetar positivamente o fenômeno da adsorção. A Figura 14 mostra o gráfico de ∆pH, que é obtido através da diferença entre o pHinicial e o pHfinal em função do pHinicial.
Figura 14 – Análise do pH de ponto de carga zero
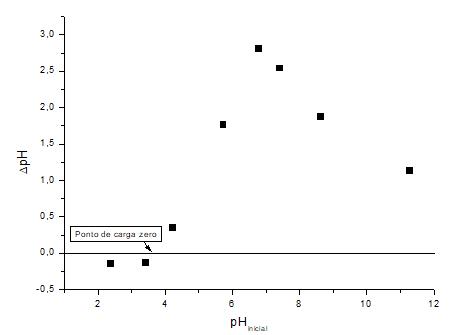
Fonte: Próprio autor (2018).
A partir do pHPCZ obtido, de aproximadamente 3,60, observa-se a formação de uma crescente curva ascendente, que atinge o seu ápice em um pH próximo a 7. Abaixo do pH de ponto de carga zero, a superfície encontra-se carregada positivamente, o que favorece a adsorção de ânions e, acima deste valor, a carga superficial é negativa, o que promove a atração por compostos catiônicos (GOMES, NASCIMENTO & SILVA, 2016). Desta forma, é possível constatar que a adsorção do dodecil sulfato sódico, um tensoativo aniônico, se dá em pH abaixo do pHPCZ, pois nessa faixa de pH tem-se que as interações entre o tensoativo e o carvão de caroço de açaí podem estar sendo favorecidas pela contribuição dos grupamentos protonados do meio.
6.5. Titulação de grupos ácidos e básicos através do método de Boehm
O procedimento de titulação foi executado para analisar quantitativamente os grupamentos ácidos e básicos incorporados na superfície do material. Os resultados obtidos por meio da utilização da metodologia de Boehm para a determinação de grupos superficiais do CCA é apresentado na Tabela 8.
Tabela 8: Análise quantitativa dos grupos superficiais presentes no CCA
|
Grupos superficiais |
Concentração |
|
|
mmol/g |
% |
|
|
Carboxílicos |
0 |
0 |
|
Lactônicos |
2,93 |
42,10 |
|
Fenólicos |
4,03 |
57,90 |
|
Básicos |
0 |
0 |
Fonte: Próprio autor (2018).
Todos os grupamentos ácidos normalmente encontrados em carvões ativados, com exceção dos grupos carboxílicos, também se fazem presentes no carvão empregado no projeto. É observado que os grupos fenólicos correspondem a maior parte dos grupos superficiais, contabilizando mais de 50% do total. Os grupos lactônicos também apresentam um percentual elevado, correspondendo a 42%. Outros grupos não tiveram quantidade analítica detectada.
Na literatura, geralmente os grupos de maior concentração são os fenólicos e lactônicos (BARBOSA, 2013). Ambos os grupos são considerados relativamente fracos e se dissociam em valores de pH mais altos do que os grupamentos de ácidos carboxílicos. Estes, quando presentes em concentrações elevadas, em comparação com os outros grupos funcionais, melhoram o processo de adsorção, principalmente se o pH de trabalho estiver situado na faixa ácida, que favorece a protonação desses grupos (TSANG et al., 2007).
6.6. Avaliação do potencial de limpeza do carvão não ativado em leito fixo
Para esse estudo, foi utilizado um carvão não ativado de caroço de açaí não lavado, com intuito de verificar o perfil de limpeza da amostra de carvão perante um fluxo de água, a fim de analisar a condutividade e eficiência de limpeza em comparação ao método de tratamento convencional. A vantagem seria de diminuir o volume de água utilizado durante a prática de limpeza, além de tentar reduzir o tempo operacional. A Figura 15 ilustra o comportamento dos gráficos obtidos através das análises.
Figura 15 - Análise da capacidade de limpeza para diferentes alturas de carvão
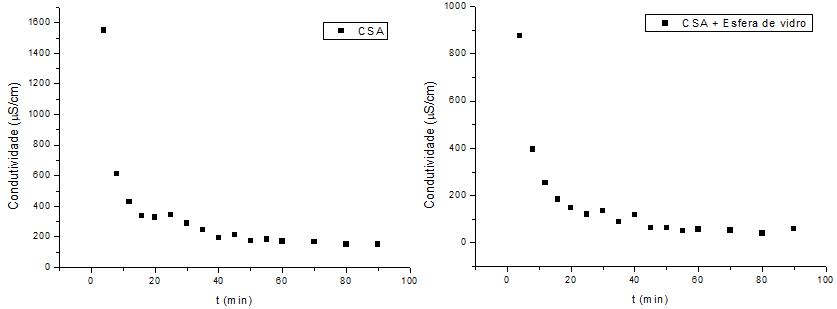
Fonte: Próprio autor (2018).
O primeiro gráfico é referente ao leito completamente preenchido de carvão sem ativação (CSA), já a segunda imagem caracteriza o perfil obtido através de uma coluna preenchida com carvão não ativado e esferas de vidro em proporção de 1:1. A partir desses gráficos é possível observar que os dois sistemas apresentam comportamentos similares, sendo que na faixa com maior concentração de carvão, o sistema se inicia com uma elevada condutividade, que, ao longo do tempo, tende a reduzir e parece começar a se estabilizar próximo ao tempo final de contato. Percebe-se que uma alta carga de eletrólitos é rapidamente eliminada do carvão, assim como uma pequena carga de eletrólitos presentes no carvão tende a demandar mais tempo para deixar o sistema, mesmo após uma hora e meia de contato. Tendo em vista que a faixa de uso para o SDS deve ser baixa, pode ser considerado o uso de diferentes vazões visando a remoção dessas impurezas, avaliando também a existência de caminhos preferenciais no sistema, a fim de melhorar sua eficiência.
Além disso, analisou-se uma metodologia complementar, baseada em um carvão que foi purificado com água destilada em um processo de batelada e, em seguida, submetido a uma lavagem para posterior avaliação da remoção de impurezas residuais, através de um sistema misto composto por 2/3 de carvão sem ativação e 1/3 de esferas de vidro, cujos resultados são caracterizados pela Figura 16.
Figura 16 – Análise da capacidade de limpeza para carvão pré-lavado
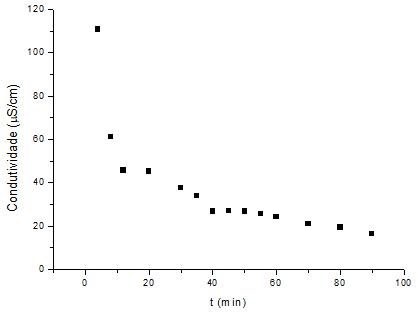
Fonte: Próprio autor (2018).
É possível verificar que a concentração de impurezas reduz rapidamente e apresenta decaimento contínuo até o tempo final de contato, sendo esta faixa mais próxima de 0. Esse comportamento encontra-se dentro do esperado para um carvão cuja finalidade é o tratamento de efluentes de tensoativos, tendo em vista o caráter das análises a serem realizadas. Além disso, objetivando diminuir o tempo de contato para que a operação se torne mais econômica, é possível observar, ao analisar os três gráficos obtidos, que a condutividade se torna mais estável a partir dos 40 minutos de execução dos ensaios, o que pode fazer com que o tempo de operação seja menor, não sendo necessário alcançar os 90 minutos pré-estabelecidos.
6.7. Perfil de saturação do leito para diferentes recheios
Em um sistema de leito fixo, além das características de avaliação do perfil da vazão, o comportamento do recheio é determinante para a efetividade do processo de adsorção do efluente de interesse, pois esse fenômeno é afetado diretamente pelos sítios ativos presentes no adsorvente. Desse modo, foi analisado o perfil de saturação através do pH da solução (Figura 17), como forma de determinar o modelo da curva de ruptura. Inicialmente, com a adsorção das moléculas no adsorvente e eventual arraste de eletrólitos dos sítios ativos, a solução assume um perfil inicial em função do adsorvente e, à medida em que o leito sofre saturação, o comportamento do perfil do pH tende a relacionar-se ao pH da amostra de tensoativo, no caso SDS, até atingir um patamar de estabilidade por meio do pH inicial do efluente analisado.
Figura 17 – Análise do pH para coluna com diferentes recheios
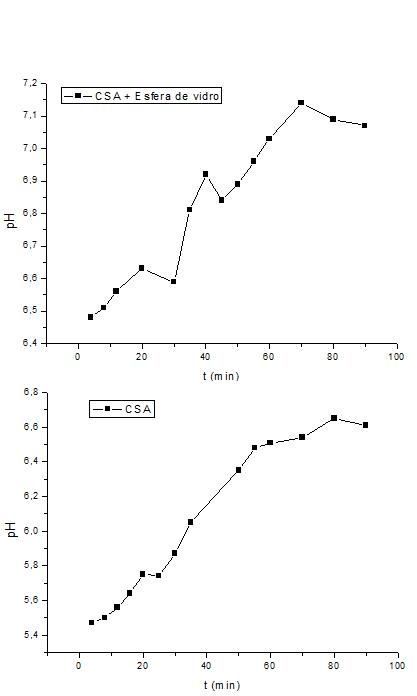
Fonte: Próprio autor (2018).
A análise do carvão sem ativação foi realizada a partir de uma coluna completamente recheada apenas com carvão, enquanto que para o recheio misto de esferas de vidro e CSA foi dividido em função da altura de ambas, sendo a metade inferior da coluna destinada ao carvão e a metade superior para as esferas de vidro. Os resultados obtidos demonstram que, a partir do ponto "zero", sendo este o primeiro minuto de coleta da solução, tem-se que ambas as situações apresentam um perfil de crescimento do pH, tendendo a saturação ao final do tempo de contato. É possível observar alguns pontos de dispersão, mas que naturalmente se ajustam a fim de construir um comportamento característico da curva de pH. Além disso, haja vista que a solução de tensoativo possui pH em torno de 7,4, conforme mensurado anteriormente, faz-se necessário um maior tempo de contato para consolidar a curva de saturação.
Verifica-se também que o ponto inicial de cada curva difere na escala de pH, o que pode ser explicado devido à maior presença de carvão, que através de suas características químicas é constatado que apresenta em sua composição compostos mais ácidos, conferindo a solução um pH inicialmente mais baixo. As esferas de vidro também possuem menor poder de adsorção, por conta da transferência de massa se dar principalmente através de adsorção física, fenômeno dotado de menor intensidade, o que pode fazer com que a solução seja menos adsorvida ao longo da coluna. Ou seja, observa-se que a coluna que possui maior altura de carvão tem seu processo de adsorção favorecido.
6.8. Determinação da curva de calibração do sistema
A construção da curva de calibração faz-se necessária a fim de estudar as características da adsorção do tensoativo aniônico perante o adsorvente empregado, bem como auxiliar na determinação das concentrações finais das soluções empregadas nos experimentos. Por meio da análise condutivimétrica, foi possível construir o gráfico dos valores de condutividade obtidos vs. concentrações (Figura 18), através do software Origin 8.
Figura 18 - Curva de calibração do sistema
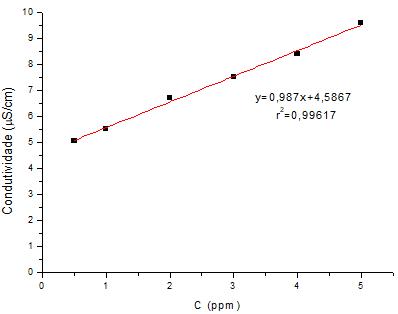
Fonte: Próprio autor (2018).
A Equação 5 representa a equação de ajuste dos dados e foi utilizada para definição das concentrações finais das amostras coletadas durante a realização dos experimentos, onde y representa os valores de condutividade e x, as concentrações.
(5)
Conforme citado em Vicente et al. (2004), para baixas concentrações de SDS é possível obter um perfil linear de coeficiente de regressão satisfatório, com valores superiores a 0,99, o que indica que o ajuste possui alta qualidade. Sendo assim, foram utilizadas soluções de surfactante com baixas concentrações, a fim de gerar um perfil com boa faixa de linearidade.
6.9. Análise da cinética de equilíbrio em função das concentrações de contaminante
A eficiência da remoção do tensoativo foi avaliada a partir da análise das concentrações por meio de medições da condutividade. Esse parâmetro foi obtido através dos valores de condutividade que, posteriormente, puderam ser convertidos para concentração molar, através da curva de calibração do sistema. Durante os ensaios de adsorção que se dá no tempo de contato pré-determinado, observa-se que o sistema tende a uma queda na condutividade, o que demonstra a adsorção das moléculas de tensoativos aniônicos presentes nas amostras.
A avaliação da quantidade de surfactante adsorvida pelo carvão não-ativado é estudada através da concentração de adsorvente contabilizada no tempo final do experimento, bem como na fase de equilíbrio, e foi calculada a partir da Equação (6), apresentada em Gomes, Nascimento & Silva (2016), onde qe é o potencial de remoção (mmol de adsorvato/g de adsorvente); Co e Cf são as concentrações de soluto no tempo inicial e final do processo, respectivamente (mmol/L); m é a massa de adsorvente que corresponde a 0,4 g e V é o volume de solução utilizado nos ensaios de adsorção, sendo de 0,1 L. No momento em que o equilíbrio de adsorção é alcançado, tem-se a concentração final do soluto na solução Cf e a capacidade de remoção do adsorvente qe. A Tabela 9 expressa os valores encontrados para esses parâmetros.
(6)
Tabela 9: Dados obtidos para os parâmetros de adsorção
|
Amostras |
Condutividade (S/cm) |
Cf (mmol/L) |
Co - Cf (mmol/L) |
qe (mmol/g) |
|
1 |
5,050 |
0,469402 |
0,030598 |
0,007649 |
|
2 |
5,467 |
0,891895 |
0,108105 |
0,027026 |
|
3 |
6,285 |
1,720669 |
0,279331 |
0,069833 |
|
4 |
7,036 |
2,481560 |
0,518440 |
0,129610 |
|
5 |
7,792 |
3,247518 |
0,752482 |
0,188121 |
|
6 |
8,501 |
3,965856 |
1,034144 |
0,258536 |
Fonte: Próprio autor (2018).
A partir dos valores obtidos pela Equação (6) e expressos na Tabela 9, foi possível plotar o gráfico da isoterma de adsorção experimental, expresso pela Figura 19.
Figura 19 - Avaliação do potencial de remoção em função da concentração
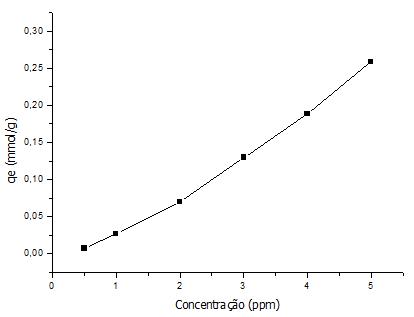
Fonte: Próprio autor (2018).
Através dos dados obtidos para as diferentes concentrações empregadas na análise, constata-se que o gráfico ilustrado pela Figura 19 apresenta um perfil de comportamento crescente, comprovando que o aumento das concentrações não alterou o perfil de adsorção, o que torna possível a utilização de concentrações mais elevadas, tendo em vista que será mantida a capacidade de remoção do tensoativo pelo adsorvente.
O aumento da concentração resulta em um aumento na eficiência da adsorção, isso porque com o aumento da concentração, mais espécies livres estarão distribuídas na superfície do adsorvente para serem adsorvidas. Já em baixas concentrações existe uma grande quantidade de sítios disponíveis para a adsorção e poucas espécies livres de surfactante (GOMES, NASCIMENTO & SILVA, 2016).
Além disso, a partir dos resultados obtidos, foi possível analisar o potencial de remoção em bases percentuais, a fim de avaliar a adsorção do sistema através da concentração de adsorvato que foi removida. A fórmula empregada é apresentada por Gomes, Nascimento & Silva (2016) e caracteriza-se pela Equação (7), a seguir.
(7)
Através da capacidade de remoção do tensoativo contaminante na solução, comparou-se esse desempenho em relação às diferentes concentrações empregadas, a fim de verificar o comportamento do sistema diante de uma maior disponibilidade de adsorvato no meio proporcionada pela quantidade de sítios ativos presentes nas amostras. A partir desses resultados, foi possível plotar o gráfico a seguir (Figura 20), que ilustra o perfil do potencial de remoção (%) vs. concentrações.
Figura 20 - Percentual das capacidades adsortivas das diferentes concentrações do surfactante
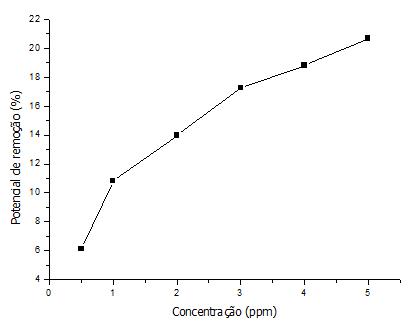
Fonte: Próprio autor (2018).
De posse do gráfico acima, verificou-se que as maiores concentrações empregadas no estudo apresentaram melhor capacidade de remoção, com valores próximos a 20% de retirada do meio aquoso, o que indica que o adsorvente empregado pode ser utilizado a fim de remover os surfactantes. Tendo em vista que as concentrações encontram-se abaixo da concentração micelar crítica, avaliada em 8,1 mmol/L (MORAES & REZENDE, 2004), o tensoativo existe na forma de monômeros, o que possibilita melhores potenciais de adsorção e remoção à medida em que a concentração aumenta.
É importante ressaltar que o carvão não sofreu ativação, o que sinaliza que esse material ainda pode melhorar a sua capacidade adsortiva, à medida em que sofrer mudanças em sua estrutura para acomodar macromoléculas, como os surfactantes. Além disso, a presença de grupamentos funcionais de caráter negativo nos sítios ativos pode dificultar a adsorção em baixas concentrações devido a repulsão entre as cargas, porém para que essa hipótese seja confirmada, faz-se necessário uma caracterização mais detalhada acerca do carvão de caroço de açaí.
7. CONCLUSÃO
A contaminação das águas vem sendo cada vez mais debatida na comunidade científica, tendo em vista que é um dos grandes problemas ambientais que assolam a sociedade moderna. A fim de minimizar a poluição presente nas águas superficiais, novas técnicas estão sendo desenvolvidas. Nesse cenário, a adsorção surge como uma boa alternativa para a descontaminação dos efluentes, devido ao seu baixo custo, alta eficiência e facilidade de execução. Observa-se também que a utilização do carvão produzido a partir do caroço de açaí como adsorvente caracteriza-se como uma alternativa econômica frente aos adsorventes comerciais, além de ser um material renovável e de fácil obtenção, pois existe em abundância nas regiões Norte e Nordeste do Brasil. A relevância da pesquisa se dá ao promover um destino sustentável aos resíduos gerados a partir do processamento da polpa do açaí, bem como auxiliar na descontaminação das águas, um recurso essencial para a manutenção da vida humana. A partir das análises realizadas ao longo do presente estudo, observa-se que os resultados obtidos são satisfatórios perante o objetivo proposto, tendo em vista que o carvão de caroço de açaí apresentou um percentual de remoção de surfactantes de até 20%, o que enfatiza a possibilidade desse material ser utilizado como adsorvente em leito fixo empacotado, visando o tratamento de efluentes. Além disso, em um estudo realizado por Oliveira (2003), no qual foi utilizado um leito recheado com bagaço de cana de acúçar objetivando a adsorção do corante remazol black B em soluções com concentrações iniciais variando de 5 a 50 mg/l, o leito apresentou um potencial de remoção de até 0,7 mg/g. Já nos ensaios realizados por Gomes, Nascimento & Silva (2016), em que o recheio da coluna consistia em farinha do mesocarpo do babaçu in natura e a solução utilizada foi de dodecil benzeno sulfato de sódio (SDBS) com concentrações de 0,5 a 3,5 mmol/l, o leito fixo apresentou um potencial de remoção de até 5,5 mmol/g. Ao comparar os resultados obtidos a partir dos ensaios realizados com outros encontrados na literatura, é possível inferir que o carvão de caroço de açaí apresenta um bom potencial de adsorção, porém sua capacidade adsortiva poderia ser ainda mais eficiente, tendo em vista que alguns processos químicos podem melhorar a sua performance, como o processo de ativação.
8. REFERÊNCIAS
ANJANEYULU, Y.; CHARY, N. S.; RAJ, D. S. S. D. Decolourization of industrial effluents – available methods and emerging technologies – A review. Environmental Science and Bio/Technology, v. 4, p. 245–273, 2005.
ARAÚJO, K. C. F. Estudo de diferentes mecanismos para produção de persulfato utilizando ânodo de diamante dopado com boro. 2016. 70 f. Dissertação (Mestrado em Química) – Programa de Pós-Graduação em Química, Universidade Federal do Rio Grande do Norte, Natal, 2016.
BARBOSA, C. S. Adsorção de compostos fenólicos em carvão ativado preparado a partir do aguapé (Eichhornia crassipes). 2013. 64 f. Dissertação (Mestrado em Química Analítica) – Programa de Pós-Graduação em Química, Universidade Federal do Maranhão, São Luís, 2013.
BARROS, T. V. Estudo do potencial de adsorção de azul de metileno em escamas de peixe Cynoscion acoupa (pescada amarela) em sistemas batelada e contínuo. 2017. 61 f. Trabalho de Conclusão de Curso (Graduação em Engenharia Química) - Centro de Ciências Exatas e Tecnologia, Universidade Federal do Maranhão, São Luís, 2018.
BEZERRA, J. M. M. Síntese de tensoativo para extração de metal pesado. 2012. 63 f. Trabalho de Conclusão de Curso (Graduação em Engenharia Química) – Centro de Engenharias, Universidade Federal Rural do Semi-Árido, Mossoró, 2012.
CAMARA, A. S. Adsorção de cromo (VI) em leito fixo utilizando partículas de areia recobertas com quitosana. 2014. Dissertação (Mestrado em Química) - Programa de Pós-Graduação em Química Tecnológica e Ambiental, Universidade Federal do Rio Grande, Rio Grande, 2014.
CANTRELL, K. B. Impact of pyrolisys temperature and manure source on physicochemical characteristics of biochar. Bioresource Technology, v. 107, p. 419-428, 2012.
CASTRO, D. A. R.; GUERREIRO, L. H. H.; SANTOS, M. C.; RIBEIRO, H. J. S.; SANTOS, W. G.; MACHADO, N. T. Produção de biocarvão a partir de sementes de açaí (Euterpe oleracea) via pirólise em escala de laboratório. In: 9 CONGRESSO BRASILEIRO DE P&D EM PETRÓLEO E GÁS, 2017, Maceió. Anais eletrônicos. Belém: Programa de Pós-Graduação em Engenharia de Recursos Naturais da Amazônia – Universidade Federal do Pará, 2017. Disponível em <https://www.researchgate.net/publication/320505143_PRODUCAO_DE_BIOCARVAO_A_PARTIR_DE_SEMENTES_DE_ACAI_EUTERPE_OLERACEA_VIA_PIROLISE_EM_ESCALA_DE_LABORATORIO> Acesso em 19 de junho de 2018.
CORDEIRO, T. R.; PAULA, C. C. A.; SOUSA, D. R.; AMORIM, M. S. Aproveitamento do caroço de açaí como fonte de energia térmica para as olarias do município de Bragança-Pará. In: VIII CONGRESSO BRASILEIRO DE GESTÃO AMBIENTAL, 2017, Campo Grande. Anais eletrônicos. Bragança: Instituto Federal de Educação, Ciência e Tecnologia do Pará, 2017. Disponível em <http://www.ibeas.org.br/congresso/Trabalhos2017/XI-050.pdf> Acesso em 19 de junho de 2018.
COSTA, L. S. Utilização do caroço de açaí como leito filtrante no tratamento de água de abastecimento e residuária. 2014. Dissertação (Mestrado em Engenharia Civil) – Programa de Pós-Graduação em Engenharia Civil, Universidade Federal do Pará, Belém, 2014.
CRISPIM, S. C. L. Remoção de cálcio (II) em solução aquosa por meio de carvões ativados submetidos a tratamentos superficiais. 2009. Tese (Doutorado em Química Analítica) – Programa de Pós-Graduação em Química, Universidade Federal da Paraíba, João Pessoa, 2009.
DIAS, Y. R.; RODRIGUES, R.; MUNIZ, A. R. C. Estudo da adsorção em leito fixo de cinzas volantes na remoção de compostos de enxofre do gás obtido na gaseificação do carvão mineral de Candiota-RS. In: V CONGRESSO BRASILEIRO DE CARVÃO MINERAL, 2017, Criciúma. Anais eletrônicos. Bagé: Universidade Federal do Pampa, 2017. Disponível em <http://www.swge.inf.br/ANAIS/CBCM2017/PDF/CBCM2017-0151.PDF> Acesso em 19 de junho de 2018.
EICHHORN, P.; RODRIGUES, S. V.; BAUMANN, W.; KNEPPER, T. P. Incomplete degradation of linear alkylbenzene sulfonate surfactants in Brazilian surface waters and pursuit of their polar metabolites in drinking waters. The Science of The Total Environment, v. 284, p. 123-134, 2002.
FONTAN, R. C. I.; BONOMO, R. C. F.; COIMBRA, J. S. R. Adsorção e troca iônica. Operações Unitárias na Indústria de Alimentos. 1 ed. Rio de Janeiro: LTC, v. 2, p. 453-482, 2016.
FU, Y.; VIRARAGHEVAN, T. Fungal decolorization of dye wastewater: A review. Bioresource Technology, v. 79, p. 251-262, 2001.
GANTUSS, C. A. R. Caracterização física e química de locais de ocorrência do açaizeiro (Euterpe oleracea, Mart) no Estado do Amapá e sua relação com o rendimento e qualidade do fruto. 2006. Dissertação (Mestrado em Agronomia) – Programa de Pós-Graduação em Agronomia, Universidade Federal da Paraíba, Areia, 2006.
GOMES, M. S. S. O.; NASCIMENTO, J. R.; SILVA, M. G. O. Mesocarpo de babaçu (Orbinya sp) como adsorvente do dodecil benzeno sulfonato de sódio (SDBS). Holos, v. 7, p. 51-61, 2016.
GOMIDE, R. Operações unitárias: Operações de transferência de massa. 1 ed. São Paulo: Dag Gráfica e Editora Ltda., v. 4, p. 311-315, 1988.
HOLMBERG, B.; JONSSON, B.; KRONBERG, B.; LINDMAN, E. Surfactants and polymers in aqueous solutions. John Wiley and Son, 2 ed. Surrey: Ltd, 2003.
JUNQUEIRA, A. A.; BASSO, V. M.; SOUZA, N. D. Evolução da produção de açaí no período de 2004 a 2015. In: I SEMANA DE APERFEIÇOAMENTO EM ENGENHARIA FLORESTAL, 2017, Curitiba. Anais eletrônicos. Curitiba: Departamento de Engenharia Florestal, 2017. Disponível em <https://www.even3.com.br/anais/iseaflor/52062-evolucao-da-producao-de-acai-no-periodo-de-2004-a-2015> Acesso em 19 de junho de 2018.
KIMURA, L. M. Uma contribuição à pirólise de biomassa: Avaliação de alguns resíduos da agroindústria como fonte de energia alternativa. 2009. 87 f. Dissertação (Mestrado em Engenharia Química) – Programa de Pós-Graduação em Engenharia Química, Universidade Federal de Uberlândia, Uberlândia, 2009.
LORA, E. E. S. et al. Gaseificação e pirólise para a conversão da biomassa em eletricidade e biocombustíveis. Biocombustíveis, v. 1, p. 411-498, 2012.
LUZ, A. D. Aplicação de coluna de adsorção em leito fixo para a remoção de compostos BTX multicomponentes presentes em efluentes petroquímicos. 2012. Tese (Doutorado em Engenharia Química) – Programa de Pós-Graduação em Engenharia Química, Universidade Federal de Santa Catarina, Florianópolis, 2012.
MEIER, D.; FAIX, O. State of the art of applied fast pyrolysis of lignocellulosic materials—a review. Bioresource technology, v. 68, n. 1, p. 71-77, 1999.
MENDHAM, J.; DENNEY, R. C.; BARNES, J. D.; THOMAS, M. J. K. VOGEL - Análise Química Quantitativa. 6 ed. Rio de Janeiro: Livros Técnicos e Científicos, 2002.
MESQUITA, F. Fibra de açaí pode ser alternativa barata na produção de MDF. 2014. Disponível em <https://www.acritica.com/channels/governo/news/fibra-de-acai-pode-ser-alternativa-barata-na-producao-de-mdf>. Acesso em 16 de julho de 2018.
MORAES, S. L.; REZENDE, M. O. O. Determinação da concentração micelar crítica de ácidos húmicos por medidas de condutividade e espectroscopia. Química Nova, v. 27, n. 5, p. 701-705, 2004.
MOREIRA, R. Estudo da pirólise lenta da casca da castanha de caju. 2015. Dissertação (Mestrado em Ciências na Área de Tecnologia Nuclear – Materiais) – Instituto de Pesquisas Energéticas e Nucleares, Universidade de São Paulo, São Paulo, 2015.
NASCIMENTO, R. F.; LIMA, A. C. A.; VIDAL, C. B.; MELO, D. Q.; MELO, G. S. C. Adsorção: Aspectos Teóricos e Aplicações Ambientais. 1 ed. Fortaleza: Imprensa Universitária, 256 p, 2014.
NGUYEN, N. T. Adsorption of phosphorus from wastewater onto biochar: Batch and fixed-bed column studies. 2015. Trabalho de Conclusão de Curso (Graduação em Engenharia Ambiental) - Helsinki Metropolia University of Applied Sciences, Helsinki, 2015.
OLIVEIRA, C. C. N. Estudos de equilíbrio e modelagem cinética da adsorção de corante têxtil "remazol black B" sobre bagaço de cana in natura e carvão ativado. 2003. Dissertação (Mestrado em Engenharia Química) – Coordenação de Pós-Graduação em Engenharia Química, Universidade Federal de Pernambuco, Recife, 2003.
OTERO, M.; ROZADA, F; CALVO, L. F.; GARCIA, A. I; MORÁN, A. Kinetic and equilibrium modeling of the methylene blue removal from solution by adsorbent materials produced from sewage sludges. Biochemical Engineering Journal, v.15, p. 59–68, 2003.
PANNIRSELVAM, P. V. et al. Desenvolvimento de projeto para produção de fibra de coco com inovação de tecnologia limpa e geração de energia. Revista Analytica, n. 15, p. 56-61, 2005.
PARADELA, F. M. R. Estudo da pirolise de misturas de resíduos de plásticos, pneus e biomassa. 2012. 322 f. Tese (Doutorado em Engenharia Química e Bioquímica) - Faculdade de Ciências e Tecnologia, Universidade Nova de Lisboa, Lisboa, 2012.
PEREIRA, E.; RODRIGUES, V. Carvão do caroço de açaí (Euterpe oleracea) ativado quimicamente com hidróxido de sódio (NaOH) e sua eficiência no tratamento de água para o consumo. Relatório do Projeto de Pesquisa apresentado à Comissão Avaliadora do Prêmio Jovem Cientista, 2013.
PIRES, P. A. R. Síntese e propriedades de soluções de tensoativos catiônicos derivados de (3-Dimetilaminopropil) amidas de ácidos carboxílicos. 2002. Tese (Doutorado em Química) – Instituto de Química da Universidade de São Paulo, Universidade de São Paulo, 2002.
RANGEL, R. N. Modelagem, caracterização e simulação da pirólise do caroço de açaí. 2014. Trabalho de Conclusão de Curso (Graduação em Engenharia de Energia) – Faculdade do Gama, Universidade de Brasília, Brasília, 2014.
REIS, B. O.; SILVA, I. T.; SILVA, I. M. O.; ROCHA, B. R. P. Produção de briquetes energéticos a partir de caroços de açaí. In: 4 ENCONTRO DE ENERGIA NO MEIO RURAL, 2002, Campinas. Anais eletrônicos. Belém: Departamento de Engenharia Elétrica e da Computação, 2002. Disponível em <http://www.proceedings.scielo.br/scielo.php?pid=MSC0000000022002000200044&script=sci_arttext&tlng=pt> Acesso em 19 de junho de 2018.
RIBEIRO, T. J. B. S. Capacidade de adsorção do azul de metileno utilizando-se carvão de babaçu como bioadsorvente. 2016. Trabalho de Conclusão de Curso (Graduação em Engenharia Química) – Centro de Ciências Exatas e Tecnologia, Universidade Federal do Maranhão, São Luís, 2016.
SANTOS, D. N. Investigação do potencial adsorvente do biocarvão impregnado produzido a partir da pirólise lenta do caroço de açaí. 2017. Trabalho de Conclusão de Curso (Graduação em Engenharia Química) – Instituto de Tecnologia, Universidade Federal do Pará, Belém, 2017.
SHAHALAM, A. B.; BIOUSS, A.; AYOUB, G. M.; ACRA, A. Competitive adsorption phenomena of petrochemicals – Benzene, toluene, and xylene in hexane in fixed-beds of sands. Water, Air, & Soil Pollution, v. 95, p. 221-235, 1997.
SOUZA, C. C.; SUZUKI, K. N.; LATINI, R. M.; CANESIN, F.; BELLIDO, A. V. B. Adsorção de metais em biocarvão utilizando radiotraçadores para fins de remediação. In: XVI CONGRESSO BRASILEIRO DE GEOQUÍMICA, 2017, Búzios. Anais eletrônicos. Niterói: Programa de Geoquímica – Universidade Federal Fluminense, 2017. Disponível em <http://www.sbgq.org.br/anaisXVIcongresso/2017_05_15_09_32_40.pdf> Acesso em 19 de junho de 2018.
STRELKO, V.; MALIK, D. J. Characterization and metal sorptive properties of oxidized active carbon, J. Colloid Interface Sci., v. 250, n. 1, p. 213-220, 2002.
TSANG, D. C. W.; HU, J.; LIU, M. Y.; ZHANG, W.; LAI, K. C. K.; LO, I. M. C. Activated carbon produced from waste wood pallets: Adsorption of three classes of dye. Water, Air, & Soil Pollution, v. 184, n. 1-4, p. 141-155, 2007.
VASQUES, A. R. Caracterização e aplicação de adsorvente para remoção de corantes de efluentes têxteis em batelada e colunas de leito fixo. 2008. 153 f. Dissertação (Mestrado em Engenharia Química) – Curso de Engenharia Química, Programa de Pós-Graduação em Engenharia Química, Universidade Federal de Santa Catarina, Florianópolis, 2008.
VICENTE, J. Determinação de surfactantes aniônicos em efluentes de postos revendedores de combustíveis da região da Grande Florianópolis. 2004. Trabalho de Conclusão de Curso (Graduação em Química) – Departamento de Química, Universidade Federal de Santa Catarina, Florianópolis, 2004.
VON SPERLING, M. Associação entre a legislação brasileira de qualidade da água (Resolução CONAMA n. 20/86 de 18 de Junho de 1986) e a seleção de processos de tratamento de esgotos. Revista de Engenharia Sanitária e Ambiental, v. 3, n. 1 - n. 2, p. 67-73, 1998.