Fármaco de Vigilância Hospitalar
SUMARIO
| 1-CAPA | 1 |
| 2-CONTRA CAPA | 2 |
| 3-SUMÁRIO | 3 |
| 4-INTRODUÇÃO | 4 |
| 5-MATERIAIS E MÉTODO | |
| 4.1-Notificação espontânea | 6 |
| 4.2-Investigação intensiva | 7 |
| 6-REFERENCIAL TEORICO | 8-14 |
| 7-RESUMO | 15 |
| 8-BIBLIOGRAFIA | 16 |
| 9-ANEXO 1 | 17 |
INTRODUÇÃO
O problema relacionado às reações adversas ocasionados por medicamentos é um assunto delicado e já abordado a muito tempo por filósofos e estudiosos da área de saúde. Há indícios que em 2000 AC os babilônicos já se preocupavam com as reações indesejáveis ocasionadas por tratamentos farmacológicos, eles afirmavam que o papel do médico era auxiliar os enfermos a restaurar o seu bem físico e mental, mas quando uma pessoa morria por erro médico devido ao tratamento, estes eram punidos tendo sua mão decapitada. Pouco depois no ano de 500 AC Hipócrates citou uma frase muito conhecida na área da saúde, “primum non nocere” que quer dizer, primeiro não prejudicar.
Hoje com o avanço da tecnologia e a descoberta de drogas cada vez mais potentes, criamos a necessidade de realizarmos uma monitoração mais efetiva do uso de medicamentos. Este estudo é praticamente impossível de se realizar devido ao grande numero de pessoas que fazem a automedicação e que realizam tratamentos em casa não retornando ao consultório medico e sendo o método de notificação espontânea ser menos preciso pois e impossível padronizá-lo sendo mais eficaz para desvios de qualidades. Um meio que é utilizado a farmacovigilância hospitalar, que realiza a monitoração dos efeitos adversos dos medicamentos utilizados em pacientes internados em hospitais de forma intensiva.
Este presente trabalho tem como objetivo, mostrar a importância dos estudos de farmacovigilância bem como sua eficácia e os métodos utilizados. Isso será feito através da revisão de literatura de monografias, artigos, resenhas, com isso seus dados e números serão avaliados caracterizando por uma pesquisa cientifica exploratória.
O Boston Collaborative Drug Surveillance Program (BCDSP) foi criada em 1966. No começo dos estudos pós-comercialização de drogas realizado por pesquisadores de segurança da BCDSP ainda eram principalmente feitos em papel. Enfermeira foram treinados para recolher informações de formas padronizadas. Foram entrevistados pacientes internados recolhendo informações sobre a exposição de drogas, problemas médicos e suas características descritivas. As informações recolhidas foram então analisadas, validadas e colocadas no computador. Embora esta abordagem foi de trabalho intensivo, o BCDSP foi pela primeira vez capaz de usar essas informações para realizar investigação epidemiológica formal em grande escala e quantificar os potenciais efeitos adversos de medicamentos, utilizando este método de acompanhamento hospitalar.
No site da ANVISA paciente e profissionais de saúde podem fazer a notificação em formulário imprenso ou preenchendo o formulário na web. Este formulário esta disponibilizado no anexo1.
MATERIAIS E MÉTODOS
O presente trabalho tem como objetivo possibilitar a compreensão, a importância e o uso da farmacovigilância dentro dos hospitais brasileiros através de revisão de literatura de artigos científicos, revistas e outros documentos que venham a ser pertinentes e confiáveis ao estudo. Inicialmente será realizada uma busca ampliada de materiais que podem vir a serem utilizados na obtenção de informações para o início da obtenção dos resultados esperados citados anteriormente. Esta busca acontecera por meio de pesquisas realizadas através de palavras chaves relacionadas ao assunto, tais como farmacovigilância hospitalar, reações adversas e erros de prescrição.
Com o material obtido nas pesquisas literárias em mãos, será realizada a leitura e consequente entendimento do mesmo, com finalidade de se compactar as informações tornando-as mais específicas e fidedignas possíveis. Em seguida será realizada uma segunda leitura mais detalhada e com marcações de partes importantes, para com essas possamos iniciar a dissertação do tema a ser abordado. Os efeitos adversos são muito difíceis de ser identificados é causam problemas em 10% dos pacientes que utilizam medicamento sendo que 1% veem a falecer.
Após estas etapas também será realizada a pesquisa de fotos, tabelas e gráficos de pesquisas já realizadas, para que possamos qualificar e quantificar as informações previamente obtidas, assim proporcionando a maximização do entendimento e compreensão das informações e dos temas abordados no trabalho.
Métodos de farmacovigilância sistema de notificação voluntaria de reações adversas provocadas por medicamento. Este sistema pôde ser definido como aquele que o profissional de saude tem liberdade para comunicar a ocorrência de um acontecimento que pode ser na sua opnião, devido a um efeito adverso provado por medicamento. E de acordo com Inman e Weber(1986),deve ter os seguintes objetivos.
-Identificar a causalidade
-Estabelecer a incidência.
-Informar profissionais que prescrevem e pacientes.
-Identificar problemas de segurança dos medicamentos.
Métodos de farmacovigilância vigilância intensiva caracteriza por ser um método de investigação ativa com obtenção de informações clinicas com a utilização de Hemogramas, Ultrassonografia, ressonância magnética.
Do ponto de vista hospitalar destaca-se dois sistemas de vigilância intensiva: o”Boston Collaborative Drug Surveillance program(BCDSP)” Outro avanço importante foi a recolha de informação ao paciente mais abrangente de base populacional a partir de um "gate-keeper" verdadeiro sistema de saúde. As características do sistema de saúde do Reino Unido estão realmente muito próximos de um tal sistema ideal, onde todas as informações do paciente é coletado pelo médico generalista, tornando o Reino Unido o cenário ideal para conduzir a investigação epidemiológica. No final da década de 1980 computadores em escritórios médicos estavam se tornando disponíveis e uma organização chamada VAMP Saúde software projetado para os cargos de médico clínico geral. Estas circunstâncias começou a mudar o registro médico de um sistema baseado em papel para um sistema baseado em computador e, assim, abriu a porta para a criação do banco de dados mais valiosos para a pesquisa farmacoepidemiológica que existe hoje. Os médicos generalistas foram treinados para usar este software e decidiu permitir que os seus prontuários anônimos a ser utilizado para fins de investigação por farmacêutico e médicos. A base de dados resultante, a General Practice Research Database (GPRD), é atualmente utilizado pelo Medicamento e Produtos de Saúde do Reino Unido Agência Reguladora (MHRA). O BCDSP utiliza um subconjunto especial desta base de dados para fins de investigação que sofreu processos de validação extensa e contínua.As informações anônimas do GPRD sobre diagnósticos, prescrição de medicamentos, visitas ambulatoriais e internações hospitalares estão disponíveis para os pesquisadores do BCDSP. Validação dos diagnósticos, relatórios de testes de laboratório e notas anônimas dos internamentos e referências estão disponíveis mediante solicitação. O GPRD tem mais de quatro milhões de indivíduos e mais de 25 milhões de pessoas / ano de dados. Hoje, o BCDSP tem trabalhado com o GPRD há 15 anos e já publicou mais de 150 estudos utilizando o recurso GPRD.
REFERENCIAL TEORICO
A farmacovigilância tem como conceito e principal e objetivo identificar reações adversas previamente desconhecidas, identificar seus riscos, tomar medidas reguladoras a respeito e informar aos profissionais de saúde e ao público sobre essas questões. Segundo Arrais (2002) as reações adversas a medicamentos tem contribuído em grande numero para os gastos na saúde pública, além de causar danos como morbidade e mortalidade. Partindo da hipótese que todo medicamento é utilizado para proporcionar o bem estar físico e mental de um indivíduo e que quando utilizado de forma errônea pode provocar danos, surgiu a necessidade de se monitorar os efeitos adversos ocasionados por medicamentos onde os efeitos indesejáveis foram identificados em estudo de fase quatro. Contudo exite diferentes métodos de identificação destas reações indesejadas e infrequentes .Entre a mais utilizada a notificação espontânea sendo realizadas pelo profissionais de saúde. Os farmacêuticos em suas praticas de atenção farmacêutica e médicos em seus consultórios. Os enfermeiros fazem parte deste estudo quando são realizados em hospitais. Método considerado mais eficaz com a identificação precoce destes efeitos em uma verificação intensiva e multiprofissional.
No século XVII, o antimônio foi considerado a primeira droga proscrita devido sua toxicidade em pacientes franceses, no entanto a proibição não durou muito tempo, por se atribuir a esta substância a cura da febre tifóide do rei Luis XIV. No início do século XIX, dois acontecimentos marcaram o desenvolvimento industrial farmacêutico e a regulamentação dos medicamentos: a lei de patentes e o isolamento da morfina pura a partir do ópio em 1805 (Arrais, 1998). No Brasil foi apenas na segunda metade do século XIX e inicio do século XX que surgiram as primeiras regulamentações para garantir a qualidade dos medicamentos e em 1961 que surgiu a preocupação efetiva a níveis mundiais das autoridades para se fiscalizar os efeitos adversos de medicamentos devido aos acontecimentos atribuídos a Talidomida. Na área hospitalar, o FDA começou, a partir de 1960, a coletar os registros de reações adversas e a patrocinar programas de monitoramento de fármacos.
Pinheiro et al. (2007) destaca que entre os principais métodos para se realizar a farmacovigilância e identificação de reações adversas é a busca ativa e notificação espontânea, esta busca ativa pode ser realizada por meio de pacientes ambulatoriais e internados, selecionados previamente através de critérios pré-definidos, como, pacientes de alto risco, com exames laboratoriais alterados, com tempo de internação prolongado e pacientes em uso de medicamentos para tratar as reações adversas. Para se realizar a coleta de dados pertinentes a alguma reação adversa que não conste na bula do medicamento, deve-se elaborar um questionário a ser preenchido por profissionais da saúde que contenha no mínimo informações como, nome do paciente, idade, nome da instituição coletora dos dados, nome do medicamento utilizado, dosagem, tempo de tratamento e descrição da reação adversa. No Brasil já existe e é fornecido pela Agencia nacional de vigilância sanitária (ANVISA), um questionário em que profissionais da área de saúde podem realizar esta notificação e encaminhá-las ao órgão. Felizmente o número de notificações de 1999 ate 2005 cresceu significativamente (Gráfico 1) o que demonstra a preocupação e interesse da população com este tema.
Gráfico 1
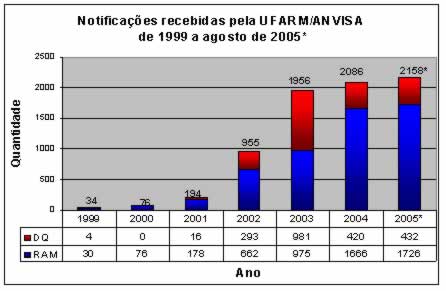
Evolução das notificações recebidas pela ANVISA de 1999 a 2005
Segundo Rozenfeld (1998) não há substância química totalmente segura ou totalmente tóxica. O dimensionamento do risco requer a compreensão dos mecanismos de produção dos efeitos tóxicos que embasam as classificações. Hoje a classificação de reações adversas a medicamentos mais utilizadas é a classificação de Rawlins e Thompson que as agrupa em dois tipos A e B. As reações do tipo A são denominadas por aquelas que têm ações farmacológicas normais porem aumentas, e se desencadeiam por fatores farmacocinéticos e farmacodinâmicos, já as reações adversas do tipo B são denominadas por aquelas que devido alguma diferença qualitativa do fármaco, paciente ou ambos.
A organização mundial de saúde (OMS) criou em meados dos anos 80 o programa internacional de monitorização de medicamentos, que hoje conta com aproximadamente 50 países (Tabela 1). Segundo Coelho (1998) participar desse programa significa, principalmente, contribuir para que reações adversas desconhecidas e de ocorrência rara a medicamentos novos ou antigos possam ser identificadas e prevenidas. O acúmulo de notificações espontâneas de suspeitas de reações adversas a medicamentos (RAM) e a sua análise sistemática, em nível local, nacional e internacional, geram hipóteses de causalidade que constituem sinais de alerta, divulgados através de boletim aos centros nacionais e disseminados entre profissionais de saúde de todo o mundo. Este programa alem de obtenção do sucesso no seu objetivo tem sido bastante discutido e aceito por estudiosos da área.

Apenas a participação neste programa não é o suficiente para garantir a um país a excelência em farmacovigilância, em primeiro lugar, é importante ressaltar o suporte técnico que um centro ou sistema nacional de farmacovigilância propicia à autoridade reguladora de medicamentos, facilitando o saneamento do mercado farmacêutico e a abordagem de problemas pontuais nessa área. De acordo com Coelho (1998), a sua estruturação gera a necessidade de que instituições e serviços, inclusive a indústria farmacêutica, supram o sistema com dados relativos à utilização de medicamentos (comercialização, distribuição, prescrição e uso), e a pacientes (variáveis sócio-econômicas , de morbidade, mortalidade), dados estes que constituem os denominadores farmacoepidemiológicos. Tais denominadores são necessários para a avaliação dos riscos relativos à exposição a medicamentos comercializados, procedimento que confere à farmacovigilância o caráter preventivo.
Em que pesem as dificuldades e limitações, as iniciativas na área de farmacovigilância no Brasil, nos últimos anos, vêm proliferando e adquirindo consistência (Arrais, 1996). Na área oficial, em maio de 1995, uma portaria da Secretaria de Vigilância Sanitária do Ministério da Saúde (MS/SVS) (Portaria n. 40 de 09/05/95) criou uma comissão cuja finalidade seria planejar a estruturação de um Sistema Nacional de Farmacoepidemiologia (Arrais, 1996). Infelizmente, o projeto preparado pela referida comissão não foi colocado em prática antes da substituição do secretário de vigilância sanitária que a criou. Na gestão seguinte, uma outra proposta foi elaborada por um grupo de técnicos a pedido do novo secretário (MS/SVS, 1997), mas, até maio de 1998, nada havia sido concretizado. Enquanto isso, em diferentes locais do País, profissionais de saúde vêm se iniciando na prática da monitorização de RAM, quase sempre mediante projetos de investigação desenvolvidos no contexto hospitalar, como podemos verificar consultando os livros de resumos dos últimos congressos da Sociedade Brasileira de Vigilância de Medicamentos (1996, 1997), da Sociedade Brasileira de Farmácia Hospitalar (1996, 1997) e do Primeiro Seminário Brasileiro de Farmacoepidemiologia (GPUIM, 1996). O interesse por essa área pode ser avaliado, também, pela grande afluência aos cursos de farmacovigilância realizados durante os referidos congressos, bem como pela participação de técnicos brasileiros em treinamentos promovidos pela OMS no exterior.
Um exemplo de farmacovigilância bem sucedida é no estado do São Paulo, que desde 1998 implantou o então chamado na época “Programa estadual de redução de latrogenias” e que mais tarde ganhou o nome popularmente conhecido como farmacovigilância. Para essa implantação foi necessário a sensibilização dos profissionais da saúde, afim de torná-los notificadores de reações adversas. Posteriormente foram ministrados cursos de capacitação destes profissionais para que cada um em seu respectivo hospital e ambiente de trabalho iniciasse a implantação da farmacovigilância. Podemos observar na gráfico a seguir os principais profissionais que vem realizando este trabalho no estado de São Paulo, que hoje é considerado exemplar.
Gráfico 1
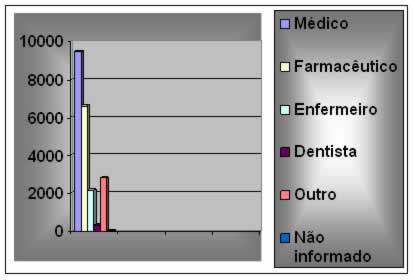
Principais notificadores de reações adversas a medicamentos no estado de São Paulo
Outro exemplo bem sucedido de farmacovigilância é a do estado do Ceará que teve resultados positivos apesar das dificuldades encontradas durante a implantação do sistema. Inicialmente foi firmada uma parceria com a universidade federal do Ceará (UFC) e a Secretaria de Estado da Saúde (SESA), tendo como órgão executor o grupo de prevenção ao uso indevido de medicamentos (GPUIM). A sua criação foi precedida pela capacitação de membros do grupo em farmacoepidemiologia, estruturação do centro de informação sobre medicamentos da UFC (CIM - UFC) e do Centro de Farmacovigilância do Ceará (CEFACE), setor do GPUIM dedicado à Farmacovigilância.
A implantação do sistema de farmacovigilância do Ceará (SIFACE) teve início através das unidades de farmácia hospitalar de quatro hospitais públicos de Fortaleza - Hospital de Messejana, Hospital Universitário Walter Cantídio, Maternidade Escola Assis Chateaubriand e Hospital Nossa Senhora da Conceição. Após contato com a direção dos mesmos e com as chefias das respectivas unidades de farmácia. Foram realizadas palestras in loco para os profissionais de saúde e apresentada a ficha de notificação, os farmacêuticos foram convidados a participar de oficinas sobre farmacovigilância e de dois cursos de curta duração promovidos pelo SIFACE sobre monitorização de pacientes hospitalizados e tópicos em epidemiologia clínica. Cada hospital passou a ser visitado semanalmente (uma ou mais vezes/semana) por membros do CEFACE, que, além de recolherem as notificações coletadas pelo farmacêutico hospitalar, percorrem as enfermarias na busca ativa de casos, entrevistando médicos e enfermeiras e/ou consultando os prontuários.
Farmacovigilância: elemento para a discussão e perspectivas
Pharmacoepidemiology: topics for siscussion and prospects
Abstract
The surveillance of medically includes Pharmacoepidemiology and the surveillance (sanitária) thats on brazil has power of police. The Pharmacoepidemiology evolved a lot on the post-war and kip evolving , in 1952 appears the first book about drug adverse events . Unit today it was proposed a lot forms of algorithm to make a questinnaire about spontancous cominication.
Anoder poit discuted was the many forms to clasification or the effects adverse. In brazil, the model used its oms (world dwide organization f health), that creals in mid of 80 the internatioal program of monitoration of medically, that today almost cout with 50 countries with the best acception on the algotithm. All of the given was coleted of cientific article.The intensive methods are more effective but are costly but with many finding love in 150 articles. The most clinically relevant findings BCDSP file, including the discovery of the protective effect of aspirin on cardiovascular events (Jick and Miettinen 1976, Jick and Elwood 1976), and since then the BCDSP had a pioneering role in developing and applying methods in epidemiology drugs. Until the mid-1970s it became clear that other more efficient methods would be available in the future as medical information began to be recorded directly to computer for health care providers. He soon realized that electronic data could be used to create large databases and increase the accuracy and efficiency of the investigation of drug safety. All data were collected from scientific articles.
Resumo
A vigilância de mediamentos inclui farmacoepidemiologia e a vigilância sanitária que no Brasil tem poder de policia. A farmacoepidemiologia evoluiu muito no pós-quera e continuo a evoluir onde em 1952 aparece o primeiro livro de reação adversa. Ate os dias atuais que foram propostos varias formas de algorítimos para se fazer um questionário de comunicação espontania. Também foram discutido as varias formas de classificação dos efeitos adversos. No Brasil o modelo utilizado foi proposto pela organização mundial de saúde (OMS), que criou em meados dos anos 80 o programa internacional de monitorização de medicamentos, que hoje conta com aproximadamente 50 países. Os métodos intensivos são mais eficientes mas são de elevado custo mas com varias descoberta em amais de 150 artigos. A descobertas mais clinicamente relevantes do arquivo BCDSP , incluindo a descoberta do efeito protetor da aspirina sobre os eventos cardiovasculares (Jick e Miettinen 1976, Jick e Elwood 1976), e desde então o BCDSP teve um papel pioneiro no desenvolvimento e aplicação de métodos em epidemiologia de drogas. Até meados dos anos 1970 tornou-se evidente que outros métodos mais eficientes estariam disponíveis no futuro, conforme informação médica começou a ser registrados diretamente no computador por prestadores de cuidados de saúde. Ele logo percebeu que esses dados eletrônico poderia ser usado para criar grandes bases de dados e aumentar a precisão ea eficiência da investigação de segurança de medicamentos. Todos os dados foram coletados de artigos científicos.
Palavras-chave: Farmacovigilância, Farmacoepidemiologia, Epidemiologia, Toxicologia, Notificação, Eventos adversos a Medicamentos.
Key Words: Pharmacovigilance; Pharmacoepidemiology; Epidemiology; Toxicology, Notification, Drug Adverse Events.
FICHAMENTO BIBLIOGRÁFICO
GATTI, Fabianade Menezes ; WILLIAN, Jorge Leandro Nascimento. Farmacologia Monitoramento de eventos adversos em ambiente hospitalar: Relato de farmacovigilância,2010,pg.1a7.
Boston Collaborative Drug Surveillance Program,site. http://bcdsp.net/history.html
NISHIOKA, Sergio de Andrade; DIAS, Murilo Freitas. Farmacovigilância no Brasil: A importância e os desafios de uma regulação para a indústria farmacêutica. Prática hospitalar, 2008, pg. 98 a 102.
Dr. Simerjot K. Jassal, VA San Diego Healthcare System, 3350 La Jolla Village Drive, Division of GIM/G, MC 111N, San Diego, CA 92161 (e-mail: sjassal@ucsd.edu).
BARBOZA, Patrícia Crizel, et al. Implantação do Serviço de Farmacovigilância: Hospital São Francisco de Paula. Revista de saúde da UCPEL vol. 1, 2007.
ARRAIS, Paulo Sérgio Dourado. O uso irracional de medicamentos e a farmacovigilância no Brasil. Caderno de Saúde Pública, 2002, vol.18, n.5, pg. 1478-1479.
COELHO, Helena Lutéscia; ARRAIS, Paulo Sergio Durado; GOMES, Adriana Parente. Sistema de farmacovigilância no Ceará: Um ano de experiência. Caderno de Saúde pública vol. 15, 1999.
COELHO, Helena Lutéscia. Farmacovigilância: um instrumento necessário. Caderno de saúde publica, 1998. Scielo Public Health.
ROZENFELD, Suely. Farmacovigilância: elemento para discussão e perspectivas. Caderno de saúde pública vol. 14, 1998.
Publicado por: bruno
O texto publicado foi encaminhado por um usuário do site por meio do canal colaborativo Monografias. Brasil Escola não se responsabiliza pelo conteúdo do artigo publicado, que é de total responsabilidade do autor . Para acessar os textos produzidos pelo site, acesse: https://www.brasilescola.com.