DIVERSIDADE E FITOSSOCIOLOGIA DAS PTERIDÓFITAS DA MATA DE GALERIA DO PARQUE MUNICIPAL MÁRIO VIANA, NOVA XAVANTINA-MT
índice
- 1. Resumo
- 2. Introdução
- 3. Objetivos
- 3.1 Geral
- 3.2 Específicos
- 4. Material e Métodos
- 4.1 Área de Estudo
- 4.2 Levantamento de Dados
- 4.3 Coleta, Identificação e Herborização do Material Botânico
- 4.4 Riqueza, Diversidade e Similaridade Florística
- 4.5 Análise Fitossociológica
- 5. Resultados e Discussão
- 6. Considerações Finais
- 7. Referências Bibliográficas
- 8. Anexos
- 8.1 Anexo 1:
O texto publicado foi encaminhado por um usuário do site por meio do canal colaborativo Monografias. Brasil Escola não se responsabiliza pelo conteúdo do artigo publicado, que é de total responsabilidade do autor . Para acessar os textos produzidos pelo site, acesse: https://www.brasilescola.com.
1. Resumo
Foi realizada uma análise fitossociológica das pteridófitas ocorrentes na mata de galeria do Parque Municipal Mário Viana em Nova Xavantina, Mato Grosso. Os estudos foram desenvolvidos ao longo de 400 parcelas de 25 m2, distribuídas entre dois trechos (um superior e outro inferior), compreendendo 1 ha da mata de galeria do córrego Bacaba (14°43’S e 52°21’W) em Nova Xavantina. Assim, no período de março a novembro de 2004, foram levantadas, em campo, informações sobre abundância, altura e área de cobertura dos indivíduos amostrados. Registrou-se a ocorrência de 11 espécies de pteridófitas, distribuídas em oito gêneros e seis famílias. Entretanto, a curva do coletor aponta a possível existência de mais seis espécies na área. O índice de diversidade de Shannon-Wienner foi H’= 1,26 nats/indivíduo e J= 0,53, sendo considerada baixa quando comparada a outras áreas, como em floresta de restinga no Estado do Rio Grande do Sul e mata de terra firme, ao norte do Pará. Quanto à similaridade florística, o índice de Sørensen aponta um valor de S= 0,43 e o de Jaccard C=0,27, sugerindo que os trechos são similares. Foram analisados 3.418 indivíduos, apresentando média de 8,55 indivíduos/25 m2. Adiantum serratodentatum apresentou os maiores valores relativos de densidade (46,31%) e freqüência (43,96%) na área, enquanto que Pityrogramma calomelanos foi a espécie dominante (37,18%). Assim, Adiantum serratodentatum e Pityrogramma calomelanos foram as espécies mais importantes, totalizando 60% do valor de importância para a área. Thelypteris serrata apresentou a maior média de altura (121 cm) e Polypodium polypodioides a menor (2,71 cm), enquanto que a altura média da comunidade foi 14,13 cm. Dos indivíduos analisados, 94,32% foram enquadrados na primeira classe de altura (0-30 cm) e 0,03% ocuparam a sexta e última classe (151-180 cm). Este estudo permitiu compreender alguns aspectos ecológicos importantes das pteridófitas da região, grupo ainda pouco estudado no Cerrado.
Palavras-chave: pteridófitas, similaridade florística, abundância, altura e Mato Grosso.
Abstract
Was accomplished a phytosociological analysis of the pteridophytes occurred in the gallery forest of the "Parque Municipal Mário Viana" in Nova Xavantina, Mato Grosso. The studies were developed along 400 plots of 25 m2, distributed among two stretches (a upper and other lower), totaling 1 ha of the Bacaba stream gallery forest (14°43’S and 52°21’W) in Nova Xavantina. Then, in the period of March to November 2004, were surveyed, in field, information about abundance, height and area of covering belonged to the sampled individuals. A total of 11 species of pteridophytes were found, distributed in eight genera and six families. However, the collector curve shows the possible existence of more six species in the area. The index of diversity of Shannon-Wienner was H' = 1,26 nats/individual e J= 0,53 considered low when compared to other areas, as in a restinga forest of the State of Rio Grande do Sul and a dry forest, in the north of Pará. About the floristic similarity, the index of Sørensen shows a value of S = 0,43 while Jaccard C=0,27, this suggesting that the stretch are similar. 3.418 individuals were analyzed, presenting at mean 8,55 individuals/25 m2. Adiantum serratodentatum showed the largest relative values of density (46,31%) and frequency (43,96%) in the area, while Pityrogramma calomelanos was the dominant species (37,18%). Adiantum serratodentatum and Pityrogramma calomelanos were the most important species, totaling 60% of the value of importance. Thelypteris serrata presented the largest mean height (121 cm) and Polypodium polypodioides the smallest (2,71 cm), while the community's mean height was 14,13 cm. Among the analyzed individuals, 94,32% were classified in the first height class (0-30 cm) and 0,03% occupied the sixth and last class (151-180 cm). This study it allowed to understand some important ecological aspects of the pteridophytes of the region, group still little studied in the Cerrado.
Key-words: pteridophytes, floristic similarity, abundance, height and Mato Grosso.
2. Introdução
O bioma Cerrado é quase totalmente tropical, com apenas sua borda sul situada em altitudes moderadas no sudoeste de São Paulo e altitudes maiores no sul de Minas Gerais (1000-1700 m). Ocorre no Brasil Central ao longo de um gradiente de formas fisionômicas abrangendo a parte sul de Mato Grosso, todo o Estado de Goiás, Tocantins, Mato Grosso do Sul, oeste da Bahia, oeste de Minas Gerais e o Distrito Federal. No entanto, se estende para fora do Brasil Central ao norte, oeste e ao sul e nordeste como áreas disjuntas (Eiten 1993).
São descritos onze tipos fitofisionômicos para o Cerrado que se enquadram em formações florestais, savânicas e campestres (Ribeiro & Walter 1998). De acordo com os referidos autores, dentre os tipos fitofisionômicos mencionados ocorrem as matas de galeria. Trata-se de uma formação florestal do bioma Cerrado, que acompanha rios de pequeno porte e córregos do Brasil Central, formando corredores (galerias) sobre o curso d’água. Caracteriza-se também, como uma fitofisionomia perenifólia, com estrato arbóreo que varia entre 20 e 30 metros e cobertura de 70% a 95%. Apresenta umidade relativa elevada em seu interior, mesmo em época seca do ano.
De um modo geral, a maior diversidade de espécies de pteridófitas concentra-se em duas grandes regiões, onde ocorrem aproximadamente 75% das 9000 espécies. Uma destas é a América, incluindo as Grandes Antilhas, México, América Central, Andes, Venezuela e Bolívia, com aproximadamente 2250 espécies (Tryon & Tryon 1982).
Windisch (1992) discute que cerca de 30% das espécies americanas de pteridófitas podem ser encontradas em território brasileiro, que abriga inclusive um dos centros de endemismo e especiação do continente. Os Estados brasileiros de Minas Gerais, sul do Espírito Santo e Rio Grande do Sul, contém aproximadamente 600 espécies de pteridófitas (Tryon & Tryon 1982).
Estudos de cunho florístico-taxonômico ainda são restritos para o Estado de Mato Grosso, destacando-se os trabalhos de Windisch (1975; 1985; 1994; 1995; 1996a; 1996b; 1997; 1998), Mendonça et al. (1998), Windisch & Nonato (1999), Souza (2001), Windisch & Tryon (2001), Athayde Filho & Windisch (2003), Souza (2003) e Athayde Filho & Agostinho (2005). Já estudos ecológicos para esta região, envolvendo pteridófitas, são ainda mais restritos.
Mendonça et al. (1998) apresentaram uma lista de caráter preliminar que aponta para o Cerrado a ocorrência de 267 espécies de pteridófitas, distribuídas em 51 gêneros e 19 famílias. Destas, cerca de 57,7% são encontradas em mata de galeria. Entretanto, Windisch (1996b) apresenta uma estimativa mais ampla para este número, apontando para 310 espécies.
Athayde Filho & Windisch (2003) analisando a pteridoflora do Parque Municipal Mário Viana listaram para a mata de galeria do Parque 19 espécies. Enquanto que Souza (2003), listou para a mesma mata de galeria a ocorrência de 12 espécies de pteridófitas distribuídas em 10 gêneros e oito famílias.
No Brasil, bem como no Cerrado, são bastante comuns estudos fitossociológicos envolvendo espécies arbóreas da flora fanerogâmica, podendo ser mencionados dentre muitos os trabalhos de Batista Neto (2002), Felfili et al. (2002), Marimon et al. (2002), Silva et al. (2002), Fonseca & Silva-Júnior (2004), Silva-Junior (2004) e Guarino & Walter (2005). No entanto, estudos sobre a ecologia de pteridófitas são ainda escassos, sendo a maioria realizados na Mata Atlântica e Amazônia. Neste contexto, destacam-se os pioneiros trabalhos de Schimitt (2001), Athayde Filho (2002) e Rodrigues et al. (2004).
Diante desses fatos, visando conhecer um pouco mais a ecologia da pteridoflora regional foi proposto o presente trabalho, no qual realizou-se uma análise florística e fitossociológica de pteridófitas da mata de galeria do Parque Municipal Mário Viana, em Nova Xavantina-MT.
3. Objetivos
3.1. Geral
Realizar um estudo da diversidade floristica e fitossociologia de pteridófitas na mata de galeria do Parque Municipal Mário Viana, em Nova Xavantina-MT.
3.2. Específicos
-
Avaliar a diversidade florística da pteridoflora local;
-
Verificar a similaridade florística de pteridófitas entre dois trechos da mata de galeria;
-
Analisar os parâmetros fitossociológicos da comunidade pteridofítica.
4. Material e Métodos
4.1. Área de Estudo
O município de Nova Xavantina pertence à mesorregião Nordeste Mato-grossense (Figura 1) (Ferreira 2001). O clima é do tipo Aw, conforme a classificação de Köppen, com cerca de seis a oito meses de chuvas. A precipitação anual de 1300 mm a 1500 mm, com intensidade máxima de dezembro a fevereiro. A temperatura média mensal é de 25°C (Marimon et al. 2003).
O município abrange áreas com fitofisionomias típicas do bioma Cerrado (Piaia 1999; Miranda & Amorin 2000) e nele situa-se o Parque Municipal Mário Viana (14°43’S e 52°21’W) (Figura 2). Este Parque é uma unidade de conservação que abrange 450 ha, a qual é restrita às atividades de ensino, pesquisa e educação conservacionista (Nova Xavantina 2002).
O Parque apresenta cinco classes de solo: Latossolos, Neossolos, Gleissolos, Plintossolos e Planossolos. Nele verifica-se a ocorrência das seguintes fisionomias do Cerrado: parque de cerrado, campo úmido, cerrado rupestre, cerrado típico, cerradão e floresta de galeria (Rossete & Ivanauskas 2000).
O presente estudo foi realizado em dois trechos distintos, denominados como trechos um e dois, situados respectivamente nas porções alta e baixa, nas adjacências do canal do córrego no interior da mata de galeria do referido Parque (Figura 3).
O primeiro trecho (Figura 4 a e b) apresenta declividade média de 42%, é marcado pela presença de afloramentos rochosos de quartzito e ocorrência de enchentes sazonais com drenagem rápida. Em áreas intermediárias ao leito do córrego e a borda da mata de galeria do mencionado trecho, o nível do lençol freático, no decorrer do ano, oscila entre -100 e -250 cm de profundidade, alcançando os menores valores entre janeiro e março, e os maiores entre agosto e setembro (Marimon et al. 2003). A flora fanerogâmica está representada por 74 espécies arbóreas. Dentre as mais importantes, destacam-se: Calophyllum brasiliense Cambess., Apuleia leiocarpa (Vog.) Marcbr. var molaris (Spruce ex Benth.) Koeppen e Hymenaea courbaril L. var. stilbocarpa (Hayne) Lee & Langenheim. que são emergentes, com algumas árvores que atingem 25 m (Marimon et al. 2002).
O segundo trecho analisado (Figura 5 a e b) apresenta declividade média de 5%. As rochas estão ausentes e a drenagem do solo é deficiente. Nas áreas intermediárias ao leito do córrego e a borda da mata, a profundidade do lençol freático, no transcorrer do ano, varia entre -50 e -120 cm, apresentando menor profundidade em relação ao trecho um, fato decorrente do relevo mais plano exibido pelo referido trecho (Marimon et al. 2003). A flora está representada por 77 espécies arbóreas, dentre elas apenas Mauritia flexuosa L. é emergente, alcançando 25 m, enquanto que alguns indivíduos de Physocalymma scaberrimum Pohl e Tapirira guianensis Aubl. alcançam 20 m (Marimon et al. 2002).
.jpg)
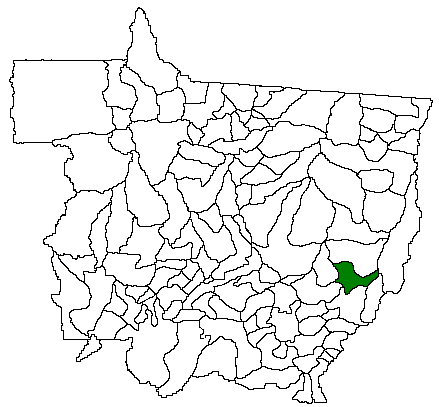
Figura 1: Localização do município de Nova Xavantina, Estado de Mato Grosso. Fonte: Athayde Filho & Windisch (2003).
.jpg)
Figura 2: Composição colorida da imagem de satélite apresentando a localização aproximada do Parque Municipal Mário Viana, delimitada pelo círculo amarelo. Escala: 1:50.000. Fonte: Miranda & Coutinho (2004).
.jpg)
Figura 3: Parque Municipal Mário Viana. Localização dos trechos estudados na extremidade inferior da figura (Córrego do Bacaba). Fonte: Adaptado de Rossete & Ivanauskas (2000).
A

B

Figura 4: Primeiro segmento analisado da mata de galeria do Parque Municipal Mário Viana, Nova Xavantina-MT. A: aspecto geral da borda da mata; B: aspecto geral do interior da mata.
A

B

Figura 5: Segundo segmento analisado da mata de galeria do Parque Municipal Mário Viana, Nova Xavantina-MT. A: aspecto geral da borda da mata; B: aspecto geral do interior da mata.
4.2. Levantamento de Dados
Foram realizadas visitas semanais à área de estudo no período de março a novembro de 2004. Para a amostragem da área foi adotada a metodologia descrita por Windisch (1992) e Athayde Filho (2002). Assim, com auxílio de uma trena, estacas de metal e barbantes, foram delimitadas sistematicamente 400 parcelas de 5 x 5 m (25 m2) (Figura 6), sendo 200 parcelas distribuídas em cada trecho, compondo uma área amostral de 1 ha (Figura 7). A partir de então, realizou-se a contagem e as mensurações de cada indivíduo presente ao longo das parcelas analisadas em cada trecho (Figura 8 a e b).
Para a contagem dos indivíduos pertencentes a espécies reptantes, utilizou-se a metodologia apresentada por Athayde Filho (2002) e Rodrigues et al. (2004). Cada colônia foi considerada um único indivíduo (Figura 8 b).
As informações da comunidade estudada foram coletadas com o auxílio de um gravador microcassete, visando à redução do período de trabalho em campo. Também foram feitas fotografias com o auxílio de uma máquina fotográfica digital para demonstrações e esclarecimentos dos estudos realizados.
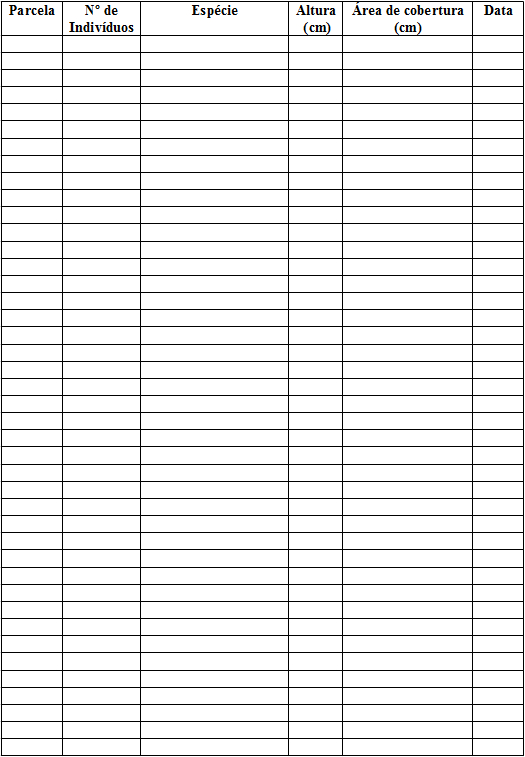
Posteriormente, as informações foram cuidadosamente transcritas para fichas auxiliares de estudos adaptadas de Durigan (2003) (Anexo 1).
4.3. Coleta, Identificação e Herborização do Material Botânico
Os espécimes foram coletados e herborizados de acordo com metodologia a proposta por Windisch (1992). Para a identificação das espécies, foi adotado o sistema de classificação proposto por Tryon & Tryon (1982).
Foram consultados também os trabalhos de Windisch (1992), Athayde Filho & Windisch (2003) e Souza (2003), além de bibliografias especializadas. Quando necessário, recorreu-se a consultas ao acervo do Herbário NX, da Coleção Zoobotânica James Alexander Ratter, da Universidade do Estado de Mato Grosso (Unemat), Campus Universitário de Nova Xavantina. Também foram consultados os especialistas Dr. Jefferson Prado (Instituto de Botânica-SP), para Pteridaceae, e MSc. Maria Angélica Rubeo-Kieling (Laboratório de Pteridologia, UNISINOS-RS), para Thelypteridaceae.
O material testemunho coletado foi tombado e incorporado ao acervo pteridofítico do referido Herbário (Tabela 1).
.jpg)
Figura 6: Detalhes da parcela de 25 m2 demarcada na mata de galeria do Parque Municipal Mário Viana, Nova Xavantina-MT.
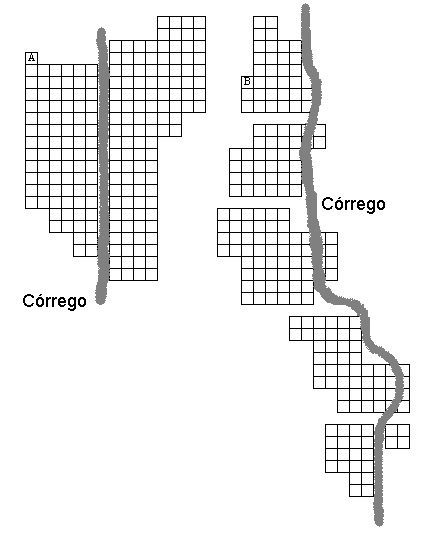
Figura 7: Representação das 400 parcelas (25 m2) demarcadas na mata de galeria do Parque Municipal Mário Viana, Nova Xavantina-MT. A: primeiro trecho (200 parcelas) e B: segundo trecho (200 parcelas).
A

B

Figura 8: Coleta dos dados referentes à altura e área de cobertura dos indivíduos analisados na mata de galeria do Parque Municipal Mário Viana, Nova Xavantina-MT. A: aspectos gerais de um indivíduo reptante, pertencente à espécie Adiantum serratodentatum, no qual está sendo medida a área de cobertura; B: detalhes da mensuração da altura de uma colônia de Pityrogramma calomelanos.
4.4. Riqueza, Diversidade e Similaridade Florística
Para as análises da riqueza, similaridade e diversidade florísticas das pteridófitas, foram utilizadas as informações referentes à presença das espécies, bem como da abundância de seus indivíduos registrados durante o levantamento.
A riqueza de pteridófitas das áreas avaliadas foi analisada de acordo com a presença ou não das espécies nas parcelas delimitadas. Espécies observadas fora da área amostral não foram consideradas.
O programa Microsoft Excel do Office 2002, foi utilizado para a confecção do gráfico da análise florística. Utilizou-se, ainda, o programa EstimateS 5 (Colwell 1997) para a confecção do gráfico das curvas do coletor e estimador de diversidade. Para as análises, adotou-se o estimador de diversidade ICE (Lee & Chao 1994), e a curva cumulativa de espécies de Coleman.
A diversidade florística da área estudada foi avaliada de acordo com o Índice de Diversidade de Shannon-Wienner (H’). O Índice de Equabilidade de Pielou (J’) também foi calculado, bem como a curva do componente dominância da diversidade (Odum 1988; Ricklefs 2001; Sambuichi 2002). Todos estes cálculos foram realizados a partir do programa Microsoft Excel do Office 2002.
Foi realizada também uma análise da similaridade florística entre os trechos um e dois, utilizando os Índices de similaridade de Sørensen (S) e o de Jaccard (C) (Durigan 2003; Fonseca & Silva-Júnior 2004). Os valores para o índice de similaridade variam de 0 a 1, sendo que, para Sørensen, valores acima de 0,5 indicam uma elevada similaridade, enquanto que para Jaccard, o mesmo vale para valores acima de 0,25 (Fonseca & Silva-Júnior 2004). Para os cálculos foi utilizado o programa Microsoft Excel do Office 2002.
4.5. Análise Fitossociológica
Para a análise fitossociológica, foram utilizados os dados de abundância, alturas e áreas de cobertura dos indivíduos de pteridófitas encontrados em cada parcela.
Os parâmetros fitossociológicos avaliados foram: Ni: número de indivíduos da espécie i ocorrente na área; Ui: número de unidades amostrais que a espécie i ocorreu; DRi: densidade relativa, expressa em porcentagem dos indivíduos da comunidade correspondente aos indivíduos da espécie i; FRi: frenquência relativa da espécie i (%); DoRi: dominância relativa da espécie i (%); VI: valor de importância da espécie i; Alt. Méd.: altura média; Alt. Máx.: altura máxima; Alt. Min.: altura mínima (Martins 1993; Durigan 2003). Os cálculos dos referidos parâmetros foram efetuados utilizando-se o programa Mata Nativa 1.0 (Souza et al. 2002).
Foi calculada a média de indivíduos por parcela (x), bem como o desvio padrão (s), o coeficiente de variação (CV) e a mediana (Pagano & Gauvreau 2004; Vieira 2004). Para as análises das alturas, foi calculado o número de classes, bem como intervalos das mesmas segundo Marimon (2005), visando minimizar o número de classes vazias. Assim, foram obtidas seis classes com intervalos de IC=30 cm. Para a realização destes cálculos foi utilizado o programa Microsoft Excel do Office 2002.
Para os cálculos referentes à dominância das espécies de pteridófitas analisadas foram utilizados os valores das áreas de cobertura das mesmas, de acordo com Athayde Filho (2002) e Rodrigues et al. (2004).
5. Resultados e Discussão
5.1. Riqueza e Diversidade Florística
Foram registradas, ao longo das parcelas analisadas, 11 espécies de pteridófitas distribuídas em oito gêneros e seis famílias (Tabela 1 e Figura 8 a e b).1
Tabela 1: Espécies de pteridófitas registradas na mata de galeria do Parque Municipal Mário Viana, Nova Xavantina-MT.

A família com maior representatividade específica foi Pteridaceae (quatro espécies, 36,40% do total), seguida por Thelypteridaceae (duas espécies, 18,20%), Hymenophyllaceae, Dennstaedtiaceae e Schizaeaceae (todas com uma espécie cada, 9,09%) (Figura 9). Souza (2003) em estudos realizados com pteridófitas em duas áreas de mata de galeria, sendo uma delas correspondente à mesma área analisada no presente estudo, constatou também que a família Pteridaceae foi a mais representativa em número de espécies para ambas as áreas, sendo representada por 23,6% do total de 17 espécies inventariadas nas áreas. Já as análises de Athayde Filho & Windisch (2003), envolvendo a pteridoflora de três fitofisionomias do mesmo Parque (cerradão, mata de galeria e vereda), apontaram que a família Pteridaceae apresentou a maior riqueza especifica com 21% de um total de 24 espécies listadas, sendo que o percentual de representatividade específica de Pteridaceae também se manteve para a pteridoflora da mata de galeria analisada no mencionado estudo.
Os trabalhos de Souza (2001), também desenvolvidos com pteridófitas, porém em quatro fitofisionomias distintas do Cerrado (área de bacurizal úmida, mata de galeria inundável, área antropizada e mata ciliar) mostraram que, apesar da diversidade de habitats, Pteridaceae foi representada por apenas 7,7% do total de 26 espécies levantadas nas áreas.
Em termos relativos, a representatividade específica exibida pela família Pteridaceae no presente estudo (36,40% do total de 11 espécies) foi superior às verificadas em outros estudos em matas de galeria ou outras fitofisionomias (Souza 2001; Athayde Filho & Windisch 2003; Souza 2003), sendo superior inclusive aos valores encontrados nos estudos preliminares de Mendonça et al. (1998) para todo o bioma Cerrado, quando na ocasião estimaram que do total de 155 espécies pteridofíticas listadas para as matas de galeria do referido bioma cerca de 8,97% das espécies pertenciam à família Pteridaceae.
Provavelmente a alta representatividade específica exibida por Pteridaceae no presente estudo em relação aos trabalhos anteriormente mencionados, decorra do fato da área amostrada na mata de galeria do Bacaba ser heterogênea quanto a aspectos topográficos, pedológicos, hidrológicos, florísticos entre outros (Marimon et al. 2002; Marimon et al. 2003) proporcionando uma variedade de microhabitats, desse modo favorecendo o estabelecimento de várias espécies de Pteridaceae que demonstram preferências ambientais distintas, como é o caso de Pityrogramma calomelanos que ocorre em matas com vegetação menos densa e em proximidades de lagoas (Sehnem 1972; Windisch 1992) (trecho dois), bem como Adiantum serratodentatum, espécie frequentemente encontrada no interior da mata próxima à corrente de água (Sehnem 1972) (trechos um e dois).
Quanto à curva do coletor (Figura 10), pode-se observar que ela tendeu à estabilização, mas que ainda não ocorreu, indicando assim que, provavelmente, nem todas as espécies presentes na área foram amostradas. E esta constatação pode ser também verificada analisando-se a curva do estimador ICE, que aponta provavelmente, a ocorrência de outras seis espécies que potencialmente ainda ocorreriam na área. Dentre as possíveis explicações para tal situação observada, é possível mencionar: presença de espécies de dossel, cuja localização é difícil; presença de espécies de tamanho reduzido crescendo junto a briófitas, dificultando assim sua localização; outras espécies ainda desconhecidas para a área, com padrão sazonal específico, não sendo localizada durante a execução dos trabalhos, entre outras.
.jpg)
Figura 9: Representatividade e riqueza específica das famílias de pteridófitas na mata de galeria do Parque Municipal Mário Viana, Nova Xavantina-MT. Pte.: Pteridaceae; Hym.; Hymenophyllaceae; Den.: Dennstaedtiaceae; The.: Thelypteridaceae; Sch.: Schizaeaceae e Pol.: Polypodiaceae.
.jpg)
Figura 10: Curva do coletor para as espécies de pteridófitas na mata de galeria do Parque Municipal Mário Viana, Nova Xavantina-MT. ICE: estimador de diversidade; Coleman: curva cumulativa de espécies; Log. (ICE): representação logarítimica (suavizada) do estimador (ICE).
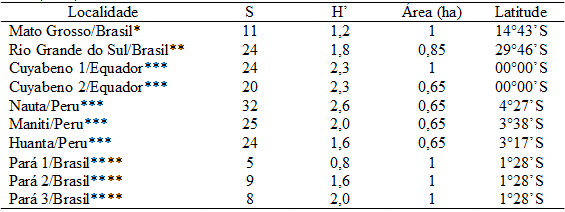
A diversidade floristica de pteridófitas calculada para a área foi H’= 1,26 nats/indivíduo e a equabilidade foi J= 0,53. De certo modo, a diversidade de espécies para a área foi baixa quando comparada aos valores de diversidade determinados por Tuomisto & Poulsen (2000), em estudos realizados com pteridófitas na Amazônia peruana e equatoriana, bem como aos trabalhos de Athayde Filho (2002) e Rodrigues et al. (2004) desenvolvidos com pteridófitas, nos Estados brasileiros do Rio Grande do Sul e Pará (Tabela 2), respectivamente. Como se pode notar, apesar da maior parte dos referidos estudos ter sido realizados em áreas inferiores a 1 ha, todos os valores de diversidades, com exceção do Pará 1 (H’=0,80), foram superiores ao obtido no presente estudo.
Odum (1988) e Gotllieb et al. (1996) assinalam a influência natural do gradiente latitudinal sobre a diversidade biológica global. Para os referidos autores diversidade de espécies tende a aumentar desde as altas latitudes em direção ao Equador. Fernandes (1998) e Primarck & Rodrigues (2001) também assinalam a influência de diferenças topográficas, climáticas e do próprio meio ambiente sobre os padrões de riquezas de espécies de localidades distintas. No entanto, para qualquer correlação destas prováveis influências sobre os padrões de diversidade das pteridófitas, torna-se necessário a realização estudos posteriores mais detalhados.
Tabela 2: Estudos referentes à diversidade de pteridófitas realizados na América do Sul. S: riqueza de espécies; H’: diversidade de Shannon-Wienner. *Informações levantadas no presente estudo, **Athayde Filho (2002), ***Tuomisto & Poulsen (2000) e ****Rodrigues et al. (2004).
Na Figura 11, nota-se a inclinação da curva do componente dominância da diversidade, caracterizada pela dominância ecológica de algumas espécies (Adiantum serratodentatum, Adiantum diogoanum e Pityrogramma calomelanos) revelando uma baixa uniformidade entre as espécies analisadas. Para Odum (1988) o tipo de curva sigmoidal, como a observada na Figura 11, é obtida na maioria das distribuições naturais dos indivíduos. É um modelo frequentemente observado em comunidades tropicais relativamente não perturbadas.
.jpg)
Figura 11: Curva do componente dominância da diversidade das espécies de pteridófitas na mata de galeria do Parque Municipal Mário Viana, Nova Xavantina-MT. Aser.: Adiantum serratodentatum; Adio.: Adiantum diogoanum; Pcal.: Pityrogramma calomelanos; Alat.: Adiantum latifolium; Tpin.: Trichomanes pinnatum; Ppol.: Polypodium polypodioides; Lven.: Lygodium venustum; Paqu.: Pteridium aquilinum; Mlin.: Microgramma lindbergii.; Tsp.: Thelypteris sp. e Tser.: Thelypteris serrata.
Dentre as 11 espécies de pteridófitas registradas na área estudada, oito ocorreram no trecho um e seis no dois, sendo que destas, três foram comuns a ambos os trechos (Tabela 1). Neste caso, a similaridade florística obtida, utilizando o índice de Sørensen, foi S= 0,43, sendo então ligeiramente baixa, revelando poucas semelhanças entre os trechos estudados.
Genevro (2004), em estudos realizados com briófitas, utilizando o mesmo índice, também constatou baixa similaridade florística (S=0,45) entre as mesmas áreas. Marimon et al. (2002), estudando espécies arbóreas da flora fanerogâmica em três porções da mesma mata de galeria, concluíram que as porções do alto e do baixo (respectivamente os trechos um e dois do presente trabalho) apresentaram baixa similaridade florística.
Marimon et al. (2003) estudaram os padrões de distribuição de espécies arbóreas em relação a fatores ambientais nas mesmas porções de mata, verificaram que as espécies analisadas formam comunidades florísticas distintas as quais se encontram associadas às variações do nível do lençol freático, constatada desde a margem do córrego até a borda da mata, bem como de um gradiente topográfico caracterizado por declividade acentuada na porção superior do canal do córrego (42%) até uma baixa declividade, em torno de 5% na porção inferior (baixo), sugerindo uma influência de tais fatores sobre a organização flora.
Assim, da mesma forma há fortes indícios que fatores abióticos como a topografia e o nível do lençol freático, que de acordo com Marimon et al. (2003), diferem entre os trechos, provavelmente possam estar favorecendo a ocorrência de várias espécies de pteridófitas em detrimento de outras, compondo floras relativamente distintas em cada trecho analisado. Assim, possivelmente, espécies de pteridófitas com baixa tolerância para as pronunciadas variações da topografia e do lençol freático entre as áreas, tiveram sua ocorrência restrita ao trecho que apresenta fatores mais próximos de seu ótimo ecológico. Em contrapartida, algumas espécies aparentemente mais tolerantes às mencionadas variações, ocorreram em ambos os trechos analisados (Tabela 1).
O índice de Jaccard foi de C= 0,27, indicando que os trechos estudados são floristicamete similares. Provavelmente a diferença verificada entre os valores demonstrados pelos índices de Sørensen e Jaccard nas análises da pteridoflora da floresta do Bacaba, decorra do fato do primeiro índice atribuir maior peso às espécies de pteridófitas comuns aos trechos, entretanto não atribuídos pelo segundo, gerando tal situação. Contudo, este quadro descrito por ambos os índices sugere, de modo generalizado, que os trechos são similares, e que se deve atentar para o fato de ambos os índices serem distintos e atribuírem pesos diferentes às espécies da flora analisada.
5.2. Fitossociologia
Ao longo das 400 parcelas demarcadas (1 ha) foram amostrados 3.418 indivíduos da pteridoflora. Rodrigues et al. (2004) estimaram para uma Floresta Densa de Terra Firme na Amazônia um total de 5000 indivíduos, em um Igapó encontraram 4467 indivíduos e em uma Floresta de Transição, 1067 indivíduos. Athayde Filho (2002), em trabalhos realizados em área menor (0,85 ha) levantou 9731 indivíduos de pteridófitas.
A baixa abundância das pteridófitas verificada no presente estudo, em relação aos trabalhos anteriormente mencionados, provavelmente esteja associada às possíveis diferenças no período de execução de cada pesquisa, bem como às diferenças climáticas de cada região. Haja vista que o período de realização dos trabalhos de campo do presente estudo coincidiu com os meses em que o nível do lençol freático da área se aprofunda (Marimon et al. 2003), provavelmente influenciando negativamente sobre a abundância de pteridófitas no local.
Odum (1988) discorre exaustivamente sobre o efeito de fatores limitantes (bióticos e/ou abióticos) sobre a abundância das populações, principalmente quando envolve populações com estreita tolerância às pronunciadas variações hidrológicas, como é o caso das pteridófitas, fator decisivo para a sua sobrevivência e reprodução (Windisch 1992; Raven et al. 2001). Merece destaque também o fato das áreas analisadas por Rodrigues et al. (2004) estarem em meio à floresta Amazônica e aquela analisada por Athayde Filho (2002) em floresta de restinga sofrendo influência direta da Floresta Atlântica, ambas com histórico de alta riqueza e diversidade florística (Tabela 2).
As espécies de pteridófitas analisadas no presente estudo estiveram presentes em apenas 182 parcelas (45,50%), do total de parcelas amostradas. Destas, 143 (78,57%) localizam-se no segundo trecho enquanto que apenas 39 (21,43%) no primeiro. Este quadro parece estar relacionado às diferenças do nível do lençol freático de cada trecho, descritas por Marimon et al. (2003), bem como a disponibilidade de substrato preferencial para a ocupação de pteridófitas (Athayde Filho & Windisch 2003; Souza 2003). Provavelmente pelo fato do segundo trecho apresentar o nível do lençol freático mais raso (maior disponibilidade de água para as plantas) em relação ao primeiro trecho, possa ter determinado a ocupação de uma área relativamente maior pelas espécies naquela porção de mata.
Todavia, o fato do lençol freático diferir na superfície também pode ser limitante no que ser refere à ocupação espacial pelas espécies, já que apenas organismos adaptados a esta situação sobreviveriam, como por exemplo Pteridium aquilinum e Thelypteris sp. Para o trecho um, como boa parte do substrato disponível é rochoso, um outro fator limitante surge claramente, agindo como seletor de espécies, como observado em e Polypodium polypodioides com preferência por substrato rochoso (Sehnem 1970; Souza 2003).
Adiantum serratodentatum foi a espécie presente em maior número de parcelas (80), seguida por Pityrogramma calomelanos (48), Adiantum diogoanum (23) e Adiantum latifolium (17). Enquanto que Thelypteris serrata, Thelypteris sp., Pteridium aquilinum e Microgramma lindbergii foram as espécies presentes em menor número de parcelas, uma parcela ocupada por cada espécie (Tabela 3).
O número de indivíduos por parcela variou de 0 a 126, com média de 8,55 indivíduos/25 m2, desvio padrão de s= 19,54 e coeficiente de variação de CV= 228,54% (Mediana de 11 indivíduos/ m2). O elevado valor apresentado pelo coeficiente de variação no presente estudo decorre do fato de alguns dados levantados em cada parcela, acerca do número de indivíduos, serem discrepantes como aqueles observados anteriormente (0 a 126 indivíduos/25 m2), e a média tratar-se de uma medida-resumo sensível a tais dados, acarretando naturalmente esta variação do valor médio como fora assinalada por Pagano & Gauvreau (2004) e Vieira (2004).
Provavelmente a heterogeneidade verificada na área estudada com relação aos aspectos topográficos, pedológicos, hidrológicos (lençol freático) e da flora fanerogâmica (Marimon et al. 2002; Marimon et al. 2003), possam ter determinados os referidos valores discrepantes levantados no presente estudo. Ao passo que os mencionados aspectos possam estar favorecendo a ocupação de determinadas localidades da área amostrada por um elevado número de indivíduos de pteridófitas (parcelas com elevado número de indivíduos) e, ao mesmo tempo, limitando o estabelecimento das espécies analisadas nas demais localidades da área (parcelas com baixo número de indivíduos ou até mesmo vazias).
Athayde Filho (2002) constatou uma média de indivíduos relativamente maior para parcelas de 25 m2 (28 indivíduos/25 m2). Entretanto deve ser lembrado que a abundância de pteridófitas verificadas pelo referido autor (9731 indivíduos) foi consideravelmente superior à constatada no presente estudo (3418 indivíduos), como também o número de parcelas e a área de mata por ele analisada foram relativamente menores (338 parcelas/0,85 ha).
A espécie que apresentou maior número de indivíduos foi Adiantum serratodentatum (1583 indivíduos), seguida por Adiantum diogoanum (960), Pityrogramma calomelanos (601 indivíduos) e Adiantum latifolium (247), somando 3391 (99,21%) do total de indivíduos analisados (Tabela 3).
Dentre as espécies amostradas, Thelypteris serrata e Thelypteris sp. apresentaram somente um indivíduo. Uma problemática preocupante acerca das espécies que apresentam um único indivíduo como as mencionadas anteriormente, diz respeito a um potencial evento de extinção das mesmas no local, podendo ser causada por eventos naturais, por ação antrópica descontrolada e até por pesquisadores desatentos. Primarck & Rodrigues (2001) chamam a atenção para populações com número reduzido de indivíduos, as quais são susceptíveis a serem extintas em uma determinada localidade. Contudo vale lembrar que o presente estudo foi realizado em apenas um hectare da floresta de galeria do Parque, podendo haver outros indivíduos das referidas espécies distribuídos em outras localidades da mata.
A espécie com maior densidade relativa (DR) foi Adiantum serratodentatum (46,31%), seguida por Adiantum diogoanum (28,09%), Pityrogramma calomelanos (17,58%) e Adiantum latifolium (7,23%), totalizando 99,21% da densidade de espécies para a área. Desta forma, as sete espécies restantes somaram apenas 0,79% da densidade local (Tabela 3).
Desse modo, 99,21% dos indivíduos analisados pertenciam à família Pteridaceae; 0,32%; a Hymenophyllaceae; 0,26% a Polypodiaceae; 0,09% a Schizaeaceae; 0,06% a Dennstaedtiaceae e 0,06% pertenciam a Thelypteridaceae. Na área estudada por Athayde Filho (2002) a família de pteridófita que apresentou maior densidade relativa foi Blechnaceae (42,92%), sendo que Pteridaceae não foi representada. Enquanto que, nos trabalhos de Rodrigues et al. (2004), a família com maior densidade foi Vittariaceae (40,67%), sendo que Pteridaceae apresentou densidade relativa de apenas 2,65%.
A elevada representatividade exibida pela família Pteridaceae no parâmetro densidade, verificada no presente estudo, provavelmente decorre do fato desta família ter apresentado a maior riqueza (Figura 9) de espécies e estas espécies serem aparentemente mais tolerantes às variações topográficas, pedológicas, hidrológicas entre outras (Marimon et al. 2002; Marimon et al. 2003), da área estudada em relação às demais espécies da comunidade analisada. Para Martins (1993) a dominância por família parece ser muito freqüente em florestas tropicais.
Tabela 3: Parâmetros fitossociológicos das espécies de pteridófitas analisadas na mata de galeria do Parque Municipal Mário Viana, Nova Xavantina-MT. Ni: número de indivíduos ocorrentes na área; Ui: número de unidades amostrais que as espécies ocorrem; DR: densidade relativa; FR: frenquência relativa; DoR: dominância relativa; VI: valor de importância; VI(%): valor relativo de importância; Alt. Méd.: altura média; Alt. Máx.: altura máxima e Alt. Min.: altura mínima.
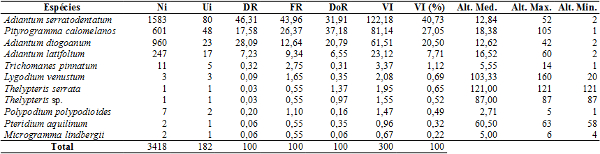
Adiantum serratodentatum apresentou, também, a maior freqüência relativa (FR) na área (43,96%), seguida por Pityrogramma calomelanos (26,37%), Adiantum diogoanum (12,64%) e Adiantum latifolium (9,34), totalizando 92,31% da freqüência total das espécies. Em contrapartida, as sete espécies restantes contabilizaram apenas 7,69% de freqüência total (Tabela 3). As elevadas freqüências apresentadas pelas quatro espécies da família Pteridaceae, provavelmente, resultem de uma maior tolerância que as referidas espécies venham a apresentar diante das variações na topografia, dos substratos disponíveis, do nível do lençol freático entre outras, de cada trecho analisado.
Assim, a família Pteridaceae esteve presente em 92,30% das parcelas confeccionadas, seguida por Hymenophyllaceae (2,75%), Schizaeaceae (1,65%) e Polypodiaceae (1,1%). Enquanto que as famílias restantes representaram pouco mais de 2% da freqüência total.
A respeito da dominância relativa (DoR%) das pteridófitas, observou-se que apesar de Pityrogramma calomelanos apresentar a terceira maior densidade da comunidade, foi a espécie de maior dominância (37,18%), seguida por Adiantum serratodentatum (31,91%), Adiantum diogoanum (20,79%) e Adiantum latifolium (6,55%), totalizando 96,43%. Desse modo, ficou clara a expressiva dominância destas espécies na comunidade. Em ordem decrescente de importância, os aspectos determinantes para a elevada dominância exibida pela primeira espécie, apesar de não ser a mais densa na comunidade, foi a área de cobertura ocupada por cada indivíduo que, em média, foi maior em relação às áreas individuais das demais.
Os aspectos determinantes da dominância observada em Adiantum serratodentatum, Adiantum diogoanum e Adiantum latifolium estão, em primeiro plano, associados à densidade e, em segundo, à área de cobertura individual de cada espécie. Haja vista que a área de cobertura individual de cada espécie não apresentou significativas variações, sendo a densidade o fator preponderante para o estabelecimento de suas respectivas dominâncias. Em contrapartida, com mais de 3%, as demais espécies demonstraram pequenos valores de dominância na comunidade (Tabela 3). No estudo de Athayde Filho (2002) podem-se observar também mudanças nos parâmetros densidade e freqüência
Com 96,43% do valor de dominância, a família Pteridaceae dominou a área. Enquanto que as demais famílias apresentaram pequenos valores relativos de dominância, somando pouco mais de 3%.
Quanto ao valor relativo de importância (VI%) distinguiu-se dois grupos de pteridófitas com valores completamente distintos. O primeiro grupo foi composto por espécies da família Pteridaceae que reuniu, em ordem decrescente de importância, as quatro espécies mais importantes da comunidade analisada, sendo elas: Adiantum serratodentatum (40,73%), seguida por Pityrogramma calomelanos (27,05%), Adiantum diogoanum (20,50%) e Adiantum latifolium (7,71%), que compuseram mais de 95% do valor de importância total. De um modo geral, os parâmetros determinantes para o maior VI exibido pela primeira espécie foram os elevados valores relativos da densidade e freqüência. Os parâmetros responsáveis pelo valor de importância demonstrado pela segunda espécie foram os elevados valores relativos da freqüência e dominância. Enquanto que os valores demonstrados pela terceira e quarta espécies decorrem das diferenças verificadas em todos os componentes dos VIs das mesmas em relação às espécies subseqüentes (Tabela 3).
Nos estudos de Athayde Filho (2002), foi verificado um padrão semelhante ao exibido pelas espécies mais importantes na composição do valor de importância para a comunidade analisada no presente estudo. Nos referidos estudos quatro espécies também apresentaram os maiores VIs, entretanto com a família Blechnaceae representando o maior percentual (40,86%), padrão este observado também na densidade e freqüência relativas do mesmo estudo. No entanto, torna-se necessário a realização de estudos posteriores que averigúem se este padrão também se repete em outras áreas ou se trata de uma mera coincidência.
O segundo grupo, por sua vez, reúne os VIs de todas as espécies restantes que somaram pouco mais de 4% do valor de importância na comunidade (Tabela 3).
Com relação à altura das espécies de pteridófitas, Thelypteris serrata apresentou a maior (121 cm), seguido por Lygodium venustum (103,33 cm), Thelypteris sp. (87 cm) e Pteridium aquilinum (60,5 cm). A menor média foi registrada para Polypodium polypodioides (2,71 cm) (Tabela 3). Assim, a altura média da comunidade de pteridófitas analisada foi 14,13 cm. A pteridoflora analisada por Athayde Filho (2002) apresentou uma média de altura consideravelmente maior que a observada no presente estudo, 34,05 cm.
Uma observação importante no que se refere às variações de altura dos indivíduos observados é que, por exemplo, Lygodium venustum, normalmente se porta como hemiepífita, utilizando outras plantas como escora, mas ainda mantendo contato com o solo (Sehnem 1974; Windisch 1992; Souza 2003), daí sua elevada altura média. Thelypteris serrata, Thelypteris sp. e Pteridium aquilinum, são espécies que ocorrem em ambientes alagados e/ou com grande competição por luz, já que normalmente desenvolvem longas frondes, com extensos pecíolos corroborando com os aspectos discutidos por Rizzini (1997) para espécies vegetais de ambientes com pouca luminosidade. Para o referido autor tais espécies tendem a apresentar maior desenvolvimento, resultando em indivíduos maiores com folhas robustas. E por fim, Polypodium polypodioides é uma planta de crescimento reptante e de frondes discretas, crescendo sempre sobre rochas ou outras plantas, como epífitas, daí sua baixa estatura (Sehnem 1970).
Cerca de 94,32% dos indivíduos analisados foram enquadrados na primeira classe de altura (Classe 1: 0-30 cm); 4,94% enquadraram-se na Classe 2 (31-60 cm); 0,61% compuseram a Classe 3 (61-90 cm); 0,03% enquadraram-se na Classe 4 (91-120 cm); 0,07% ocuparam a Classe 5 (121-150 cm) e 0,03% compuseram a sexta classe de altura (Calsse 6: 151-180 cm). Athayde Filho (2002) apresentou valores muito próximos aos obtidos no presente estudo, apesar de ter adotado uma intervalo de classe superior (IC=50 cm). Assim, conforme o referido autor, do total de indivíduos analisados (9731) o maior percentual (89,68%) também foi enquadrado na primeira classe de altura (até 50 cm).
6. Considerações Finais
A partir do presente estudo foi possível compreender alguns aspectos ecológicos importantes da pteridoflora da região, principalmente no que se refere à fitossociologia de pteridófitas no Cerrado mato-grossense, área ainda pouco estudada.
Foram identificadas 11 espécies de pteridófitas na área estudada e dentre as famílias analisadas, Pteridaceae apresentou maior riqueza específica.
Constatou-se, ainda, que a diversidade de pteridófitas na área é baixa quando comparada a outros estudos realizados com pteridófitas no Brasil e em outros países da América do Sul.
Observou-se, também, que os trechos analisados são similares (índices de Sørensen e Jaccard). Apesar do valor encontrado pelo índice de Sørensen apontar um valor ligeiramente abaixo do valor de refêrencia para a análise, demonstra uma forte tendência à similaridade.
Nos estudos fitossociológicos foram analisados 3418 indivíduos da pteridoflora local. Adiantum serratodentatum foi a espécie mais importante na comunidade, apresentou a maior densidade relativa e a maior freqüência relativa na área, enquanto que Pityrogramma calomelanos foi a espécie dominante. Provavelmente Adiantum serratodentatum ocupe posição de destaque na comunidade resultante de uma maior tolerância que a referida espécie possa apresentar frente às variações ambientais verificadas em cada trecho.
A espécie com maior média de altura na comunidade foi Thelypteris serrata, enquanto que a menor foi Polypodium polypodioides. E a altura média da comunidade foi 14,13 cm. Cerca de 94,32% dos indivíduos apresentaram alturas que variaram entre 0 e 30 cm. Enquanto que apenas 0,03% mediram entre 151 e 180 cm. Padrões de valores similares forma registrados em estudos anteriores realizados com pteridófitas.
Recomenda-se a realização de estudos posteriores que dêem continuidade ao crescente e importante conhecimento acerca da ecologia das pteridófitas ocorrentes no Cerrado brasileiro.
7. Referências Bibliográficas
Athayde Filho, F. P. 2002. Análise da pteridoflora em uma mata da restinga na região de Capão da Canoa, Rio Grande do Sul, Brasil. Dissertação de Mestrado, Universidade do Vale do Rio dos Sinos, São Leopoldo, 177p.
Athayde Filho, F.P. & Agostinho, A.A. 2005. Pteridofloara de duas veredas no município de Campinápolis, Mato Grosso, Brasil. Pesquisas, Bot. 56:145-160.
Athayde Filho, F. P. & Windisch, P. G. 2003. Análise da pteridoflora da Reserve Biológica Mário Viana, Município de Nova Xavantina, Estado de Mato Grosso (Brasil). Bradea 9(13): 67-76.
Batista Neto, J.P. 2002. Levantamento florístico e fitossocilógico em campo de murundum no pantanal Mortes-Araguaia, Cocalinho-MT. Trabalho de Conclusão de Curso, Departamento de Ciências Biológicas da Universidade do Estado de Mato Grosso, Campus de Nova Xavantina, Nova Xavantina, 25p.
Colwell, R.K. 1997. EstimateS 5. Statistical estimation of species richness and shared species from samples. User’s guide. Connecticut, 22p.
Durigan, G. 2003. Métodos para análise de vegetação arbórea. Pp. 455-479. In: L. Cullen Jr.; R. Rudran & C. Valladares-Pádua (Orgs.). Métodos de estudo em biologia da conservação e manejo da vida silvestre. Curitiba, Editora UFPR / Fundação O Boticário.
Eiten, G. 1993. Vegetação do Cerrado Pp.17-73. In: Cerrado: caracterização, ocupação e perspectivas (M. N. Pinto, coord.). 2.ed. Brasília, Universidade de Brasília, 681p.
Felfili, J. M; Nogueira, P.E; Silva-Júnior, M.C; Marimon, B.S; Delitti, W.B.C. 2002. Composição florística e fitossociologia do cerrado sentido restrito no município de Água Boa - MT. Acta Bot. Bras. 16(1):103-112.
Fernandes, A. 1998. Fitogeografia Brasileira. Fortaleza, Multigraf, 340p.
Ferreira, J.C. 2001. Mato Grosso e Seus Municípios. Cuiabá, Secretaria de Estado da Educação, 660p.
Fonseca, M. S. & Silva Júnior, M. C. 2004. Fitossociologia e similaridade florística entre trechos de Cerrado sentido restrito em interflúvio e em vale no Jardim Botânico de Brasília, DF. Acta Bot. Bras.18(1):19-29.
Genevro, J.A. 2004. Briófitas de Mata de Galeria no Parque Municipal Mário Viana, Nova Xavantina-MT. Trabalho de Conclusão de Curso, Departamento de Ciências Biológicas da Universidade do Estado de Mato Grosso, Campus de Nova Xavantina, 66p.
Gottlieb, O.R; Kaplan, M.A.C. & Borin, M.R.M.O. 1996. Biodiversidade: um enfoque químico-biológico. Rio de Janeiro, UFRJ.267p.
Guarino, E. S. G. & Walter, B. M. T. 2005. Fitossociologia de dois trechos inundáveis de Matas de Galeria no Distrito Federal, Brasil. Acta Bot. Bras. 19(3):431-442.
Lee, S.M. & Chao, A. 1994. Estimating population size via sample coverage for closed capture-recapture models. Biometrics, 50:88-97.
Marimon, B.S.; Felfili, J.M. & Lima, E.S. 2002. Floristics and Phytossocilogy of the gallery forest of the Bacaba stream, Nova Xavantina, Mato Grosso, Brazil. Edinburgh Journal of Botany 59(2): 303-318.
Marimon, B.S.; Felfili, M.J.; Lima, E.S e Pinheiro-Neto, J. 2003. Padrões de distribuição de espécies na mata de galeria do córrego bacaba, Nova Xavantina, Mato Grosso, em relação a fatores ambientais. Brasília, DF. Boletim do Herbário Ezechias Paulo Heringer 12:1-108.
Marimon, B.S. 2005. Dinâmica de uma floresta monodominante de Brosimum rubescens Taub. e comparação com uma floresta mista em Nova Xavantina-MT. Tese de doutorado, Universidade de Brasília, Brasília.
Martins, F.R. 1993. Estrutura de uma floresta mesófila. 2.ed. Campinas, UNICAMP, 246p.
Mendonça, R.C. de; Felfili, J.M.; Walter, B.M.T.; Silva-Júnior, M.C. da; Rezende, A.V.; Filgueiras, T.S. & Ernane, P.E. 1998. Flora Vascular do Cerrado. In: Cerrado: ambiente e flora (S. M. Sano & S.P. de Almeida, coord.). Planaltina, EMBRAPA, 556 p.
Miranda, L. & Amorin, L. 2000. Mato Grosso: Atlas Geográfico. Cuiabá, Entrelinhas, 40p.
Miranda, E. E. de; Coutinho, A. C. (Coord.). 2004. Brasil Visto do spaço. Campinas, Embrapa Monitoramento por Satélite. Disponível em: http://www.cdbrasil.cnpm.embrapa.br>. Acesso em: 27 jan. 2006.
Nova Xavantina (município). 2002. Decreto-lei no 975 de 12 de agosto de 2002. Dispõe sobre a criação do Parque Municipal de Preservação Permanente e dá outras providencias. Palácio dos Pioneiros – Gabinete do Prefeito Municipal, Nova Xavantina, 2p.
Odum, P.G. 1988. Ecologia. Rio de Janeiro, Guanabara Koogan, 434p.
Pagano, M. & Gauvreau, K. 2004. Princípios de bioestatística. São Paulo, Pioneira Thonson Learning, 506p.
Piaia, I.I. 1999. Geografia de Mato Grosso. 2.ed. Cuiabá, EdUNIC, 184p.
Primarck, R.B. & Rodrigues, E. 2001. Biologia da conservação. Londrina, E. Rodrigues, 328p.
Raven, P.H.; Evert, R.F. & Eichorn, S.E. 2001. Biologia Vegetal. 6.ed. Rio de Janeiro: Guanabara Koogan, 906p.
Ribeiro, J.F. & Walter, B.M.T. 1998. Fitofisionomias do Bioma Cerrado Pp. 89-152. In: Cerrado: ambiente e flora (S. M. Sano & S. P. de Almeida, coord.). Planaltina, EMBRAPA, 556p.
Ricklefs, R.E. 2001. A Economia da Natureza. 5.ed. Rio de Janeiro, Guanabara Koogan, 503p.
Rizzine, C.T.1997. Tratado de Fitogeografia do Brasil: aspectos ecológicos, sociológicos e florísticos. Rio de Janeiro, Âmbito Cultural Edições Ltda.
Rodrigues, S. T.; Almeida, S.S.; Andrade, L.H.C.; Barros, I.C.L.; Van Den Berg, M.E. 2004. Composição florística e abundância de pteridófitas em três ambientes da bacia do rio Guamá, Belém, Pará, Brasil. Acta Amaz 34(1):35-42.
Rossete, A.N. & Ivanauskas, N.M. 2000. Mapeamento do Meio Físico e da Vegetação do Parque Municipal Mário Viana. Relatório científico, Nova Xavantina-MT.
Sambuichi, R.H.S. 2002. Fitossociologia e diversidade de espécies arbóreas em Cabruca (Mata raleada sobre plantação de cacau) na região sul da Bahia, Brasil. Acta. bot. bras., 16(1):89-101.
Schmitt, J.L. 2001. Desenvolvimento da fase esporofítica de Alsophila setosa Kaulf. (Pteridophyta, Cyatheaceae) em duas formações florestais no Estado do Rio Grande do Sul, Brasil. Dissertação de mestrado. São Leopoldo, Universidade do Vale do Rio dos Sinos, 106p.
Sehnem, A. 1970. Polipodiáceas. Pp. 156-158. In: R. Reitz (ed.). Flora Ilustrada Catarinense. Herbário Barbosa Rodrigues, Itajaí.
______. 1972. Pteridáceas. Pp. 200-202. In: R.Reitz (ed.). Flora Ilustrada Catarinense. Herbário Barbosa Rodrigues, Itajaí.
______.1974. Esquizeáceas. Pp. 14-17. In: R. Reitz (ed.). Flora Ilustrada Catarinense. Herbário Barbosa Rodrigues, Itajaí.
Silva, L. O.; Costa, D.A.; Filho, K.E.S.; Ferreira, H.D.; Brandão, D. 2002. Levantamento florístico e fitossociológico em duas áreas de cerrado sensu stricto no Parque Estadual da Serra de Caldas Novas, Goiás. Acta Bot. Bras.16(1):43-53.
Silva-Júnior, M.C. 2004. Fitossociologia e estrutura diamétrica da mata de galeria do Taquara, na reserva ecológica do IBGE, DF. Rev. Árvore.28(3):419-428.
Souza, A.L.; Silva, G.F.; Chichorro, J.F.; Caraciolo, R.L. 2002. Mata Nativa-Sistema para análise fitossociológica e elaboração de planos de manejo de florestas nativas: manual do usuário. Viçosa, Cientec, 126 p.
Souza, D.J. 2001. Levantamento da diversidade de pteridophyta na fazenda Boa Sorte, município de Nova Xavantina-MT. Monografia de Conclusão de Curso. Universidade do Estado de Mato Grosso, Nova Xavantina, 29p.
Souza, J.G. 2003. Levantamento das Espécies de Pteridófitas nas Margens dos Córregos Bacaba e Salgadinho, no Município de Nova Xavantina-MT. Trabalho de Conclusão de Curso, Departamento de Ciências Biológicas da Universidade do Estado de Mato Grosso, Campus de Nova Xavantina, Nova Xavantina, 34p.
Tryon, R.M. & Tryon, A.F. 1982. Ferns na allied plants, with special reference to tropical America. New York, Springer-Verlog, 857p.
Tuomisto, H. & Poulsen, A.D. 2000. Pteridophyte diversity and species composition in tour Amazonian rain florests. Journal of vegetation Science 11: 383-396.
Vieira, S. 2004. Bioestatística: tópicos avançados. 2.ed. Rio de Janeiro, Elsevier, 216p.
Windisch, P.G. 1975. Contribuição ao conhecimento das pteridófitas sa Serra Ricardo Franco (Estado de Mato Grosso). Bradea 2(1): 1-4.
______.1985. Pteridófitas do Estado de Mato Grosso. Bradea 4(28): 180-187.
______.1994. Pteridófitas do Estado de Mato Grosso – Gleicheniaceae. Bradea 6(37): 304-311.
______.1992. Pteridófitas da Região Norte-ocidental do Estado de São Paulo: guia para estudo e excursões. 2.ed. São José do Rio Preto, UNESP, 107p.
______.1995. Pteridófitas do Estado de Mato Grosso – Marattiaceae. Bradea 5(46): 396-399.
______.1996a. Pteridófitas do Estado de Mato Grosso – Hymenophyllaceae. Bradea 7(47): 400-423.
______.1996b. Towards Assaying Biodiversity In Brazilian Pteridophytes In: Biodiverstiy in Brazil: A First Approach.1 ed. BRASÍLIA, CNPq, p. 326.
______.1997. Pteridófitas do Estado de Mato Grosso – Psilotaceae. Bradea 7(10): 57-60.
______.1998. Pteridófitas do Estado de Mato Grosso – Osmundaceae. Bradea 8(19): 107-110.
Windisch, P.G. & Nonato, F.R. 1999. Pteridófitas do Estado de Mato Grosso, Brasil: Vittariaceae. Acta Bot. Bras. 13(3): 290-297.
Windisch, P.G. & Tryon, R.M. 2001. The Serra Ricardo Franco (State of Mato Grosso, Brazil) as probable migration route and its present fern flora. Bradea 8(39): 267-276.
8. Anexos
8.1. Anexo 1:
Modelo de ficha utilizada para as transcrições dos dados coletados em campo. Adaptada de Durigan (2003).
Anexo 2: Normas gerais para publicação de artigos na Acta Botanica Brasilica.
1. A Acta Botanica Brasilica (Acta bot. bras.) publica artigos originais em Português, Espanhol e Inglês.
2. Os artigos devem ser concisos, em quatro vias, com até 25 laudas, seqüencialmente numeradas, incluindo ilustrações e tabelas (usar fonte Times New Roman, tamanho 12, espaço entre linhas 1,5; imprimir em papel tamanho A4, margens ajustadas em 1,5 cm). A critério da Comissão Editorial, mediante entendimentos prévios, artigos mais extensos poderão ser aceitos, sendo o excedente custeado pelo(s) autor(es).
3. Palavras em latim no título ou no texto, como por exemplo: in vivo, in vitro, in loco, et al. devem estar em itálico.
4. O título deve ser escrito em caixa alta e baixa, centralizado, e deve ser citado da mesma maneira no Resumo e Abstract da mesma maneira que o título do trabalho. Se no título houver nome específico, este deve vir acompanhado dos nomes dos autores do táxon, assim como do grupo taxonômico do material tratado (ex.: Gesneriaceae, Hepaticae, etc.).
5. O(s) nome(s) do(s) autor(es) deve(m) ser escrito(s) em caixa alta e baixa, todos em seguida, com números sobrescritos que indicarão, em rodapé, a filiação Institucional e/ou fonte financiadora do trabalho (bolsas, auxílios etc.). Créditos de financiamentos devem vir em Agradecimentos, assim como vinculações do artigo a programas de pesquisa mais amplos, e não no rodapé. Autores devem fornecer os endereços completos, evitando abreviações, elegendo apenas um deles como Autor para correspondência. Se desejarem, todos os autores poderão fornecer e-mail.
6. A estrutura do trabalho deve, sempre que possível, obedecer à seguinte seqüência:
- RESUMO e ABSTRACT (em caixa alta e negrito) - texto corrido, sem referências bibliográficas, em um único parágrafo e com cerca de 200 palavras. Deve ser precedido pelo título do artigo em Português, entre parênteses. Ao final do resumo, citar até cinco palavras-chave à escolha do autor, em ordem de importância. A mesma regra se aplica ao Abstract em Inglês ou Resumen em Espanhol.
- Introdução (em caixa alta e baixa, negrito, deslocado para a esquerda): deve conter uma visão clara e concisa de: a) conhecimentos atuais no campo específico do assunto tratado; b) problemas científicos que levou(aram) o(s) autor(es) a desenvolver o trabalho; c) objetivos.
- Material e métodos (em caixa alta e baixa, negrito, deslocado para a esquerda): deve conter descrições breves, suficientes à repetição do trabalho; técnicas já publicadas devem ser apenas citadas e não descritas. Indicar o nome da(s) espécie(s) completo, inclusive com o autor. Mapas - podem ser incluídos se forem de extrema relevância e devem apresentar qualidade adequada para impressão. Todo e qualquer comentário de um procedimento utilizado para a análise de dados em Resultados deve, obrigatoriamente, estar descrito no item Material e métodos.
- Resultados e discussão (em caixa alta e baixa, negrito, deslocado para a esquerda): podem conter tabelas e figuras (gráficos, fotografias, desenhos, mapas e pranchas) estritamente necessárias à compreensão do texto. Dependendo da estrutura do trabalho, resultados e discussão poderão ser apresentados em um mesmo item ou em itens separados.
As figuras devem ser todas numeradas seqüencialmente, com algarismos arábicos, colocados no lado inferior direito; as escalas, sempre que possível, devem se situar à esquerda da figura. As tabelas devem ser seqüencialmente numeradas, em arábico com numeração independente das figuras.
Tanto as figuras como as tabelas devem ser apresentadas em folhas separadas (uma para cada figura e/ou tabela) ao final do texto (originais e 3 cópias). Para garantir a boa qualidade de impressão, as figuras não devem ultrapassar duas vezes a área útil da revista que é de 17,5 23,5 cm. Tabelas - Nomes das espécies dos táxons devem ser mencionados acompanhados dos respectivos autores. Devem constar na legenda informações da área de estudo ou do grupo taxonômico. Itens da tabela, que estejam abreviados, devem ter suas explicações na legenda.
As ilustrações devem respeitar a área útil da revista, devendo ser inseridas em coluna simples ou dupla, sem prejuízo da qualidade gráfica. Devem ser apresentadas em tinta nanquim, sobre papel vegetal ou cartolina ou em versão eletrônica, gravadas em TIF, com resolução de pelo menos 300 dpi (ideal em 600 dpi). Para pranchas ou fotografias - usar números arábicos, do lado direito das figuras ou fotos. Para gráficos - usar letras maiúsculas do lado direito.
As fotografias devem estar em papel brilhante e em branco e preto. Fotografias coloridas poderão ser aceitas a critério da Comissão Editorial, que deverá ser previamente consultada, e se o(s) autor(es) arcar(em) com os custos de impressão.
As figuras e as tabelas devem ser referidas no texto em caixa alta e baixa, de forma abreviada e sem plural (Fig. e Tab.). Todas as figuras e tabelas apresentadas devem, obrigatoriamente, ter chamada no texto.
Legendas de pranchas necessitam conter nomes dos táxons com respectivos autores. Todos os nomes dos gêneros precisam estar por extenso nas figuras e tabelas. Gráficos - enviar os arquivos em Excel. Se não estiverem em Excel, enviar cópia em papel, com boa qualidade, para reprodução.
s siglas e abreviaturas, quando utilizadas pela primeira vez, devem ser precedidas do seu significado por extenso. Ex.: Universidade Federal de Pernambuco (UFPE); Microscopia Eletrônica de Varredura (MEV).
Usar unidades de medida de modo abreviado (Ex.: 11 cm; 2,4 µm), o número separado da unidade, com exceção de percentagem (Ex.: 90%).
Escrever por extenso os números de um a dez (não os maiores), a menos que seja medida. Ex.: quatro árvores; 6,0 mm; 1,0 4,0 mm;125 exsicatas.
Em trabalhos taxonômicos o material botânico examinado deve ser selecionado de maneira a citarem-se apenas aqueles representativos do táxon em questão e na seguinte ordem: PAÍS. Estado: Município, data, fenologia, coletor(es) número do(s) coletor(es) (sigla do Herbário).
Ex.: BRASIL. São Paulo: Santo André, 3/XI/1997, fl. fr., Milanez 435 (SP).
No caso de mais de três coletores, citar o primeiro seguido de et al. Ex.: Silva et al. (atentar para o que deve ser grafado em CAIXA ALTA, Caixa Alta e Baixa, caixa baixa, negrito, itálico).
Chaves de identificação devem ser, preferencialmente, indentadas. Nomes de autores de táxons não devem aparecer. Os táxons da chave, se tratados no texto, devem ser numerados seguindo a ordem alfabética. Ex.:
|
1. Plantas terrestres |
|
2. Folhas orbiculares, mais de 10 cm diâm. ..................................2. S. orbicularis |
|
2. Folhas sagitadas, menos de 8 cm compr. .................................... 4. S. sagittalis |
|
1. Plantas aquáticas |
|
3. Flores brancas ............................................................................... 1. S. albicans |
|
3. Flores vermelhas .......................................................................... 3. S. purpurea |
O tratamento taxonômico no texto deve reservar o itálico e o negrito simultâneos apenas para os nomes de táxons válidos. Basiônimo e sinonímia aparecem apenas em itálico. Autores de nomes científicos devem ser citados de forma abreviada, de acordo com índice taxonômico do grupo em pauta (Brummit & Powell 1992 para Fanerógamas). Ex.:
1. Sepulveda albicans L., Sp. pl. 2: 25. 1753. Pertencia albicans Sw., Fl. bras. 4: 37, t. 23, f. 5. 1870. Fig. 1-12.
Subdivisões dentro de Material e métodos ou de Resultados e/ou discussão devem ser escritas em caixa alta e baixa, seguida de um traço e o texto segue a mesma linha. Ex.: Área de estudo - localiza se ...
Resultados e discussão devem estar incluídos em conclusões.
- Agradecimentos (em caixa alta e baixa, negrito, deslocado para a esquerda): devem ser sucintos; nomes de pessoas e Instituições devem ser por extenso, explicitando o porquê dos agradecimentos.
- Referências bibliográficas
- Ao longo do texto: seguir esquema autor, data. Ex.: Silva (1997), Silva & Santos (1997), Silva et al. (1997) ou Silva (1993; 1995), Santos (1995; 1997) ou (Silva 1975; Santos 1996; Oliveira 1997).
- Ao final do artigo: em caixa alta e baixa, deslocado para a esquerda; seguir ordem alfabética e cronológica de autor(es); nomes dos periódicos e títulos de livros devem ser grafados por extenso e em negrito. Exemplos:
Santos, J. 1995. Estudos anatômicos em Juncaceae. Pp. 5-22. In: Anais do XXVIII Congresso Nacional de Botânica. Aracaju 1992. São Paulo, HUCITEC Ed. v.I.
Santos, J.; Silva, A. & Oliveira, B. 1995. Notas palinológicas. Amaranthaceae. Hoehnea 33(2): 38-45.
Silva, A. & Santos, J. 1997. Rubiaceae. Pp. 27-55. In: F.C. Hoehne (ed.). Flora Brasilica. São Paulo, Secretaria da Agricultura do Estado de São Paulo.
Para maiores detalhes consulte os últimos fascículos rescentes da Revista, ou os links da mesma na internet: www.botanica.org.br. ou ainda artigos on line por intermédio de www.scielo.br/abb.
Não serão aceitas Referências bibliográficas de monografias de conclusão de curso de graduação, de citações de simples resumos simples de Congressos, Simpósios, Workshops e assemelhados. Citações de Dissertações e Teses devem ser evitadas ao máximo; se necessário, citar no corpo do texto. Ex.: J. Santos, dados não publicados ou J. Santos, comunicação pessoal.
1 A espécie Adiantum deflectens Mart. registrada por Athayde Filho & Windisch (2003) e Souza (2003) na mesma área estudada, não foi incluída na relação de espécies do presente trabalho por apresentar padrão sazonal ativo na estação chuvosa, podendo então ter sua população subestimada na área analisada.
Publicado por: Fábio Alves Rezende
O texto publicado foi encaminhado por um usuário do site por meio do canal colaborativo Monografias. Brasil Escola não se responsabiliza pelo conteúdo do artigo publicado, que é de total responsabilidade do autor . Para acessar os textos produzidos pelo site, acesse: https://www.brasilescola.com.